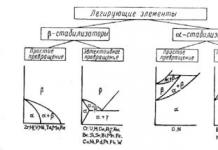
Ковалентная химическая связь обычно возникает между атомами неметаллов с одинаковой или не очень сильно различающейся электроотрицательностью. Если различие в электроотрицательности атомов, между которыми образуется химическая связь, велико (∆x превышает 1.7), то общая электронная пара практически полностью смещается к атому с большей электроотрицательностью. В результате этого образуются частицы, имеющие заряды – положительно и отрицательно заряженные ионы с устойчивой электронной конфигурацией атомов ближайшего благородного газа. Противоположно заряженные ионы прочно удерживаются силами электростатического притяжения – между ними возникает химическая связь, которая называется ионной.
Ионная связь, как правило, возникает между атомами типичных металлов и типичных неметаллов. Характерным свойством атомов металлов является то, что они легко отдают свои валентные электроны, тогда как атомы неметаллов способны легко их присоединять.
Рассмотрим возникновение ионной связи, например, между атомами натрия и атомами хлора в хлориде натрия NaCl.
Отрыв электрона от атома натрия приводит к образованию положительно заряженного иона – катиона натрия Na + .
Присоединение электрона к атому хлора приводит к образованию отрицательно заряженного иона – аниона хлора Cl — .
Между образовавшимися ионами Na + и Cl — , имеющими противоположный заряд, возникает электростатическое притяжение, в результате которого образуется соединение – хлорид натрия с ионным типом химической связи.
Ионная связь – это химическая связь, которая осуществляется за счет электростатического взаимодействия противоположно заряженных ионов.
Таким образом, процесс образования ионной связи сводится к переходу электронов от атомов натрия к атомам хлора с образованием противоположно заряженных ионов, имеющих завершенные электронные конфигурации внешних слоев.
Экспериментально установлено, что в действительности электроны не отрываются полностью от атома металла, а лишь смещаются в сторону атома хлора. Это смещение тем значительней, чем больше разность электроотрицательностей атомов, между которыми образуется ионная связь. Однако даже в случае фторида цезия CsF, в котором разность электроотрицательностей превышает 3.0, заряд атома цезия не равен 1+. Это означает, что электрон атома цезия не полностью переходит к атому фтора. В случае других соединений, для которых разность электроотрицательностей не так велика, смещение электрона еще меньше, и поэтому следует говорить об ионной химической связи с определенной долей ковалентной.
Соединения, в которых вклад ионной связи значителен, принято называть ионными. Большинство бинарных соединений, содержащих атомы металлов, являются ионными, т. е. в них химическая связь в значительной степени ионная. К числу таких соединений относятся галогениды, оксиды, сульфиды, нитриды и др.
Ионная связь возникает не только между простыми катионами и простыми анионами типа F — , Cl — , F 2- , но и между простыми катионами и сложными анионами типа NO 3 — , NO 4 2- , NO 4 3- или гидроксид-ионами ОН — . Подавляющее большинство солей и оснований являются ионными соединениями, например Na 2 SO 4 , Cu(NO 3) 2 , Mg(OH) 2 . Существуют ионные соединения, в состав которых входят сложные катионы, не содержащие атомы металла, например ион аммония NH 4 + , а также соединения, в которых сложными являются и катион, и анион, например сульфат аммония (NH 4) 2 SO 4 .
Вам необходимо включить JavaScript, чтобы проголосоватьИонная связь
Теория химической связи занимает важнейшее место в современной химии . Она объясняет, почему атомы объединяются в химические частицы , и позволяет сравнивать устойчивость этих частиц . Используя теорию химической связи , можно предсказать состав и строение различных соединений . Понятие о разрыве одних химических связей и образовании других лежит в основе современных представлений о превращениях веществ в ходе химических реакций .
Химическая связь - это взаимодействие атомов , обусловливающее устойчивость химической частицы или кристалла как целого . Химическая связь образуется за счет электростатического взаимодействия между заряженными частицами : катионами и анионами, ядрами и электронами . При сближении атомов начинают действовать силы притяжения между ядром одного атома и электронами другого, а также силы отталкивания между ядрами и между электронами . На некотором расстоянии эти силы уравновешивают друг друга , и образуется устойчивая химическая частица .
При образовании химической связи может произойти существенное перераспределение электронной плотности атомов в соединении по сравнению со свободными атомами .
В предельном случае это приводит к образованию заряженных частиц - ионов (от греческого "ион" - идущий).
1 Взаимодействие ионов
Если атом теряет один или несколько электронов , то он превращается в положительный ион - катион (в переводе с греческого – «идущий вниз »). Так образуются катионы водорода Н + , лития Li + , бария Ва 2+ . Приобретая электроны, атомы превращаются в отрицательные ионы - анионы (от греческого "анион" - идущий вверх ). Примерами анионов являются фторид ион F − , сульфид-ион S 2− .
Катионы и анионы способны притягиваться друг к другу . При этом возникает химическая связь , и образуются химические соединения . Такой тип химической связи называется ионной связью :
2 Определение Ионной связи
Ионная связь - это химическая связь, образованная за счет электростатического притяжения между катионами и анионами .
Механизм образования ионной связи можно рассмотреть на примере реакции между натрием и хлором . Атом щелочного металла легко теряет электрон , а атом галогена - приобретает . В результате этого возникает катион натрия и хлорид-ион . Они образуют соединение за счет электростатического притяжения между ними .
Взаимодействие между катионами и анионами не зависит от направления , поэтому о ионной связи говорят как о ненаправленной . Каждый катион может притягивать любое число анионов , и наоборот . Вот почему ионная связь является ненасыщенной . Число взаимодействий между ионами в твердом состоянии ограничивается лишь размерами кристалла . Поэтому "молекулой " ионного соединения следует считать весь кристалл .
Для возникновения ионной связи необходимо , чтобы сумма значений энергии ионизации E i (для образования катиона) и сродства к электрону A e (для образования аниона) должна быть энергетически выгодной . Это ограничивает образование ионной связи атомами активных металлов (элементы IA- и IIA-групп, некоторые элементы IIIA-группы и некоторые переходные элементы) и активных неметаллов (галогены, халькогены, азот).
Идеальной ионной связи практически не существует . Даже в тех соединениях, которые обычно относят к ионным , не происходит полного перехода электронов от одного атома к другому ; электроны частично остаются в общем пользовании . Так, связь во фториде лития на 80% ионная , а на 20% - ковалентная . Поэтому правильнее говорить о степени ионности (полярности ) ковалентной химической связи . Считают, что при разности электроотрицательностей элементов 2,1 связь является на 50% ионной . При большей разности соединение можно считать ионным .
Ионной моделью химической связи широко пользуются для описания свойств многих веществ , в первую очередь, соединений щелочных и щелочноземельных металлов с неметаллами . Это обусловлено простотой описания таких соединений : считают, что они построены из несжимаемых заряженных сфер , отвечающих катионам и анионам . При этом ионы стремятся расположиться таким образом, чтобы силы притяжения между ними были максимальными, а силы отталкивания - минимальными.
Ионная связь - прочная химическая связь, образующаяся между атомами с большой разностью (>1,7 по шкале Полинга) электроотрицательностей , при которой общая электронная пара полностью переходит к атому с большей электроотрицательностью. Это притяжение ионов как разноименно заряженных тел. Примером может служить соединение CsF, в котором «степень ионности» составляет 97 %.
Ионная связь - крайний случай поляризации ковалентной полярной связи . Образуется между типичными металлом и неметаллом . При этом электроны у металла полностью переходят к неметаллу . Образуются ионы.
Если химическая связь образуется между атомами, которые имеют очень большую разность электроотрицательностей (ЭО > 1.7 по Полингу) , то общая электронная пара полностью переходит к атому с большей ЭО . Результатом этого является образование соединения противоположно заряженных ионов :
Между образовавшимися ионами возникает электростатическое притяжение , которое называется ионной связью . Вернее, такой взгляд удобен . На деле ионная связь между атомами в чистом виде не реализуется нигде или почти нигде , обычно на деле связь носит частично ионный , и частично ковалентный характер . В то же время связь сложных молекулярных ионов часто может считаться чисто ионной . Важнейшие отличия ионной связи от других типов химической связи заключаются в ненаправленности и ненасыщаемости . Именно поэтому кристаллы, образованные за счёт ионной связи, тяготеют к различным плотнейшим упаковкам соответствующих ионов.
3 Ионные радиусы
В простой электростатической модели ионной связи используется понятие ионных радиусов . Сумма радиусов соседних катиона и аниона должна равняться соответстующему межъядерному расстоянию :
r 0 = r + + r −
При этом остается неясным , где следует провести границу между катионом и анионом . Сегодня известно , что чисто ионной связи не существует , так как всегда имеется некоторое перекрывание электронных облаков . Для вычисления радиусов ионов используют методы исследования , которые позволяют определять электронную плотность между двумя атомами . Межъядерное расстояние делят в точке , где электронная плотность минимальна .

Размеры иона зависят от многих факторов . При постоянном заряде иона с ростом порядкового номера (а, следовательно, заряда ядра ) ионный радиус уменьшается . Это особенно хорошо заметно в ряду лантаноидов , где ионные радиусы монотонно меняются от 117 пм для (La 3+) до 100 пм (Lu 3+) при координационном числе 6 . Этот эффект носит название лантаноидного сжатия .
В группах элементов ионные радиусы в целом увеличиваются с ростом порядкового номера . Однако для d -элементов четвертого и пятого периодов вследствие лантаноидного сжатия может произойти даже уменьшение ионного радиуса (например, от 73 пм у Zr 4+ до 72 пм у Hf 4+ при координационном числе 4).
В периоде происходит заметно уменьшение ионного радиуса , связанное с усилением притяжения электронов к ядру при одновременном росте заряда ядра и заряда самого иона : 116 пм у Na + , 86 пм у Mg 2+ , 68 пм у Al 3+ (координационное число 6). По этой же причине увеличение заряда иона приводит к уменьшению ионного радиуса для одного элемента : Fe 2+ 77 пм, Fe 3+ 63 пм, Fe 6+ 39 пм (координационное число 4).
Сравнение ионных радиусов можно проводить только при одинаковом координационном числе , поскольку оно оказывает влияние на размер иона из-за сил отталкивания между противоионами . Это хорошо видно на примере иона Ag + ; его ионных радиус равен 81, 114 и 129 пм для координационных чисел 2, 4 и 6 , соответственно .
Структура идеального ионного соединения , обусловленная максимальным притяжением между разноименными ионами и минимальным отталкиванием одноименных ионов , во многом определяется соотношением ионных радиусов катионов и анионов . Это можно показать простыми геометрическими построениями.
4 Энергия ионной связи
Энергия связ и для ионного соединения - это энергия , которая выделяется при его образовании из бесконечно удаленных друг от друга газообразных противоионов . Рассмотрение только электростатических сил соответствует около 90% от общей энергии взаимодействия , которая включает также вклад неэлектростатических сил (например, отталкивание электронных оболочек ).
При возникновении ионной связи между двумя свободными ионами энергия их притяжения определяется законом Кулона :
E(прит.) = q+ q− / (4π r ε),
где q+ и q− - заряды взаимодействующих ионов , r - расстояние между ними , ε - диэлектрическая проницаемость среды .
Так как один из зарядов отрицателен , то значение энергии также будет отрицательным .
Согласно закону Кулона , на бесконечно малых расстояниях энергия притяжения должна стать бесконечно большой . Однако этого не происходит , так как ионы не являются точечными зарядами . При сближении ионов между ними возникают силы отталкивания , обусловленные взаимодействием электронных облаков . Энергия отталкивания ионов описывается уравнением Борна :
Е(отт.) = В / rn,
где В - некоторая константа , n может принимать значения от 5 до 12 (зависит от размера ионов ). Общая энергия определяется суммой энергий притяжения и отталкивания :
Е = Е(прит.) + Е(отт.)
Её значение проходит через минимум . Координаты точки минимума отвечают равновесному расстоянию r 0 и равновесной энергии взаимодействия между ионами E 0 :
E0 = q+ q− (1 - 1 / n) / (4π r0 ε)
В кристаллической решетке всегда имеет место большее число взаимодействий , чем между парой ионов . Это число определяется в первую очередь типом кристаллической решетки . Для учета всех взаимодействий (ослабевающих с увеличением расстояния) в выражение для энергии ионной кристаллической решетки вводят так называемую константу Маделунга А :
E(прит.) = A q+ q− / (4π r ε)
Значение константы Маделунга определяется только геометрией решетки и не зависит от радиуса и заряда ионов . Например, для хлорида натрия она равна 1,74756 .
5 поляризация ионов
Помимо величины заряда и радиуса важной характеристикой иона являются его поляризационные свойства . Рассмотрим этот вопрос несколько подробнее. У неполярных частиц (атомов, ионов, молекул) центры тяжести положительных и отрицательных зарядов совпадают . В электрическом поле происходит смещение электронных оболочек в направлении положительно заряженной пластины , а ядер - в направлении отрицательно заряженной пластины . Вследствие деформации частицы в ней возникает диполь , она становится полярной .
Источником электрического поля в соединениях с ионным типом связи являются сами ионы . Поэтому, говоря о поляризационных свойствах иона , необходимо различать поляризующее действие данного иона и способность его самого поляризоваться в электрическом поле .
Поляризующее действие иона будет тем большим , чем больше его силовое поле , т. е. чем больше заряд и меньше радиус иона . Поэтому в пределах подгрупп в Периодической системе элементов поляризующее действие ионов понижается сверху вниз , так как в подгруппах при постоянной величине заряда иона сверху вниз увеличивается его радиус .
Поэтому поляризующее действие ионов щелочных металлов например растет от цезия к литию , а в ряду галогенид-ионов - от I к F . В периодах поляризующее действие ионов растет слева направо вместе с увеличением заряда иона и уменьшением его радиуса .
Поляризуемость иона , способность его к деформации растут с уменьшением силового поля , т. е. с уменьшением величины заряда и увеличением радиуса . Поляризуемость анионов обычно выше , чем катионов и в ряду галогенидов растет от F к I .
На поляризационные свойства катионов оказывает влияние характер их внешней электронной оболочки . Поляризационные свойства катионов как в активном , так и в пассивном смысле при одинаковом заряде и близком радиусе растут при переходе от катионов с заполненной оболочкой к катионам с незаконченной внешней оболочкой и далее к катионам с 18-электронной оболочкой .
Например, в ряду катионов Mg 2+ , Ni 2+ , Zn 2+ поляризационные свойства усиливаются . Эта закономерность согласуется с изменением в приведенном в ряду радиуса иона и строения его электронной оболочки:
Для анионов поляризационные свойства ухудшаются в такой последовательности:
I - , Br - , Cl - , CN - , OH - , NO 3 - , F - , ClO 4 - .
Результатом поляризационного взаимодействия ионов является деформация их электронных оболочек и, как следствие этого, сокращение межионных расстояний и неполное разделение отрицательного и положительного зарядов между ионами.
Например, в кристалле хлорида натрия величина заряда на ионе натрия составляет +0,9 , а на ионе хлора - 0,9 вместо ожидаемой единицы . В молекуле KCl , находящейся в парообразном состоянии , величина зарядов на ионах калия и хлора составляет 0,83 единицы заряда , а в молекуле хлороводорода - лишь 0,17 единицы заряда.
Поляризация ионов оказывает заметное влияние на свойства соединений с ионной связью , понижая их температуры плавления и кипения , уменьшая электролитическую диссоциацию в растворах и расплавах и др .
Ионные соединения образуются при взаимодействии элементов , значительно различающихся по химическим свойствам . Чем больше удалены друг от друга элементы в периодической системе , тем в большей степени проявляется в их соединениях ионная связь . Напротив , в молекулах, образованных одинаковыми атомами или атомами элементов, близких по химическим свойствам , возникают другие типы связи . Поэтому теория ионной связи имеет ограниченное применение .
6 Влияние поляризации ионов на свойства веществ и свойства Ионной связи и ионных соединений
Представления о поляризации ионов помогают объяснить различия в свойствах многих однотипных веществ . Например, сравнение хлоридов натрия и калия с хлоридом серебра показывает, что при близких ионных радиусах
поляризуемость катиона Ag+ , имеющего 18-электронную внешнюю оболочку , выше , что приводит к увеличению прочности связи металл-хлор и меньшей растворимости хлорида серебра в воде .
Взаимная поляризация ионов облегчает разрушение кристаллов , что приводит к понижению температур плавления веществ . По этой причине температура плавления TlF (327 oС) существенно ниже , чем RbF (798 oC). Температура разложения веществ также понижатся с усилением взаимной поляризации ионов . Поэтому иодиды обычно разлагаются при более низких температурах , чем остальные галогениды , а соединения лития - термически менее устойчивы , чем соединения других щелочных элементов .
Деформируемость электронных оболочек сказывается и на оптических свойствах веществ . Чем более поляризована частица , тем ниже энергия электронных переходов . Если поляризация мала , возбуждение электронов требует более высокой энергии , что отвечает ультрафиолетовой части спектра . Такие вещества обычно бесцветны . В случае сильной поляризации ионов возбуждение электронов происходит при поглощении электромагнитного излучения видимой области спектра . Поэтому некоторые вещества , образованные бесцветными ионами, окрашены .
Характеристикой ионных соединений служит хорошая растворимость в полярных растворителях (вода, кислоты и т. д.) . Это происходит из-за заряженности частей молекулы . При этом диполи растворителя притягиваются к заряженным концам молекулы , и, в результате Броуновского движения , «растаскивают » молекулу вещества на части и окружают их , не давая соединиться вновь . В итоге получаются ионы окружённые диполями растворителя .
При растворении подобных соединений, как правило, выделяется энергия , так как суммарная энергия образованных связей растворитель-ион больше энергии связи анион-катион . Исключения составляют многие соли азотной кислоты (нитраты) , которые при растворении поглощают тепло (растворы охлаждаются ). Последний факт объясняется на основе законов, которые рассматриваются в физической химии .
7 Кристаллическая решётка
Ионные соединения (например, хлорид натрия NaCl) - твердые и тугоплавкие от того, что между зарядами их ионов ("+" и "–") существуют мощные силы электростатического притяжения .
Отрицательно заряженный ион хлора притягивает не только "свой " ион Na+ , но и другие ионы натрия вокруг себя . Это приводит к тому , что около любого из ионов находится не один ион с противоположным знаком , а несколько (рис. 1).

Рис. 1. Строение кристалла поваренной соли NaCl .
Фактически, около каждого иона хлора располагается 6 ионов натрия , а около каждого иона натрия - 6 ионов хлора .
Такая упорядоченная упаковка ионов называется ионным кристаллом . Если в кристалле выделить отдельный атом хлора , то среди окружающих его атомов натрия уже невозможно найти тот , с которым хлор вступал в реакцию . Притянутые друг к другу электростатическими силами , ионы крайне неохотно меняют свое местоположение под влиянием внешнего усилия или повышения температуры . Но если температура очень велика (примерно 1500°C ), то NaCl испаряется , образуя двухатомные молекулы . Это говорит о том, что силы ковалентного связывания никогда не выключаются полностью .
Ионные кристаллы отличаются высокими темпертурами плавления , обычно значительной шириной запрещенной зоны , обладают ионной проводимостью при высоких температурах и рядом специфических оптических свойств (например, прозрачностью в ближней области ИК спектра ). Они могут быть построены как из одноатомных , так и из многоатомных ионов . Пример ионных кристаллов первого типа - кристаллы галогенидов щелочных и щелочно-земельных металлов ; анионы располагаются по закону плотнейшей шаровой упаковки или плотной шаровой кладки , катионы занимают соответствующие пустоты . Наиболее характерные структуры такого типа - NaCl, CsCl, CaF2. Ионные кристаллы второго типа построены из одноатомных катионов тех же металлов и конечных или бесконечных анионных фрагментов . Конечные анионы (кислотные остатки) - NO3-, SO42-, СО32- и др . Кислотные остатки могут соединяться в бесконечные цепи , слои или образовывать трехмерный каркас , в полостях которого располагаются катионы , как, например, в кристаллических структурах силикатов . Для ионных кристаллов можно рассчитать энергию кристаллической структуры U (см. табл.), приближенно равную энтальпии сублимации ; результаты хорошо согласуются с экспериментальными данными . Согласно уравнению Борна-Майера , для кристалла , состоящего из формально однозарядных ионов :
U = -A/R + Ве-R/r - C/R6 - D/R8 + E0
(R - кратчайшее межионное расстояние , А - константа Маделунга , зависящая от геометрии структуры , В и r - параметры , описывающие отталкивание между частицами , C/R6 и D/R8 характеризуют соответствующие диполь-дипольное и диполь-квадрупольное взаимодействие ионов , E 0 - энергия нулевых колебаний , е - заряд электрона ). С укрупнением катиона возрастает вклад диполь-дипольных взаимодействий .
7.1. Что такое химические связи
В предыдущих главах вы познакомились с составом и строением изолированных атомов различных элементов, изучили их энергетические характеристики. Но в окружающей нас природе изолированные атомы встречаются крайне редко. Атомы почти всех элементов " стремятся" соединиться, образуя молекулы или другие более сложные химические частицы. Принято говорить, что при этом между атомами возникают химические связи.
В образовании химических связей участвуют электроны. Каким образом это происходит, вы узнаете, изучив эту главу. Но прежде нам надо ответить на вопрос, почему атомы образуют химические связи. На этот вопрос мы можем ответить, даже не зная ничего о природе этих связей: " Потому что это энергетически выгодно!" А вот, отвечая на вопрос, откуда при образовании связей возникает выигрыш в энергии, мы постараемся понять, как и почему химические связи образуются.
Как и электронное строение атомов, подробно и строго научно химические связи изучает квантовая химия, а мы с вами можем только воспользоваться некоторыми важнейшими выводами, сделанными учеными. При этом для описания химических связей мы будем пользоваться одной из простейших моделей, предусматривающей существование трех типов химической связи (ионной, ковалентной и металлической).
Вспомните – грамотно пользоваться любой моделью можно, только зная границы применимости этой модели. Модель, которой мы будем пользоваться, тоже имеет свои границы применимости. Например, в рамках этой модели нельзя описать химические связи в молекулах кислорода, большинства бороводородов и некоторых других веществ. Для описания химических связей в этих веществах используют более сложные модели.
1. Если связываемые атомы сильно отличаются по размерам, то маленькие атомы (склонные принимать электроны) отнимут электроны у больших атомов (склонных отдавать электроны), и образуется ионная связь. Энергия ионного кристалла меньше, чем энергия изолированных атомов, поэтому ионная связь возникает даже тогда, когда атому не удается, отдавая электроны, полностью завершить свою электронную оболочку (незавершенным может остаться d - или f -подуровень). Рассмотрим примеры.
2. Если связываемые атомы маленькие(r
o
<1),
то все они склонны принимать электроны, а
отдавать их не склонны; поэтому отобрать друг у
друга электроны такие атомы не могут. В этом
случае связь между ними возникает за счет
попарного обобществления неспаренных валентных
электронов: один электрон одного атома и один
электрон другого атома с разными спинами
образуют пару электронов, принадлежащую обоим
атомам и связывающую их. Так образуется ковалентная
связь
.
Образование ковалентной связи в пространстве
можно представить себе как перекрывание
электронных облаков неспаренных валентных
электронов разных атомов. При этом пара
электронов образует общее электронное облако,
связывающее атомы. Чем больше электронная
плотность в области перекрывания, тем больше
выделяется энергии при образовании такой связи.
Прежде чем рассмотреть простейшие примеры
образования ковалентной связи, договоримся
валентные электроны атома обозначать точками
вокруг символа этого атома, причем парой точек –
неподеленные электронные пары и пары электронов
ковалентной связи, а отдельными точками –
неспаренные электроны. При таком обозначении
валентная электронная конфигурация атома,
например, фтора будет изображаться символом , а атома кислорода – . Построенные из таких
символов формулы называются электронными
формулами
или формулами Льюиса (американский
химик Гилберт Ньютон Льюис предложил их в 1916
году). По объему передаваемой информации
электронные формулы относятся к группе
структурных формул. Примеры образования атомами
ковалентных связей:


3. Если связываемые атомы большие (r o > 1А), то все они более или менее склонны отдавать свои электроны, а склонность принимать чужие электроны у них незначительна. Поэтому образовать между собой ионную связь эти большие атомы тоже не могут. Ковалентная связь между ними также оказывается невыгодной, так как электронная плотность в больших по размеру внешних электронных облаках незначительна. В этом случае при образовании из таких атомов химического вещества происходит обобществление валентных электронов всех связываемых атомов (валентные электроны становятся общими для всех атомов), и образуется металлический кристалл (или жидкость), в котором атомы связаны металлической связью.
Как определить, связи какого типа образуют
атомы элементов в определенном веществе?
По положению элементов в естественной системе
химических элементов, например:
1. Хлорид цезия CsCl. Атом цезия (IА группа) большой,
легко отдает электрон, а атом хлора (VIIА группа)
маленький и легко его принимает, следовательно,
связь в хлориде цезия ионная.
2. Диоксид углерода CO 2 . Атомы углерода (IVА
группа) и кислорода (VIА группа) не сильно
отличаются по размерам – оба маленькие. По
склонности принимать электроны они отличаются
незначительно, следовательно связь в молекуле CO 2
ковалентная.
3. Азот N 2 . Простое вещество. Связываемые
атомы одинаковые и при этом маленькие,
следовательно, связь в молекуле азота
ковалентная.
4. Кальций Са. Простое вещество. Связываемые атомы
одинаковые и довольно большие, следовательно
связь в кристалле кальция металлическая.
5. Барий-тетраалюминий BaAl 4 . Атомы обоих
элементов достаточно велики, особенно атомы
бария, поэтому оба элемента склонны только
отдавать электроны, следовательно, связь в этом
соединении металлическая.
ИОННАЯ
СВЯЗЬ, КОВАЛЕНТНАЯ СВЯЗЬ, МЕТАЛЛИЧЕСКАЯ СВЯЗЬ,
УСЛОВИЯ ИХ ОБРАЗОВАНИЯ.
1.Что является
причиной соединения атомов и образования между
ними химических связей?
2.Почему благородные газы состоят не из молекул, а
из атомов?
3.Определите тип химической связи в бинарных
соединениях: а) KF, K 2 S, SF 4 ; б) MgO, Mg 2 Ba,
OF 2 ; в) Cu 2 O, CaSe, SeO 2 . 4.Определите
тип химической связи в простых веществах: а) Na, P,
Fe; б) S 8 , F 2 , P 4 ; в) Mg, Pb, Ar.
7.З. Ионы. Ионная связь
В предыдущем параграфе вы познакомились с
ионами, которые образуются, когда отдельные
атомы принимают или отдают электроны. В этом
случае число протонов в атомном ядре перестает
быть равным числу электронов в электронной
оболочке, и химическая частица приобретает
электрический заряд.
Но в состав иона может входить и не одно ядро, как
в молекуле. Такой ион представляет собой единую
систему, состоящую из нескольких атомных ядер и
электронной оболочки. В отличие от молекулы
общее число протонов в ядрах не равно общему
числу электронов в электронной оболочке, отсюда
– электрический заряд иона.
Какие бывают ионы? То есть, чем они могут
различаться?
По числу атомных ядер ионы делятся на простые
(или
одноатомные
), то есть содержащие одно ядро
(например: K,
O 2 ), и сложные
(или многоатомные
), то есть содержащие
несколько ядер (например: CO 3 2 , 3 ). Простые ионы
– заряженные аналоги атомов, а сложные –
заряженные аналоги молекул.
По знаку заряда ионы делятся на катионы
и анионы
.
Примеры катионов: K (ион калия), Fe 2 (ион железа), NH 4 (ион аммония), 2 (ион тетраамминмеди). Примеры анионов: Cl (хлорид-ион), N 3 (нитрид-ион), PO 4 3 (фосфат-ион), 4 (гексацианоферрат-ион).
По значению заряда ионы делятся на однозарядные (K , Cl , NH 4 , NO 3 и т. п.), двухзарядные (Са 2 , O 2 , SО 4 2 и т. д.) трехзарядные (Аl 3 , РО 4 3 и т. п.) и так далее.
Итак, ион РО 4 3 мы назовем трехзарядным сложным анионом, а ион Са 2 – двухзарядным простым катионом.
Кроме этого, ионы различаются еще и своими размерами. Размер простого иона определяется радиусом этого иона или ионным радиусом . Размер сложных ионов охарактеризовать труднее. Радиус иона, как и радиус атома, непосредственно измерить невозможно (как вы понимаете, четких границ у иона нет). Поэтому для характеристики изолированных ионов используют орбитальные ионные радиусы (примеры – в таблице 17).
Таблица 17.Орбитальные радиусы некоторых простых ионов
Орбитальный радиус, А |
Орбитальный радиус, А |
||||
| Li | F | 0,400 | |||
| Na | Cl | 0,742 | |||
| K | Br | 0,869 | |||
| Rb | I | 1,065 | |||
| Cs | O 2 | 0,46 | |||
| Be 2 | S 2 | 0,83 | |||
| Mg 2 |
Ионная связь − химическая связь, образованная в результате взаимного электростатического притяжения противоположно заряженных ионов, при котором устойчивое состояние достигается путем полного перехода общей электронной плотности к атому более электроотрицательного элемента.
Чисто ионная связь есть предельный случай ковалентной связи.
На практике полный переход электронов от одного атома к другому атому по связи не реализуется, поскольку каждый элемент имеет большую или меньшую (но не нулевую) ЭО, и любая химическая связь будет в некоторой степени ковалентной.
Такая связь возникает в случае большой разности ЭО атомов, например, между катионами s -металлов первой и второй групп периодической системы и анионами неметаллов VIА и VIIА групп (LiF, NaCl, CsF и др.).
В отличие от ковалентной связи, ионная связь не обладает направленностью . Это объясняется тем, что электрическое поле иона обладает сферической симметрией, т.е. убывает с расстоянием по одному и тому же закону в любом направлении. Поэтому взаимодействие между ионами независимо от направления.
Взаимодействие двух ионов противоположного знака не может привести к полной взаимной компенсации их силовых полей. В силу этого у них сохраняется способность притягивать ионы противоположного знака и по другим направлениям. Следовательно, в отличие от ковалентной связи, ионная связь характеризуется также ненасыщаемостью .
Отсутствие у ионной связи направленности и насыщаемости обуславливает склонность ионных молекул к ассоциации. Все ионные соединения в твердом состоянии имеют ионную кристаллическую решетку, в которой каждый ион окружен несколькими ионами противоположного знака. При этом все связи данного иона с соседними ионами равноценны.
Металлическая связь
Металлы характеризуются рядом особых свойств: электро- и теплопроводностью, характерным металлическим блеском, ковкостью, высокой пластичностью, большой прочностью. Эти специфические свойства металлов можно объяснить особым типом химической связи, получившей название металлической .
Металлическая связь – результат перекрывания делокализованных орбиталей атомов, сближающихся между собой в кристаллической решетке металла.
У большинства металлов на внешнем электронном уровне имеется значительное число вакантных орбиталей и малое число электронов.
Поэтому энергетически более выгодно, чтобы электроны не были локализованы, а принадлежали всему атому металла. В узлах решетки металла находятся положительно заряженные ионы, которые погружены в электронный «газ», распределенный по всему металлу:
Me ↔ Me n + + n .
Между положительно заряженными ионами металла (Me n +) и нелокализованными электронами (n ) существует электростатическое взаимодействие, обеспечивающее устойчивость вещества. Энергия этого взаимодействия является промежуточной между энергиями ковалентных и молекулярных кристаллов. Поэтому элементы с чисто металлической связью (s -, и p -элементы) характеризуются относительно высокими температурами плавления и твердостью.
Наличие электронов, которые свободно могут перемещаться по объему кристалла, и обеспечивают специфические свойства ме-
Водородная связь
Водородная связь – особый тип межмолекулярного взаимодействия. Атомы водорода, которые ковалентно связаны с атомом элемента, имеющего высокое значение электроотрицательности (чаще всего F, O, N, а также Cl, S и C), несут на себе относительно высокий эффективный заряд. Вследствие этого такие атомы водорода могут электростатически взаимодействовать с атомами указанных элементов.
Так, атом Н d + одной молекулы воды ориентируется и соответственно взаимодействует (что показано тремя точками) с атомом О d - другой молекулы воды:

Связи, образуемые атомом Н, находящимся между двумя атомами электроотрицательных элементов, называются водородными:
d- d+ d-
А − Н ××× В
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (150–400 кДж/моль), однако этой энергии достаточно, чтобы вызвать агрегацию молекул соответствующих соединений в жидком состоянии, например, в жидком фтороводороде НF (рис. 2.14). Для соединений фтора она достигает порядка 40 кДж/моль.

Рис. 2.14. Агрегация молекул НF за счет водородных связей
Длина водородной связи также меньше длины ковалентной связи. Так, в полимере (HF) n длина связи F−H=0,092 нм, а связи F∙∙∙H= 0,14 нм. У воды длина связи O−H=0,096 нм, а связи O∙∙∙H=0,177нм.
Образование межмолекулярных водородных связей приводит к существенному изменению свойств веществ: повышению вязкости, диэлектрической постоянной, температур кипения и плавления.
Назад
Вперёд
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Цели урока :
- Сформировать понятие об химических связях на примере ионной связи. Добиться понимания образования ионной связи как крайнего случая полярной.
- Обеспечить в ходе урока усвоение следующих основных понятий: ионы (катион, анион), ионная связь.
- Развивать умственную деятельность учащихся через создание проблемной ситуации при изучении нового материала.
Задачи:
- научить распознавать виды химической связи;
- повторить строение атома;
- исследовать механизм образования ионной химической связи;
- научить составлять схемы образования и электронные формулы ионных соединений, уравнения реакций с обозначением перехода электронов.
Оборудование : компьютер, проектор, мультимедийный ресурс, периодическая система химических элементов Д.И. Менделеева, таблица «Ионная связь».
Тип урока: Формирование новых знаний.
Вид урока: Мультимедиа урок.
Х од урока
I. Организационный момент .
II. Проверка домашнего задания .
Учитель: Как атомы могут принимать устойчивые электронные конфигурации? Каковы cпособы образования ковалентной связи?
Ученик: Полярная и неполярная ковалентные связи образованы по обменному механизму. К обменному механизму относят случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону. Например, водород: (слайд 2)

Связь возникает благодаря образованию общей электронной пары за счет объединения неспаренных электронов. У каждого атома есть по одному s-электрону. Атомы Н равноценны и пары одинаково принадлежат обоим атомам. Поэтому же принципу происходит образование общих электронных пар (перекрывание р-электронных облаков) при образовании молекулы F 2 . (слайд 3)

Запись H· означает, что у атома водорода на внешнем электронном слое находится 1 электрон. Запись показывает, что на внешнем электронном слое атома фтора находится 7 электронов.
При образовании молекулы N 2 . Образуются 3 общие электронные пары. Перекрываются р-орбитали. (слайд 4)

Связь называется неполярная.
Учитель: Мы сейчас рассмотрели случаи, когда образуются молекулы простого вещества. Но вокруг нас множество веществ, сложного строения. Возьмем молекулу фтороводорода. Как в этом случае происходит образование связи?
Ученик: При образовании молекулы фтороводорода перекрывается орбиталь s-электрона водорода и орбиталь р-электрона фтора Н-F. (слайд 5)

Связывающая электронная пара смещена к атому фтора, в результате чего образуется диполь . Связь называется полярная .
III. Актуализация знаний .
Учитель: Химическая связь возникает вследствие изменений, которые происходят с наружными электронными оболочками соединяющихся атомов. Это возможно потому, что наружные электронные слои не завершены у элементов, кроме инертных газов. Химическая связь объясняется стремлением атомов приобрести устойчивую электронную конфигурацию, подобную конфигурации «ближайшего» к ним инертного газа.

Учитель: Записать схему электронного строения атома натрия (у доски). (слайд 6)

Ученик: Атому натрия для достижения устойчивости электронной оболочки необходимо либо отдать один электрон, либо принять семь. Натрий легко отдаст свой далекий от ядра и слабо связанный с ним электрон.
Учитель: Составить схему отдачи электрона.

Nа° - 1ē → Nа+ = Ne
Учитель: Записать схему электронного строения атома фтора (у доски).
Учитель: Как добиться завершения заполнения электронного слоя?
Ученик: Атому фтора для достижения устойчивости электронной оболочки необходимо либо отдать семь электронов, либо принять один. Энергетически выгоднее фтору принять электрон.
Учитель: Составить схему приема электрона.
F° + 1ē → F- = Ne
IV. Изучение нового материал.
Учитель обращается с вопросом к классу, в котором ставится задача урока:
Возможны ли другие варианты, при которых атомы могут принимать устойчивые электронные конфигурации? Каковы пути образования таких связей?
Сегодня мы рассмотрим один из видов связей – ионную связь. Сопоставим строение электронных оболочек уже названных атомов и инертных газов.
Беседа с классом.
Учитель: Какой заряд имели атомы натрия и фтора до реакции?
Ученик: Атомы натрия и фтора электронейтральны, т.к. заряды их ядер уравновешиваются электронами, вращающимися вокруг ядра.
Учитель: Что происходит между атомами при отдаче и принятии электронов?
Ученик: Атомы приобретают заряды.
Учитель дает пояснения: В формуле иона дополнительно записывают его заряд. Для этого используют верхний индекс. В нем цифрой указывают величину заряда (единицу не пишут), а потом – знак (плюс или минус). Например, ион Натрия с зарядом +1 имеет формулу Na + (читается «натрий-плюс»), ион Фтора с зарядом -1 – F - («фтор-минус»), гидроксид-ион с зарядом -1 – ОН - («о-аш-минус»), карбонат-ион с зарядом -2 – CO 3 2- («цэ-о-три-два-минус»).
В формулах ионных соединений сначала записывают, не указывая зарядов, положительно заряженные ионы, а потом - отрицательно заряженные. Если формула правильная, то сумма зарядов всех ионов в ней равна нулю.
Положительно заряженный ионназывается катионом ,аотрицательно заряженный ион- анионом.
Учитель: Записываем определение в рабочие тетради:
Ион - это заряженная частица, в которую превращается атом в результате принятия или отдачи электронов.
Учитель: Как определить величину заряда иона кальция Ca 2+ ?
Ученик: Ио́н - электрически заряженная частица, образующаяся в результате потери или присоединения одного или нескольких электронов атомом. У кальция на последнем электронном уровне находятся два электрона, ионизация атома кальция происходит при отдаче двух электронов. Ca 2+ - двухзарядный катион.
Учитель: Что происходит с радиусами этих ионов?
При переходе электронейтрального атома в ионное состояние размер частицы сильно изменяется. Атом, отдавая свои валентные электроны, превращается при этом в более компактную частицу - катион. Например, при переходе атома натрия в катион Na+, имеющий, как указано выше, структуру неона, радиус частицы сильно уменьшается. Радиус аниона всегда больше радиуса соответствующего электронейтрального атома.
Учитель: Что происходит с разноименно заряженными частицами?
Ученик: Разноименно заряженные ионы натрия и фтора, возникающие в результате перехода электрона от атома натрия к атому фтора, взаимно притягиваются и образуют фторид натрия. (слайд 7)
Nа + + F - = NаF
Рассмотренная нами схема образования ионов показывает, как между атомом натрия и атомом фтора образуется химическая связь, которую называют ионной.
Ионная связь – химическая связь, образованная электростатическим притяжением друг к другу разноименно заряженных ионов.
Соединения, которые при этом образуются, называют ионными соединениями.
V. Закрепление нового материала .
Задания для закрепления знаний и умений
1. Сравните строение электронных оболочек атома кальция и катиона кальция, атома хлора и хлорид - аниона:






Прокомментируйте схему образования ионной связи в хлориде кальция:
2. Для выполнения данного задания необходимо разделиться на группы по 3–4 человека. Каждый участник группы рассматривает один пример и результаты представляет всей группе.
Ответ учащихся:
1. Кальций – это элемент главной подгруппы II группы, металл. Его атому легче отдать два внешних электрона, чем принять недостающие шесть:
![]()
2. Хлор – это элемент главной подгруппы VII группы, неметалл. Его атому легче принять один электрон, которого ему не хватает до завершения внешнего уровня, чем отдать семь электронов с внешнего уровня:
3. Сначала найдем наименьшее общее кратное между зарядами образовавшихся ионов, оно равно 2 (2x1). Затем определим, сколько атомов кальция нужно взять, чтобы они отдали два электрона, то есть надо взять один атом Са и два атома CI.
4. Схематично образование ионной связи между атомами кальция и хлора можно записать: (слайд 8)
Са 2+ + 2СI - → СаСI 2

Задания для самоконтроля
1. На основе схемы образования химического соединения составьте уравнение химической реакции: (слайд 9)

2. На основе схемы образования химического соединения составьте уравнение химической реакции: (слайд 10)

3. Дана схема образования химического соединения: (слайд 11)

Выберите пару химических элементов, атомы которых могут взаимодействовать в соответствии с этой схемой:
а) Na и O ;
б) Li и F ;
в) K и O ;
г) Na и F