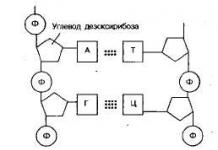
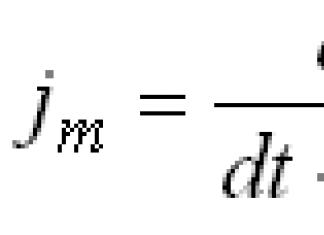Les unités de mesure des quantités sont normalisées dans le Système international d'unités de mesure (SI). Les normes SI sont reconnues communauté internationale (Organisation internationale normalisation - ISO). La Russie est membre de l'ISO et la Russie est l'un des trois langues officielles de cette association (également en anglais et en français).
Le SI peut également être appelé système MKSA (mètre, kilogramme, seconde, ampère).
La littérature et la documentation technique et commerciale russes et étrangères (en particulier l'anglais) continuent d'utiliser des unités de mesure obsolètes et non systémiques. Ceux d'entre eux qui sont au moins légèrement liés au traitement de l'eau sont indiqués ci-dessous avec conversion en unités SI.
Dans les cas de purification et de traitement de l'eau, des unités de mesure standardisées sont également utilisées, qui permettent, sur la base des résultats, de tirer des conclusions compréhensibles et de haute qualité, d'évaluer son niveau et d'autres indicateurs de la qualité de l'eau, ainsi que de sélectionner pour sa purification.
P.1.1. Température
La méthode de réglage des valeurs de température est l'échelle de température. Plusieurs échelles de température sont connues.
Échelle Kelvin (du nom du physicien anglais W. Thomson, Lord Kelvin).
Symbole de l'unité : K (et non « degré Kelvin » et non °K).
1 K = 1/273,16 – partie de la température thermodynamique du point triple de l'eau, correspondant à l'équilibre thermodynamique d'un système constitué de glace, d'eau et de vapeur.
Échelle Celsius (du nom de l'astronome et physicien suédois A. Celsius).
Dans cette échelle, la température de fusion de la glace à pression normale est de 0°C et le point d’ébullition de l’eau est de 100°C.
Les échelles Kelvin et Celsius sont liées par l'équation :
t (°C) = T (K) – 273,15.
Échelle Fahrenheit (D. G. Fahrenheit - physicien allemand).
Symbole de l'unité : °F. Largement utilisé, notamment aux USA.
L'échelle Fahrenheit et l'échelle Celsius sont liées : t (°F) = 1,8 · t (°C) + 32°C.
En valeur absolue, 1 (°F) = 1 (°C). Échelle de Réaumur (du nom du physicien français R.A. Réaumur).
Désignation : °R et °r. Cette balance est quasiment hors d'usage.
Rapport aux degrés Celsius :
t (°R) = 0,8 t (°C).
L'échelle Rankine (Rankine) doit son nom à l'ingénieur et physicien écossais W. J. Rankin.
La désignation est la même que pour le diplôme Réau-mur : °R (parfois : °Rank).
Cette échelle est également utilisée aux États-Unis. La température sur l'échelle de Rankine est liée à la température sur l'échelle Kelvin :
t (°R) = 9/5 T (K).
La relation entre les valeurs des indicateurs de température à différentes échelles est présentée dans le tableau. P.1.1
P.1.2. Longueur
L'unité de mesure SI est le mètre (m).
Unité non systémique: Angström (Å). 1Å = 1·10-10 m.
Pouce (du néerlandais duim - pouce) ; pouce; dans; ́ ́; 1 = 25,4 mm.
Main (main anglaise – main) ; 1 aiguille = 101,6 mm. Lien (lien anglais – lien) ; 1 li = 201,168 mm.
Span (span anglais – span, span) ; 1 travée = 228,6 mm.
Pied (pied anglais – jambe, pieds – pieds) ; 1 pied = 304,8 mm. Cour (cour anglaise - cour, corral) ; 1 mètre = 914,4 mm. Fathom, fesom (anglais fathom - une mesure de longueur (= 6 pi), ou une mesure du volume de bois (= 216 pi3), ou une mesure de superficie de montagne (= 36 pi2), ou une brasse (Ft)) ; fath ou fth ou Ft ou ƒfm; 1 pied = 1,8288 m.
Chaîne (eng. chaîne - chaîne); 1 ch = 66 pi = 22 yd = = 20,117 m.
Furlong (eng. furlong) – 1 fourrure = 220 yd = 1/8 mile. Mile (mile anglais ; international).
1 ml (mi, MI) = 5 280 pieds = 1 760 yd = 1 609,344 m.
P.1.3. Carré
L'unité de mesure SI est le m2.
Pied carré; 1 pi2 (également pied carré) = 929,03 cm2. Pouce carré ; 1 po2 (pouces carrés) = 645,16 mm2. Brasse carrée (fesom); 1 fath2 (ft2; Ft2; sq Ft) = 3,34451 m2.
Yard carré; 1 yd2 (yd carré) = 0,836127 m2. Sq (carré) – carré.
P.1.4. Volume, capacité
L'unité de mesure SI est le m3.
Pied carré; 1 pi3 (également pi3) = 28,3169 dm3.
Brasse cubique ; 1 fath3 (fth3; Ft3; cu Ft) = = 6,11644 m3.
Verge cube ; 1 yd3 (yd cube) = 0,764555 m3. Pouce cube ; 1 po3 (po cu) = 16,3871 cm3. Boisseau (Royaume-Uni); 1 bu (Royaume-Uni, également Royaume-Uni) = 36,3687 dm3.
Boisseau (États-Unis) ; 1 bu (nous, également US) = 35,2391 dm3. Gallon (Royaume-Uni); 1 gal (Royaume-Uni, également Royaume-Uni) = 4,54609 dm3.
Gallon de liquide (États-Unis); 1 gal (nous, également US) = 3,78541dm3.
Gallon sec (États-Unis); 1 gal sec (nous, également US) = 4,40488 dm3.
Jill (branchie); 1 gi = 0,12 l (États-Unis), 0,14 l (Royaume-Uni).
Baril (États-Unis); 1 baril = 0,16 m3.
ROYAUME-UNI - Royaume-Uni– Royaume-Uni (Royaume-Uni) ;
États-Unis – États-Unis (USA).
P.1.5. Poids
L'unité de mesure SI est le kg.
Livre (commerce) (eng. balance, livre - pesée, livre); 1 livre = 453,592 g ; livres – livres. Dans le système des anciennes mesures russes, 1 livre = 409,512 g.
Gran (grain anglais – grain, grain, grain) ; 1 gr = 64,799 mg.
Pierre (eng. pierre - pierre); 1 maille = 14 lb = 6,350 kg.
P.1.6. Densité (y compris volume)
L'unité de mesure SI est le kg/m3.
1 t/m3= 1000 kg/m3 ; 1 kg/dm3= 10-3 kg/m3. lb/pi3 ; 1 lb/pi3 = 16,0185 kg/m3.
P.1.7. Densité linéaire
L'unité de mesure SI est le kg/m.
lb/pi ; 1 lb/pied = 1,48816 kg/m.
Livre/Yard ; 1 lb / yd = 0,496055 kg/m.
P.1.8. Densité surfacique
L'unité de mesure SI est le kg/m2.
lb/pi2 ; 1 lb/pi2 (également lb/pied carré – livre par pied carré) = 4,88249 kg/m2.
lb/yd2 ; 1 lb / yd2 (également lb / sq in – livre par pouce carré) = 0,542492 kg/m2.
P.1.9. Volume spécifique
L'unité SI est m3/kg. pi3/lb ; 1 pi3 / lb = 62,428 dm3/kg.
P.1.10. Vitesse (linéaire)
L'unité SI est m/s. pieds/h ; 1 pied/h = 0,3048 m/h. pieds/s ; 1 pied/s = 0,3048 m/s.
P.1.11. Accélération
L'unité SI est m/s2. pi/s2 ; 1 pi/s2 = 0,3048 m/s2.
P.1.12. Débit massique
L'unité SI est kg/s. lb/h ; 1 lb/h = 0,453592 kg/h. Kg; 1 lb/s = 0,453592 kg/s.
P.1.13. Débit volumique
L'unité SI est m3/s.
pi3/min ; 1 pi3/min = 28,3168 dm3/min.
Cour3/min ; 1 yd3/min = 0,764555 dm3/min.
Gpm ; 1 gal/min (également GPM – gallon par min) = 3,78541 dm3/min.
P.1.14. Force, poids
L'unité de mesure SI est N.
Livre-force ; 1 lbf – 4,44822 N. (Un analogue du nom de l'unité de mesure : kilogramme-force, kgf. 1 kgf = 9,80665 N (exact). 1 lbf = 0,453592 (kg) 9,80665 N = 4, 44822 N 1N=1 kgm/s2
Poundal (anglais : livre); 1 pdl = 0,138255 N.
Poundall est la force qui confère une accélération de 1 pied/s2 à une masse d'une livre, lb·pied/s2.
P.1.15. Densité spécifique
L'unité de mesure SI est N/m3.
lb/pi3 ; 1 lbf/pi3 = 157,087 N/m3.
Livre/pi3 ; 1 pdl/pi3 = 4,87985 N/m3.
P.1.16. Pression
L'unité de mesure SI est Pa, unités multiples : MPa, kPa. Dans leur travail, les spécialistes continuent d'utiliser des unités de mesure de pression obsolètes, annulées ou précédemment acceptées en option : kgf/cm2 ; bar; au m. (atmosphère physique); à (ambiance technique); à; ati; m d'eau Art.; mmHg St; torr.
Les notions suivantes sont utilisées : « pression absolue », « surpression ».
Il y a des erreurs lors de la conversion de certaines unités de pression en Pa et ses multiples. Il faut tenir compte du fait que 1 kgf/cm2 est égal à 98066,5 Pa (exactement), c'est-à-dire que pour de petites pressions (jusqu'à environ 14 kgf/cm2) avec une précision suffisante pour le travail, vous pouvez accepter :
1 Pa = 1 kg/(m·s2) = 1 N/m2.
1 kgf/cm2 ≈ 105 Pa = 0,1 MPa.
Mais déjà à moyennes et hautes pressions : 24 kgf/cm2 ≈ 23,5 · 105 Pa = 2,35 MPa ; 40 kgf/cm2 ≈ 39 · 105 Pa = 3,9 MPa ; 100 kgf/cm2 ≈ 98 105 Pa = 9,8 MPa, etc.
Rapports :
1 atm (physique) ≈ 101325 Pa ≈ 1,013 105 Pa ≈ ≈ 0,1 MPa.
1 at (technique) = 1 kgf/cm2 = 980066,5 Pa ≈ ≈ 105 Pa ≈ 0,09806 MPa ≈ 0,1 MPa.
0,1 MPa ≈ 760 mmHg. Art. ≈ 10 m d'eau. Art. ≈ 1 barre. 1 Torr (tor) = 1 mm Hg. Art.
lbf/po2 ; 1 lbf/in2 = 6,89476 kPa (voir ci-dessous : PSI).
lb/pi2 ; 1 lbf/pi2 = 47,8803 Pa. lbf/yd2 ; 1 lbf/yd2 = 5,32003 Pa.
Livre/pi2 ; 1 pdl/pi2 = 1,48816 Pa.
Colonne d'eau au pied ; 1 pied H2O = 2,98907 kPa.
Pouce de colonne d’eau ; 1 dans H2O = 249,089 Pa.
Pouce de mercure ; 1 po Hg = 3,38639 kPa.
PSI (également psi) – livres (P) par pouce carré (S)
(I) – livres par pouce carré ; 1 PSI = 1 lbƒ/po2 = = 6,89476 kPa.
Parfois, dans la littérature, vous pouvez trouver la désignation de l'unité de pression lb/in2 - cette unité ne prend pas en compte lbƒ (livre-force), mais lb (livre-masse). Donc, en termes numériques
1 lb/in2 est légèrement différent de 1 lbf/in2, car lors de la détermination de 1 lbƒ, les éléments suivants sont pris en compte : g = 9,80665 m/s2 (à la latitude de Londres).
1 lb/po2 = 0,454592 kg/(2,54 cm)2 = 0,07046 kg/cm2 = 7,046 kPa. Calcul de 1 lbƒ – voir ci-dessus.
1 lbf/in2 = 4,44822 N/(2,54 cm)2 = 4,44822 kg m/ (2,54 0,01 m)2 s2 = 6 894,754 kg/ (m s2) = 6 894,754 Pa ≈ 6,895 kPa.
Pour les calculs pratiques, nous pouvons supposer : 1 lbf/in2 ≈ 1 lb/in2 ≈ 7 kPa. Mais en fait, l’égalité est illégale, tout comme 1 lbƒ = 1 lb, 1 kgf = 1 kg.
PSIg (psig) – identique au PSI, mais indique une pression excessive ; PSIa (psia) – identique à PSI, mais met l'accent sur : la pression absolue ;
a – absolu, g – jauge (mesure, taille).
P.1.17. Pression de l'eau
L'unité de mesure SI est m.
Tête en pieds (pieds-tête) ; 1 pied de hauteur = 0,3048 m.
P.1.18. Débit volumique spécifique
GPM/(sq·ft) – gallon (G) par (P) minute (M)/(carré (sq) · pied (ft)) – gallons par minute par pied carré ; 1GPM/(pi²)=2445l/(m2·h)·1l/(m2·h)=10-3 m/h.
gpd – gallons par jour – gallons par jour (jour) ; 1 g/j = 0,1577 dm3/h.
gpm – gallons par minute – gallons par minute ; 1 gpm = 0,0026 dm3/min.
GPS – gallons par seconde – gallons par seconde ; 1 gps = 438 10-6 dm3/s.
P.1.19. Perte de pression pendant la filtration
PSI/pied – livres (P) par pouce carré (S) pouce (I)/pied (pied) – livres par pouce carré/pied ;
1 PSI/pied = 22,62 kPa pour 1 m de couche filtrante.
P.1.20. Consommation de sorbate (par exemple, Cl2) lors de la filtration à travers une couche de sorbant (par exemple, charbon actif)
Gals/pied cube (gal/pi3) – gallons/pied cube (gallons par pied cube) ;
1 Gals/cu ft = 0,13365 dm3 pour 1 dm3 de sorbant.
P.1.21. Travail, énergie, quantité de chaleur
L'unité de mesure SI est le Joule (du nom du physicien anglais J.P. Joule).
1 J – travail mécanique d'une force de 1 N lors du déplacement d'un corps sur une distance de 1 m.
Newton (N) est l'unité SI de force et de poids ; 1 N est égal à la force qui confère une accélération de 1 m2/s à un corps pesant 1 kg dans la direction de la force.
1 J = 1 N·m.
En génie thermique, ils continuent d'utiliser l'unité de mesure abolie de la quantité de chaleur - la calorie (cal).
1 J (J) = 0,23885 cal.
1 kJ = 0,2388 kcal.
1 lbf pi (lbf) = 1,35582 J.
1 pdl ft (pieds livres) = 42,1401 mJ.
1 Btu ( Unité britannique chaleur) = 1,05506 kJ (1 kJ = 0,2388 kcal).
1 Therm (grande calorie britannique) = = 1 · 10-5 Btu.
P.1.22. Puissance, flux de chaleur
L'unité de mesure SI est le Watt (W) - du nom de l'inventeur anglais J. Watt - puissance mécanique à laquelle 1 J de travail est effectué en 1 s, soit un flux thermique équivalent à 1 W de puissance mécanique.
1 W (W) = 1 J/s = 0,859985 kcal/h (kcal/h).
1 lbf pied/s (lbf pied/s) = 1,33582 W.
1 lbf pied/min (lbf pied/min) = 22,597 mW.
1 lbf pied/h (lbf pied/h) = 376,616 µW.
1 pdl pied/s (pieds livre/s) = 42,1401 mW
1 ch (puissance/s britannique) = 745,7 W. 1 Btu/s (British Heat Unit/s) = = 1055,06 W.
1 Btu/h (British Heat Unit/h) = = 0,293067 W.
P.1.23. Densité du flux thermique superficiel
L'unité SI est W/m2.
1 W/m2 (W/m2) = 0,859985 kcal/(m2 h) (kcal/(m2 h)).
1 Btu/(pi2 h) = 2,69 kcal/(m2 h) = 3,1546 kW/m2.
P.1.24. Viscosité
Viscosité dynamique (coefficient de viscosité), η.
L'unité SI est Pa·s.
1 Pa.s = 1 N.s/m2 ; unité non systémique – équilibre (P). 1 P = 1 dyne s/m2 = 0,1 Pa s.
Dyn (dyn) – (du grec dynamique – force). 1 dyne = 10-5 N = 1 g cm/s2 = 1,02 10-6 kgf.
1 lbf h/pi2 (lbf h/pi2) = 172,369 kPa·s.
1 lbf s / pi2 (lbf s/pi2) = 47,8803 Pa.s. 1 pdl s / pi2 (livre-s/pi2) = 1,48816 Pa.s. 1 limace /(pieds) = 47,8803 Pa.s. Limace
(limace) – unité technique de masse en Système anglais mesures
Viscosité cinématique, ν. SI – m2/s ;
L'unité cm2/s est appelée « Stokes » (du nom du physicien et mathématicien anglais J. G. Stokes). Les viscosités cinématique et dynamique sont liées par l'égalité :
ν = η / ρ, où ρ est la densité, g/cm3. 1 m2/s = Stokes / 104.
1 pi2 / h (pi2/h) = 25,8064 mm2/s. 1 pi2 / s (pi2/s) = 929,030 cm2/s.
L'unité SI de tension est A/m (Ampère/mètre).
Ampère (A) est le nom de famille du physicien français A.M. Ampère. Auparavant, on utilisait l'unité Oersted (E), du nom du physicien danois H.K. Oersted.
1 A/m (A/m, At/m) = 0,0125663 Oe (Oe).
P.1.26. Dureté
Résistance à l'écrasement et à l'abrasion des matériaux filtrants minéraux et, en général, de tous les minéraux et rochers déterminé indirectement à l'aide de l'échelle de Mohs (F. Mohs - minéralogiste allemand). Dans cette échelle, les nombres par ordre croissant désignent les minéraux disposés de telle manière que chacun des suivants est capable de laisser une égratignure sur le précédent. Les substances extrêmes sur l'échelle de Mohs sont le talc (unité de dureté 1, la plus douce) et le diamant (10, le plus dur).
Dureté 1–2,5 (tiré avec un ongle) : volskonkoite, vermiculite, halite, gypse, glauconite, graphite, matériaux argileux, pyrolusite, talc, etc.
Dureté > 2,5–4,5 (ne peut pas être dessinée avec un ongle, mais peut être dessinée avec du verre) : anhydrite, aragonite, barytine, glauconite, dolomite, calcite, magnésite, muscovite, sidérite, chalcopyrite, chabazite, etc.
Dureté > 4,5–5,5 (non étirée au verre, mais étirée au couteau en acier) : apatite, vernadite, néphéline, pyrolusite, chabazite, etc.
Dureté > 5,5–7,0 (non étiré au couteau en acier, mais étiré au quartz) : vernadite, grenat, ilménite, magnétite, pyrite, feldspaths, etc.
Dureté > 7,0 (non marqué au quartz) : diamant, grenats, corindon, etc.
La dureté des minéraux et des roches peut également être déterminée à l'aide de l'échelle de Knoop (A. Knoop - minéralogiste allemand). Dans cette échelle, les valeurs sont déterminées par la taille de l'empreinte laissée sur le minéral lorsqu'une pyramide de diamant est pressée dans son échantillon sous une certaine charge.
Citation à partir de : Unités de mesure et relations entre elles. De l'anglais M. : LLC « Maison d'édition AST » ; SARL « Maison d'édition Astrel », 2004. – 255 p.
P.1.27. Radioactivité des éléments
L'unité SI est Bq (Becquerel, du nom du physicien français A.A. Becquerel).
Bq (Bq) est une unité d'activité d'un nucléide dans une source radioactive (activité isotopique). 1 Bq est égal à l'activité d'un nucléide, à laquelle un événement de désintégration se produit en 1 s.
Concentration de radioactivité : Bq/m3 ou Bq/l.
L'activité est le nombre de désintégrations radioactives par unité de temps. L'activité par unité de masse est dite spécifique.
Curie (Ku, Ci, Cu) est une unité d'activité d'un nucléide dans une source radioactive (activité isotopique). 1 Ku est l'activité d'un isotope dans lequel 3,7000 · 1010 événements de désintégration se produisent en 1 s.
1 Ku = 3,7000 · 1010 Bq.
Rutherford (Rd, Rd) est une unité d'activité obsolète de nucléides (isotopes) dans sources radioactives, du nom du physicien anglais E. Rutherford. 1 Rd = 1 106 Bq = 1/37 000 Ci.
P.1.28. Dose de rayonnement
l'énergie des rayonnements ionisants absorbée par la substance irradiée et calculée par unité de sa masse (dose absorbée). La dose s'accumule au fil du temps d'exposition. Débit de dose ≡ Dose/temps.
L'unité SI de dose absorbée est Gray (Gy, Gy).
L'unité extrasystémique est Rad, correspondant à l'énergie de rayonnement de 100 erg absorbée par une substance pesant 1 g.
Erg (erg - du grec : ergon - travail) est une unité de travail et d'énergie dans le système GHS non recommandé.
1erg=10-7 J=1,02·10-8 kgf·m=2,39·10-8 cal==2,78·10-14 kWh.
1 rad = 10-2 Gy.
1 rad(rad)=100erg/g=0,01Gy=2,388·10-6cal/g== 10-2 J/kg.
Kerma (anglais abrégé : énergie cinétique libérée dans la matière) – énergie cinétique libérée dans la matière, mesurée en gris.
La dose équivalente est déterminée en comparant le rayonnement nucléide avec le rayonnement X. Le facteur de qualité du rayonnement (K) indique combien de fois le risque d'irradiation en cas d'exposition humaine chronique (à des doses relativement faibles) pour un type de rayonnement donné est plus grand que dans le cas d'un rayonnement aux rayons X à la même dose absorbée. Pour les rayons X et les rayonnements γ, K = 1. Pour tous les autres types de rayonnement, K est établi en fonction des données radiobiologiques.
Deq = Dpogl · K.
L'unité SI de dose absorbée est 1 Sv (Sievert) = 1 J/kg = 102 rem.
BER (rem, rem - jusqu'en 1963 était défini comme l'équivalent biologique d'un rayon X) - une unité de dose équivalente de rayonnement ionisant.
Rayons X (P, R) – unité de mesure, dose d'exposition aux rayons X et aux rayons γ.
1 P = 2,58 · 10-4 C/kg.
Coulomb (C) – unité SI, quantité d’électricité, charge électrique.
1 rem = 0,01 J/kg.
Débit de dose équivalent – Sv/s.
P.1.29. Perméabilité des milieux poreux (y compris les roches et les minéraux)
Darcy (D) - du nom de l'ingénieur français. A. Darcy, darsy (D) 1 D = 1,01972 µm2
1 D est la perméabilité d'un tel milieu poreux, lors de la filtration d'un échantillon d'une superficie de 1 cm2, d'une épaisseur de 1 cm et d'une chute de pression de 0,1 MPa, le débit d'un liquide d'une viscosité de 1 cP est égal à 1 cm3/s.
P.1.30. Tailles des particules, grains (granulés) des matériaux filtrants selon SI et normes d'autres pays
Aux États-Unis, au Canada, en Grande-Bretagne, au Japon, en France et en Allemagne, la granulométrie est estimée en mailles (eng. mesh - trou, cellule, réseau), c'est-à-dire par le nombre (nombre) de trous par pouce du tamis le plus fin à travers lequel ils peuvent faire passer les grains Et le diamètre effectif des grains correspond à la taille du trou en microns. DANS dernières années Les systèmes maillés américains et britanniques sont plus couramment utilisés.
P.1.31. Concentration des solutions
Fraction massique. La fraction massique indique la quantité massique d'une substance contenue dans 100 parties en masse d'une solution.
Unités de mesure : fractions d'unité ; intérêt (%); ppm (‰); parties par million (ppm).
Concentration des solutions et solubilité. La concentration d'une solution doit être distinguée de la solubilité - la concentration d'une solution saturée, qui est exprimée par la quantité massique d'une substance dans 100 parties en masse d'un solvant (par exemple, g/100 g).
Concentration volumique. La concentration volumique est la quantité massique d'une substance dissoute dans un certain volume de solution (par exemple : mg/l, g/m3).
Concentration molaire. La concentration molaire est le nombre de moles d'une substance donnée dissoutes dans un certain volume de solution (mol/m3, mmol/l, µmol/ml).
Concentration molale. La concentration molaire est le nombre de moles d'une substance contenue dans 1 000 g de solvant (mol/kg).
Tableau A.1.2
La relation entre les unités de mesure de la granulométrie (granulés) des matériaux filtrants selon SI et les normes d'autres pays
Solution normale. Une solution est dite normale si elle contient un équivalent d'une substance par unité de volume, exprimé en unités de masse : 1H = 1 mg eq/l = 1 mmol/l (indiquant l'équivalent d'une substance spécifique).
Équivalent. L'équivalent est égal au rapport de la partie de la masse d'un élément (substance) qui ajoute ou remplace dans composé chimique une masse atomique d'hydrogène ou la moitié de la masse atomique d'oxygène, pour 1/12 de la masse de carbone12. Ainsi, l'équivalent d'un acide est égal à son poids moléculaire, exprimé en grammes, divisé par la basicité (le nombre d'ions hydrogène) ; équivalent de base - poids moléculaire divisé par l'acidité (le nombre d'ions hydrogène et pour les bases inorganiques - divisé par le nombre de groupes hydroxyle) ; équivalent sel - poids moléculaire divisé par la somme des charges (valence des cations ou des anions) ; l'équivalent d'un composé participant aux réactions redox est le quotient du poids moléculaire du composé divisé par le nombre d'électrons acceptés (donnés) par un atome de l'élément réducteur (oxydant).
Quelques exemples : HCl + NaOH = NaCl + H2O. (P.1.1)
Les masses équivalentes d'acide chlorhydrique et d'hydroxyde de sodium dans cette réaction sont égales aux masses moléculaires de ces substances, puisqu'un ion hydrogène est impliqué dans la réaction : H3PO4 + NaOH = NaH2PO4 + H2O ; (A.1.2) H3PO4 + 2NaOH = Na2HPO4 + 2H2O. (P.1.3)
Dans la réaction (A.1.2) de neutralisation de H3PO4, la masse équivalente d'acide phosphorique est égale à son poids moléculaire - 98 (un ion hydrogène est impliqué), dans la réaction (A.1.3) - la moitié du poids moléculaire - 49 ( deux ions hydrogène sont impliqués). Par conséquent, une même substance peut avoir des masses équivalentes différentes selon le type de réaction.
2KMnO4 + 10FeSO4 + 8H2SO4 = K2SO4 + 2MnSO4 + 5Fe2(SO4)3 + 8H2O. (P.1.4)
Dans cette réaction, les ions manganèse heptavalents sont convertis en ions divalents : Mn+7 + 5е→ Mn2+ – cinq électrons sont ajoutés à chaque ion manganèse. Ces électrons sont « acquis » à partir d’ions fer divalents, qui sont convertis en ions trivalents : Fe2+ – e→ Fe3+.
Au total, dix électrons (dix molécules de FeSO4) participent à la réaction. Un électron correspond à 2/10 du poids moléculaire de KMnO4 et à 10/10 du poids moléculaire de FeSO4. Cela signifie que dans cette réaction la masse équivalente de KMnO4 est égale à 1/5 de la masse moléculaire, et la masse équivalente de FeSO4 est égale à la masse moléculaire 
Citation selon F.I. Bélan.
Désignations acceptées :
ρ – densité de la solution, g/cm3 ;
m – masse moléculaire de la substance dissoute, g/mol ;
E est la masse équivalente de la substance dissoute, c'est-à-dire la quantité de substance en grammes qui interagit dans une réaction donnée avec un atome-gramme d'hydrogène ou correspond à la transition d'un électron.
P.1.32. Dureté et alcalinité de l'eau
Selon GOST 8.417-2002, l'unité de quantité d'une substance est établie : unités molaires, multiples et sous-multiples (kmol, mmol, µmol). L'unité SI de mesure de la dureté est mmol/l ; µmol/l.
DANS différents pays Souvent, les unités de dureté de l'eau annulées continuent à être utilisées :
Russie et pays de la CEI – mEq/l, μg-eq/l, g-eq/m3 ; Allemagne, Autriche, Danemark et quelques autres pays du groupe des langues germaniques – 1 degré allemand – (Н° – Harte – dureté) ≡ 1 part de CaO/100 000 parts d'eau ≡ 10 mg CaO/l ≡ 7,14 mg MgO/ l ≡ 17,9 mg CaCO3/l ≡ 28,9 mg Ca(HCO3)2/l ≡ 15,1 mg MgCO3/l ≡ 0,357 mmol/l.
1 degré français ≡ 1 part de CaCO3/100 mille parts d'eau ≡ 10 mg CaCO3/l ≡ 5,2 mg CaO/l ≡ 0,2 mmol/l. 1 degré anglais ≡ 1 grain/1 gallon d'eau ≡ 1 partie de CaCO3/70 mille parties d'eau ≡ 0,0648 g de CaCO3/4,546 l ≡ ≡ 100 mg de CaCO3/7 l ≡ 7,42 mg de CaO/l ≡ 0,285 mmol/ l.
Parfois, le degré de dureté anglais est noté Clark.
1 degré américain ≡ 1 partie de CaCO3/1 million de parties d'eau ≡ 1 mg de CaCO3/l ≡ 0,52 mg de CaO/l ≡ 0,02 mmol/l.
Ici : h. – partie ; la conversion des degrés en leurs quantités correspondantes de CaO, MgO, CaCO,3 Ca(HCO3)2, MgCO3 est présentée à titre d'exemple principalement pour les degrés allemands ; Les dimensions des degrés sont liées aux composés contenant du calcium, puisque le calcium dans la composition des ions de dureté est généralement de 75 à 95 %, dans de rares cas – de 40 à 60 %. Les nombres sont généralement arrondis à la deuxième décimale.
L'Organisation internationale de normalisation (ISO) et l'Union internationale de chimie pure et appliquée (IUPAC) n'ont pas inclus l'unité de mesure équivalente en gramme dans leurs publications depuis 1973 et 1975, respectivement. Et les degrés de rigidité étaient auparavant absents des recommandations de ces organisations.
Cette apparente contradiction est résolue depuis longtemps. Et l'ISO, l'IUPAC et le Conseil scientifique sur chimie analytique b. L'Académie des sciences de l'URSS (« Journal of Analytical Chemistry », vol. XXXXVII, numéro 5, pp. 946-961) a établi : mmol est la quantité de substance - dans ce contexte - dans une solution qui contient le même nombre d'unités structurelles tel que contenu dans 12 g de carbone12. Et c'est établi : le nombre de toutes les unités - tant réelles que conventionnelles - se mesure en taupes. Unités réelles structurelles : atomes, ions, radicaux, électrons, molécules, complexes. Unités conventionnelles structurelles : équivalents de substances, par exemple 1/2 Ca2+, 1/2 SO 2, etc.
Dans le même temps, la notion d’équivalence demeure bien entendu. Et il est donc nécessaire d'indiquer de quelle unité structurelle nous parlons.
Par exemple, n = 1 mmol/l ; n = 4 mmol/l ; n = 5 mmol/l, etc. Lors de l'écriture après un nombre, l'unité « taupe » n'est pas déclinée en cas. GOST 6055-86 « Eau. "Unités de dureté" établit également clairement : l'unité de dureté est mol/m3. La dureté totale est la somme des concentrations molaires des équivalents des ions Ca (1/2 Ca2+) et Mg (1/2 Mg2+). La quantité d'une substance équivalente est la quantité d'une substance en moles dans laquelle les particules sont équivalentes.
Le rapport entre les unités de dureté de l'eau mentionnées : 1 mmol/l = 1 mg eq/l = 2,80°H (degrés allemands) = 5,00 degrés français = 3,51 degrés anglais = 50,04 degrés américains.
Depuis le 1er janvier 2005, GOST R 52029-2003 « Eau. Unité de dureté." GOST s'applique à l'eau naturelle et potable. Contrairement aux règles ISO, ce GOST introduit une nouvelle unité de mesure de la dureté de l'eau - le degré de dureté russe - °Zh, défini comme la concentration d'un élément alcalino-terreux (principalement Ca2+ et Mg2+), numériquement égal à 1⁄2 de sa mole en mg/dm3 (g/m3).
Les unités d'alcalinité sont mmol, µmol.
P.1.33. Conductivité électrique spécifique et résistance électrique
L'unité SI de conductivité électrique est µS/cm. La conductivité électrique des solutions et sa résistance électrique inverse caractérisent la minéralisation des solutions, mais uniquement la présence d'ions. Lors de la mesure de la conductivité électrique, les substances non ioniques ne peuvent pas être prises en compte. matière organique, impuretés neutres en suspension, interférences faussant les résultats - gaz, etc. Il est impossible par calcul de trouver avec précision une correspondance entre les valeurs de conductivité électrique spécifique et le résidu sec ou même la somme de toutes les substances déterminées séparément de la solution , puisque dans l'eau naturelle, différents ions ont une conductivité électrique spécifique différente, qui dépend simultanément de la minéralisation de la solution et de sa température. Pour établir une telle dépendance, il est nécessaire d'établir expérimentalement la relation entre ces quantités pour chaque objet spécifique plusieurs fois par an.
1 µS/cm = 1 MΩ cm ; 1 S/m = 1 Ohm·m.
Pour les solutions pures de chlorure de sodium (NaCl) dans le distillat, le rapport approximatif est : 1 µS/cm ≈ 0,5 mg NaCl/l.
Le même rapport (environ), compte tenu des réserves ci-dessus, peut être accepté pour la plupart des eaux naturelles avec une minéralisation jusqu'à 500 mg/l (tous les sels sont convertis en NaCl).
Lorsque la minéralisation naturelle de l’eau est de 0,8 à 1,5 g/l, on peut prendre : 1 µS/cm ≈ 0,65 mg de sels/l, et lorsque la minéralisation est de 3 à 5 g/l : 1 µS/cm ≈ 0,8 mg de sels/l.
P.1.34. Teneur en impuretés en suspension dans l'eau, transparence et turbidité de l'eau La teneur en impuretés en suspension est mesurée
en mg/l, transparence – en cm.
La turbidité de l'eau est exprimée en unités :
JTU (Jackson Turbidity Unit) – Unité de turbidité Jackson ;
FTU (Formasin Turbidity Unit, également désigné EMF) – unité de turbidité pour la formazine ;
NTU (Nephelometric Turbidity Unit) – unité de turbidité néphélométrique.
Il est impossible de donner un rapport exact entre les unités de turbidité et la teneur en matières en suspension. Pour chaque série de déterminations, il est nécessaire de construire une courbe d'étalonnage permettant de déterminer la turbidité de l'eau analysée par rapport à l'échantillon témoin. Vous pouvez à peu près imaginer :
1 mg/l (matières en suspension) ≡ 1–5 NTU.
Si le mélange trouble (terre de diatomées) a une granulométrie de 325 mesh, alors : 10 unités. NTU ≡ 4 unités JTU.
GOST 3351-74* et SanPiN 2.1.4.1074-01 équivalent à 1,5 unités. NTU (ou 1,5 mg/l pour la silice ou le kaolin) 2,6 unités. FTU (FEM).

P.1.35. Minéralisation
Unité de mesure SI – mg/l, g/m3, µg/l.
Aux États-Unis et dans certains autres pays, la minéralisation est exprimée en unités relatives (parfois en grains par gallon, gr/gal) :
ppm (parties par million) – partie par million (1 · 10-6) d'une unité ; parfois ppm (parties pour mille) signifie également un millième (1 · 10-3) d'unité ;
ррb – (parties par milliard) milliardième (milliardième) fraction (1 · 10-9) d'une unité ;
ppt – (parties par billion) billionième partie (1 · 10-12) d'une unité ;
‰ – ppm (également utilisé en Russie) – millième partie (1 · 10-3) d'une unité.
La relation entre les unités de minéralisation :
1 mg/l=1ppm=1·103ppm=1·106ppt=1·10-3‰= =1·10-4%;1gr/gal=17,1ppm=17,1mg/l= = 0,142 lb/1000 gal.
Pour mesurer la minéralisation des eaux salées, des saumures et la teneur en sel des condensats, il est plus correct d'utiliser les unités suivantes : mg/kg. Dans les laboratoires, les échantillons d'eau sont mesurés en volume et non en fractions de masse, par conséquent, dans la plupart des cas, il est conseillé de rapporter la quantité d'impuretés au litre. Mais pour des valeurs de minéralisation grandes ou très petites l’erreur sera sensible.
Selon SI, le volume se mesure en dm3, mais la mesure en litres est également autorisée, car 1 l = 1,000028 dm3. Depuis 1964, 1 litre équivaut à 1 dm3 (exactement).
Pour les eaux salées et les saumures, des unités de salinité en degrés Baumé sont parfois utilisées (pour salinité > 50 g/kg) : 1°Be correspond à une concentration de la solution égale à 1% en NaCl. 1% NaCl = 10 g NaCl/kg.
P.1.36. Résidu sec et calciné
Mesuré en mg/l. Le résidu sec ne caractérise pas complètement la minéralisation de la solution, car les conditions de sa détermination (ébullition, séchage du résidu solide en étuve à une température de 102-110°C jusqu'à poids constant) faussent le résultat : notamment une partie des bicarbonates (conventionnellement acceptés comme moitié) se décompose et se volatilise sous forme de CO2.
P.1.37. Caractéristiques des fibres textiles
Numéro métrique (N - obsolète) - le rapport entre la longueur du fil (fibre textile) en mètres et son poids en grammes, m/g.
Tex (T) (du latin : texo - tisser, tisser) - le rapport entre la masse d'un fil (fibre) en grammes et sa longueur en kilomètres, g/km. T = 1000 / N · 1 T = 10-6 kg/m.
Le nombre de fils retors est indiqué par une fraction : le numérateur est le nombre d'un fil individuel, le dénominateur est le nombre de fils dans un brin (brin). Exemple : filtre diagonale N 20/5 - le fil est retordu à partir de fils primaires n°20 et se compose de 5 plis.
P.1.38. Multiples et sous-multiples décimaux de quantités
De plus, leurs noms et désignations doivent être formés à l'aide des facteurs et préfixes indiqués dans le tableau. P.1.7.
| Brève entrée | Signification | Traduction et notes russes |
| Bbl, bbl | baril(s) | Baril de pétrole |
| B/D, b/d | barils par jour | Barils par jour |
| DSCF | pied cube standard sec | Pied cube normal sec |
| EA, EA | Chaque par exemple. Réservoirs de stockage d'eau potable (2 chacun) | Des choses ( par exemple : Réservoirs pour stocker l'eau potable (2 pcs.)) |
| E.A. | chaque ( par exemple. 70,00 $/heure-homme chacun) | Pour chaque ( par exemple : 70 $/(heure-homme) chacun) |
| gpg | grains par gallon (ppm = 17,1 gallons par gallon) | Grains par gallon (unité de concentration) |
| gpm | gallons par minute | Gpm |
| h. p. | puissance en chevaux | Puissance ( Britanique) |
| dans les toilettes | pouces de colonne d'eau | Pouces de colonne d'eau ( basse pression, vide) |
| kli | 1 000 pli = 1 000 livres/pied linéaire | Milliers de livres par pouce linéaire |
| kp = kips | 1000 livres | Kilopound (milliers de livres) |
| ksi | 1 000 livres par pouce carré | mille livres par pouce carré |
| lb, LBS | Balance | Kg |
| livre·m | balance de masse | Masse en livres |
| lb f | balance de force | Force livre (voir aussi #) |
| l/c/d | litre par habitant et par jour | l/(personne-jour) |
| LF | pied linéaire | Pieds linéaires |
| désactivé | Des choses ( contrairement au kit). voir également pc, pcs, EA, EA. | |
| ordinateur ; pièces | pc = pièce ; pcs = pièces | Des choses. voir également off, EA, ea. |
| PCF | livres/pieds cubes | Livre par pied cube |
| plf | livres/pieds linéaires | Livre par pied linéaire |
| PS | pferdestarke (PS = 0,986 ch) | Puissance ( Allemand et russe ; on le retrouve souvent dans les textes anglais. langue) |
| psf | livres/m². pied | Livres par pied carré |
| psi | livres/m². pouce = lb/pi². pouce | Livres par pouce carré ( psi pouce) |
| psia | livres/m². pouce, absolu | Livres par pouce carré absolu (pression absolue) |
| psid | livres/m². pouces, différentiel | PSI, différentiel (la chute de pression) |
| psig | livres/m². pouce, jauge | Livres par pouce carré, jauge (surpression) |
| Qt/mi | quart par mile | quart par mile (unité de mesure de la consommation d'essence) |
| r.m. | mètre courant | Mètre linéaire ( p.m.) |
| tr/min | révolutions par minute | Régime (tr/min) |
| SCFM | pied cube standard par minute | Normale ( ceux. à température et pression normales) pieds cubes par minute |
| carré pi, S.F. | pieds carrés | Pied carré (pi²; pi 2) |
| 1/TE (par exemple $/TE) | par tonne | Par tonne (1/t) |
Système de mesures anglo-américain
| Nom | Rapport inverse | ||
| Poids | |||
| 1 once (oz) | g | 28,3500 | 0,0353 |
| 1 livre livre (lb) = 16 onces | kg | 0,4536 | 2,2046 |
| 1 pierre = 14 livres | kg | 6,3500 | 0,1575 |
| 1 quintal court de poids à main (cwt) (net, court) = 100 livres | kg | 45,3600 | 0,0220 |
| 1 quintal long (brut, long) = 112 livres | kg | 50,8000 | 0,0197 |
| 1 tonne courte tonne (ne) (sh.tn) | kg | 907,1800 | 0,0011 |
| 1 tonne longue tonne (ne) (tn) | kg | 1 016,0000 | 0,0010 |
| Mesures linéaires | |||
| 1 point | mm | 0,3528 | 2,8345 |
| 1 ligne ligne = 6 points | mm | 2,1000 | 0,4762 |
| 1 pouce (po) = 12 lignes | cm | 2,5400 | 0,3937 |
| 1 pied pied (pi) = 12 pouces | cm | 30,4800 | 0,0328 |
| 1 verge (yd) = 3 pieds = 36 pouces | m | 0,9144 | 1,0936 |
| 1 furlong (fourrure) = 220 mètres | m | 201,1700 | 0,0050 |
| 1 mile mile (ml) = 5280 pieds = 1760 yards = 8 stades | kilomètres | 1,6093 | 0,6214 |
| 1 mille marin naut. mile = 6080 pieds | kilomètres | 1,8320 | 0,5459 |
| Mesures de zone | |||
| 1 m² pouce pouce carré (po2) | cm2 | 6,4516 | 0,1550 |
| 1 m² pied carré (pi2) | cm2 | 929,0300 | 0,0011 |
| 1 m² verge carrée (yd2) | m2 | 0,8361 | 1,1960 |
| 1 acre acre (a) | m2 | 4 047,0000 | 0,0002 |
| 1 m² mile mile carré (ml2) | km2 | 2,5890 | 0,3862 |
| 1 canton = 36 milles carrés | km2 | 93,2400 | 0,0107 |
| Mesures de volumes | |||
| 1 cu. pouce pouce cube (po3) | cm3 | 16,3870 | 0,0610 |
| 1 cu. pied cube (pi3) = 1 728 pieds cubes pouce | m3 | 0,0283 | 35,3145 |
| 1 cu. verge cube (yd3) = 27 verges cubes pied | m3 | 0,7646 | 1,3080 |
| 1 pile pile = 4 cu. cour | m3 | 3,0400 | 0,3289 |
| 1 cu. mile mile cube (ml3) | km3 | 4,1682 | 0,2399 |
| Mesures liquides | |||
| 1 fl oz d'once liquide (États-Unis) | ml | 29,5700 | 0,0338 |
| 1 fl oz d'once liquide (Royaume-Uni) | ml | 28,4000 | 0,0352 |
| 1 branchie (États-Unis) | je | 0,1180 | 8,4746 |
| 1 branchie (Royaume-Uni) | je | 0,1420 | 7,0423 |
| 1 pinte pinte (pt) = 16 fl oz (US) | je | 0,4732 | 2,1133 |
| 1 pinte pinte (pt) = 20 fl oz (Royaume-Uni) | je | 0,5700 | 1,7544 |
| 1 quart de quart (qt) = 2 pintes (US) | je | 0,9464 | 1,0567 |
| 1 quart de quart (qt) = 2 pintes (Royaume-Uni) | je | 1,1400 | 0,8772 |
| 1 gallon (gal) = 4 quarts = 8 pintes (US) | je | 3,7854 | 0,2642 |
| 1 gallon (gal) = 4 quarts = 8 pintes (Royaume-Uni) | je | 4,5460 | 0,2200 |
| 1 baril baril (USA) | je | 119,2400 | 0,0084 |
| 1 baril de baril (Royaume-Uni) | je | 160,4200 | 0,0062 |
| 1 baril de pétrole | je | 158,9800 | 0,0063 |
Mesures de volume anglo-américaines utilisées dans les ménages
| Nom | Valeur en système métrique | Rapport inverse | |
| 1 cuillère à café de cuillère à café (t ou cuillère à café) | ml | 4,9000 | 0,2041 |
| 1 cuillère à soupe cuillère à soupe (T ou cuillère à soupe) | ml | 14,9000 | 0,0671 |
| 1 verre de verre à vin | ml | 56,8000 | 0,0176 |
| 1 tasse en verre (c) | ml | 236,0000 | 0,0042 |
Mesures de volume de bois
| Nom | Valeur métrique | Rapport inverse | |
| 1 petite corde (pour bois rond) corde (courte) | m3 | 3,5680 | 0,2803 |
| 1 corde grosse corde (brut) (pour bois de chauffage) | m3 | 4,6720 | 0,2140 |
| 1 norme = 165 pieds cubes | m3 | 4,6723 | 0,2140 |
| 1 Faden = 216 cm3 pied cube = 6,11643 m3 | m3 | 6,1164 | 0,1635 |
Système de mesures de Troie pour les métaux précieux et les pierres précieuses
| Nom | Valeur métrique | Rapport inverse | |
| 1 grain | mg | 64,7990 | 0,0154 |
| 1 carat = 3,086 grains | mg | 200,0000 | 0,0050 |
| 1 once (oz) = 480 grains | g | 31,1030 | 0,0322 |
| 1 livre (lb) = 12 onces | kg | 0,3732 | 2,6792 |
Conversion d'autres grandeurs physiques
| Nom | Valeur métrique | Rapport inverse | |
| UNITÉS DE PUISSANCE | |||
| Puissance | W | 745,7000 | 0,0013 |
| UNITÉS DE TEMPÉRATURE | |||
| Température Fahrenheit | F° = (C° x 9/5) + 32 | C° = (F° - 32) x 5/9 | |
| Réaumur température | Tr = 4/5Tc | TC = 5/4Tr | |
| Température absolue | Tk = Tc+273,16 | Tc = Tc-273,16 | |
| VALEURS ASTRONOMIQUES | |||
| Parsec | kilomètres | 30 860 000 000 000 | |
| Année-lumière | kilomètres | 945 750 000 000 | |
| Unité astronomique | kilomètres | 149 613 400 | |
| Minute-lumière | kilomètres | 17 993 800 | |
| Seconde lumière | kilomètres | 299 896,943 | |
| UNITÉS DE PRESSION | |||
| Pouce de mercure | Pennsylvanie | 3386,37526 | |
| Centimètre de mercure | Pennsylvanie | 1333,21957 | |
| Millimètre de mercure | Pennsylvanie | 133,321957 | |
| Atmosphère | Pennsylvanie | 101325,025 | |
| UNITÉS DE VITESSE | |||
| Noeud | km/h | 1,8520043 | |
| Miles par heure | km/h | 1,6093444 | |
quantité de chaleur
La méthode de réglage des valeurs de température est l'échelle de température. Plusieurs échelles de température sont connues.
- Échelle Kelvin(du nom du physicien anglais W. Thomson, Lord Kelvin).
Désignation de l'unité : K(pas de « degré Kelvin » ni de °K).
1 K = 1/273,16 - partie de la température thermodynamique du point triple de l'eau, correspondant à l'équilibre thermodynamique d'un système constitué de glace, d'eau et de vapeur. - Celsius(du nom de l'astronome et physicien suédois A. Celsius).
Désignation de l'unité : °C .
Dans cette échelle, la température de fusion de la glace à pression normale est de 0°C et le point d’ébullition de l’eau est de 100°C.
Les échelles Kelvin et Celsius sont liées par l'équation : t (°C) = T (K) - 273,15. - Fahrenheit(D. G. Fahrenheit - physicien allemand).
Symbole de l'unité : °F. Largement utilisé, notamment aux USA.
L'échelle Fahrenheit et l'échelle Celsius sont liées : t (°F) = 1,8 · t (°C) + 32°C. En valeur absolue, 1 (°F) = 1 (°C). - Échelle de Réaumur(du nom du physicien français R.A. Réaumur).
Désignation : °R et °r.
Cette balance est quasiment hors d'usage.
Rapport aux degrés Celsius : t (°R) = 0,8 t (°C). - Échelle de Rankin (Rankine)- du nom de l'ingénieur et physicien écossais W. J. Rankin.
Désignation : °R (parfois : °Rank).
Cette échelle est également utilisée aux États-Unis.
La température sur l'échelle de Rankine est liée à la température sur l'échelle Kelvin : t (°R) = 9/5 · T (K).
Indicateurs de température de base en unités de mesure de différentes échelles :

L'unité de mesure SI est le mètre (m).
- Unité non système : Angström (Å). 1Å = 1·10-10 m.
- Pouce(du néerlandais duim - pouce) ; pouce; dans; ''; 1´ = 25,4 millimètres.
- Main(main anglaise - main); 1 aiguille = 101,6 mm.
- Lien(Lien anglais - lien); 1 li = 201,168 mm.
- Portée(Span anglais - span, scope) ; 1 travée = 228,6 mm.
- Pied(pied anglais - jambe, pieds - pieds); 1 pied = 304,8 mm.
- Cour(Cour anglaise - cour, corral) ; 1 mètre = 914,4 mm.
- Visage gras(Bathom anglais - mesure de longueur (= 6 pi), ou mesure de volume de bois (= 216 pi 3), ou mesure de superficie de montagne (= 36 pi 2), ou brasse (Ft)); fath ou fth ou Ft ou ƒfm; 1 pied = 1,8288 m.
- Cheyne(chaîne anglaise - chaîne); 1 ch = 66 pi = 22 yd = = 20,117 m.
- Furlong(eng. furlong) - 1 fourrure = 220 mètres = 1/8 mile.
- mile(mile anglais ; international). 1 ml (mi, MI) = 5 280 pieds = 1 760 yd = 1 609,344 m.
L'unité SI est le m2.
- Pied carré; 1 pi 2 (également pied carré) = 929,03 cm 2.
- Pouce carré ; 1 sur 2 (po²) = 645,16 mm 2.
- Brasse carrée (fesom); 1 fath 2 (pi 2; Pi 2; Pi carré) = 3,34451 m 2.
- Yard carré; 1 yd 2 (yd carré) = 0,836127 m 2 .
Sq (carré) - carré.
L'unité SI est m3.
- Pied carré; 1 pi 3 (également pi cu) = 28,3169 dm 3.
- Brasse cubique ; 1 fath 3 (fth 3; Ft 3; cu Ft) = 6,11644 m 3.
- Verge cube ; 1 yd 3 (yd cube) = 0,764555 m 3.
- Pouce cube ; 1 sur 3 (pouces cubes) = 16,3871 cm 3.
- Boisseau (Royaume-Uni); 1 bu (Royaume-Uni, également Royaume-Uni) = 36,3687 dm 3.
- Boisseau (États-Unis) ; 1 bu (nous, également US) = 35,2391 dm 3.
- Gallon (Royaume-Uni); 1 gal (Royaume-Uni, également Royaume-Uni) = 4,54609 dm 3.
- Gallon de liquide (États-Unis); 1 gal (nous, également US) = 3,78541 dm 3.
- Gallon sec (États-Unis); 1 gal sec (nous, également US) = 4,40488 dm 3.
- Jill (branchie); 1 gi = 0,12 l (États-Unis), 0,14 l (Royaume-Uni).
- Baril (États-Unis); 1 baril = 0,16 m3.
Royaume-Uni – Royaume-Uni – Royaume-Uni (Grande-Bretagne) ; États-Unis - États-Unis (États-Unis).
Volume spécifique
L'unité de mesure SI est le m 3 /kg.
- pi 3/lb ; 1 pi3/lb = 62,428 dm3/kg .
L'unité de mesure SI est le kg.
- Pound (commerce) (Balance anglaise, livre - pesée, livre); 1 livre = 453,592 g; livres - livres. Dans le système des anciennes mesures russes 1 livre = 409,512 g.
- Gran (grain anglais - grain, grain, grain); 1 gr = 64,799 mg.
- Pierre (eng. pierre - pierre); 1 maille = 14 lb = 6,350 kg.
Densité, incl. en gros
L'unité de mesure SI est le kg/m3.
- lb/pi 3 ; 1 lb/pied 3 = 16,0185 kg/m 3.
Densité linéaire
L'unité SI est kg/m.
- lb/pi ; 1 lb/pied = 1,48816 kg/m
- Livre/Yard ; 1 lb / yd = 0,496055 kg/m
Densité surfacique
L'unité SI est kg/m2.
- lb/pi 2 ; 1 lb / pi 2 (également lb / pied carré - livre par pied carré) = 4,88249 kg/m2.
Vitesse linéaire
L'unité SI est m/s.
- pieds/h ; 1 pied/h = 0,3048 m/h.
- pieds/s ; 1 pied/s = 0,3048 m/s.
L'unité SI est m/s2.
- pi/s 2 ; 1 pi/s2 = 0,3048 m/s2.
Débit massique
L'unité SI est kg/s.
- lb/h ; 1 lb/h = 0,453592 kg/h.
- Kg; 1 lb/s = 0,453592 kg/s.
Débit volumique
L'unité de mesure SI est le m 3 /s.
- pi 3 /min ; 1 pied 3 / min = 28,3168 dm 3 / min.
- Cour 3/min ; 1 yd 3 / min = 0,764555 dm 3 / min.
- Gpm ; 1 gal/min (également GPM - gallon par min) = 3,78541 dm 3 /min.
Débit volumique spécifique
- GPM/(pieds carrés) - gallon (G) par (P) minute (M)/(carré (pieds carrés) · pied (pieds)) - gallons par minute par pied carré ;
1 GPM/(pied carré) = 2445 l/(m 2 h) 1 l/(m 2 h) = 10 -3 m/h. - gpd - gallons par jour - gallons par jour (jour) ; 1 gpd = 0,1577 dm 3 /h.
- gpm - gallons par minute - gallons par minute ; 1 gpm = 0,0026 dm3/min.
- GPS - gallons par seconde - gallons par seconde ; 1 gps = 438 10 -6 dm 3 /s.
Consommation de sorbate (par exemple, Cl 2) lors de la filtration à travers une couche de sorbant (par exemple, charbon actif)
- Gals/pied cube (gal/pied 3) - gallons/pied cube (gallons par pied cube) ; 1 Gals/pi3 = 0,13365 dm 3 pour 1 dm 3 de sorbant.
L'unité de mesure SI est N.
- Livre-force ; 1 lbf - 4,44822 N. (Un analogue du nom de l'unité de mesure : kilogramme-force, kgf. 1 kgf = = 9,80665 N (exact). 1 lbf = 0,453592 (kg) 9,80665 N = = 4 .44822 N 1N =1 kgm/s2
- Poundal (anglais : livre); 1 pdl = 0,138255 N. (Poundall est la force qui donne à une masse d'une livre une accélération de 1 pi/s 2, lb pi/s 2.)
Densité spécifique
L'unité de mesure SI est N/m 3 .
- lbf/pied 3 ; 1 lbf/pied 3 = 157,087 N/m 3.
- Livre/pied 3 ; 1 pdl/pied 3 = 4,87985 N/m 3.
Unité de mesure SI - Pa, plusieurs unités : MPa, kPa.
Dans leur travail, les spécialistes continuent d'utiliser des unités de mesure de pression obsolètes, annulées ou précédemment acceptées en option : kgf/cm2; bar; au m. (atmosphère physique); à(atmosphère technique); à; ati; m d'eau Art.; mmHg St; torr.
Les notions suivantes sont utilisées : « pression absolue », « surpression ». Il y a des erreurs lors de la conversion de certaines unités de pression en Pa et ses multiples. Il faut tenir compte du fait que 1 kgf/cm 2 est égal à 98066,5 Pa (exactement), c'est-à-dire que pour de petites pressions (jusqu'à environ 14 kgf/cm 2) avec une précision suffisante pour le travail, les éléments suivants peuvent être acceptés : 1 Pa = 1 kg/(m s 2) = 1 N/m 2. 1 kgf/cm 2 ≈ 105 Pa = 0,1 MPa. Mais déjà à moyennes et hautes pressions : 24 kgf/cm 2 ≈ 23,5 · 105 Pa = 2,35 MPa ; 40 kgf/cm2 ≈ 39 · 105 Pa = 3,9 MPa ; 100 kgf/cm2 ≈ 98 105 Pa = 9,8 MPa etc.
Rapports :
- 1 atm (physique) ≈ 101325 Pa ≈ 1,013 105 Pa ≈ ≈ 0,1 MPa.
- 1 à (technique) = 1 kgf/cm 2 = 980066,5 Pa ≈ ≈ 105 Pa ≈ 0,09806 MPa ≈ 0,1 MPa.
- 0,1 MPa ≈ 760 mmHg. Art. ≈ 10 m d'eau. Art. ≈ 1 barre.
- 1 Torr (tor) = 1 mm Hg. Art.
- lb/po 2 ; 1 lbf/in 2 = 6,89476 kPa (voir ci-dessous : PSI).
- lbf/pied 2 ; 1 lbf/pied 2 = 47,8803 Pa.
- lbf/vg 2 ; 1 lbf/yd 2 = 5,32003 Pa.
- Livre/pied 2 ; 1 pdl/pied 2 = 1,48816 Pa.
- Colonne d'eau au pied ; 1 pied H 2 O = 2,98907 kPa.
- Pouce de colonne d’eau ; 1 dans H 2 O = 249,089 Pa.
- Pouce de mercure ; 1 po Hg = 3,38639 kPa.
- PSI (également psi) - livres (P) par pouce carré (S) (I) - livres par pouce carré ; 1 PSI = 1 lbƒ/po 2 = 6,89476 kPa.
Parfois, dans la littérature, vous pouvez trouver la désignation de l'unité de pression lb/in 2 - cette unité ne prend pas en compte lbƒ (livre-force), mais lb (livre-masse). Par conséquent, en termes numériques, 1 lb/ sur 2 est légèrement différent de 1 lbf/ sur 2, puisque lors de la détermination de 1 lbƒ, il est pris en compte : g = 9,80665 m/s 2 (à la latitude de Londres). 1 lb/po 2 = 0,454592 kg/(2,54 cm) 2 = 0,07046 kg/cm 2 = 7,046 kPa. Calcul de 1 lbƒ - voir ci-dessus. 1 lbf/in 2 = 4,44822 N/(2,54 cm) 2 = 4,44822 kg m/ (2,54 0,01 m) 2 s 2 = 6894,754 kg/ (m s 2) = 6894,754 Pa ≈ 6,895 kPa.
Pour les calculs pratiques, nous pouvons supposer : 1 lbf/po 2 ≈ 1 lb/po 2 ≈ 7 kPa. Mais en fait, l’égalité est illégale, tout comme 1 lbƒ = 1 lb, 1 kgf = 1 kg. PSIg (psig) - identique à PSI, mais indique une pression manométrique ; PSIa (psia) - le même que le PSI, mais met l'accent sur : la pression absolue ; a - absolu, g - jauge (mesure, taille).
Pression de l'eau
L'unité de mesure SI est m.
- Tête en pieds (pieds-tête) ; 1 pied de hauteur = 0,3048 m
Perte de pression pendant la filtration
- PSI/pied - livres (P) par pouce carré (S) pouce (I)/pied (pied) - livres par pouce carré/pied ; 1 PSI/pied = 22,62 kPa pour 1 m de couche filtrante.
TRAVAIL, ÉNERGIE, QUANTITÉ DE CHALEUR |
Unité de mesure SI - Joule(du nom du physicien anglais J.P. Joule).
- 1 J - travail mécanique de force 1 N lors du déplacement d'un corps sur une distance de 1 m.
- Newton (N) est l'unité SI de force et de poids ; 1 Н est égal à la force conférant à un corps pesant 1 kg une accélération de 1 m 2 /s dans la direction de la force. 1 J = 1 N·m.
En génie thermique, ils continuent d'utiliser l'unité de mesure abolie de la quantité de chaleur - la calorie (cal).
- 1 J (J) = 0,23885 cal. 1 kJ = 0,2388 kcal.
- 1 lbf pi (lbf) = 1,35582 J.
- 1 pdl ft (pieds livres) = 42,1401 mJ.
- 1 Btu (British Heat Unit) = 1,05506 kJ (1 kJ = 0,2388 kcal).
- 1 Therm (grande calorie britannique) = 1 10 -5 Btu.
L'unité de mesure SI est le Watt (W)- du nom de l'inventeur anglais J. Watt - puissance mécanique à laquelle 1 J de travail est effectué en 1 s, ou un flux thermique équivalent à 1 W de puissance mécanique.
- 1 W (W) = 1 J/s = 0,859985 kcal/h (kcal/h).
- 1 lbf pied/s (lbf pied/s) = 1,33582 W.
- 1 lbf pied/min (lbf pied/min) = 22,597 mW.
- 1 lbf pied/h (lbf pied/h) = 376,616 µW.
- 1 pdl pied/s (pieds livre/s) = 42,1401 mW.
- 1 ch (puissance/s britannique) = 745,7 W.
- 1 Btu/s (British Heat Unit/s) = 1 055,06 W.
- 1 Btu/h (British Heat Unit/h) = 0,293067 W.
Densité du flux thermique superficiel
L'unité SI est W/m2.
- 1 W/m2 (W/m2) = 0,859985 kcal/(m2 h) (kcal/(m2 h)).
- 1 Btu/(pied 2 h) = 2,69 kcal/(m 2 h) = 3,1546 kW/m 2.
Viscosité dynamique (coefficient de viscosité), η.
Unité SI - Pa·s. 1 Pa.s = 1 N.s/m2;
unité non systémique - équilibre (P). 1 P = 1 dyne s/m 2 = 0,1 Pa s.
- Dina (dyn) - (du grec dynamique - force). 1 dyne = 10 -5 N = 1 g cm/s 2 = 1,02 10 -6 kgf.
- 1 lbf h/pi 2 (lbf h/pi 2) = 172,369 kPa·s.
- 1 lbf s / pi 2 (lbf s/pi 2) = 47,8803 Pa.s.
- 1 pdl s / ft 2 (livre-s/ft 2) = 1,48816 Pa s.
- 1 limace /(pieds) = 47,8803 Pa.s. Slug (slug) est une unité technique de masse dans le système de mesures anglais.
Viscosité cinématique, ν.
Unité de mesure en SI - m 2 /s; L'unité cm 2 /s est appelée « Stokes » (du nom du physicien et mathématicien anglais J. G. Stokes).
Les viscosités cinématique et dynamique sont liées par l'égalité : ν = η / ρ, où ρ est la densité, g/cm 3 .
- 1 m 2 /s = Stokes / 104.
- 1 pi 2 /h (pi 2 /h) = 25,8064 mm 2 /s.
- 1 pi 2 /s (pi 2 /s) = 929,030 cm 2 /s.
Unité de tension champ magnétique en SI - A/m(Ampèremètre). Ampère (A) est le nom de famille du physicien français A.M. Ampère.
Auparavant, on utilisait l'unité Oersted (E), du nom du physicien danois H.K. Oersted.
1 A/m (A/m, At/m) = 0,0125663 Oe (Oe)
La résistance à l'écrasement et à l'abrasion des matériaux filtrants minéraux et, en général, de tous les minéraux et roches est indirectement déterminée à l'aide de l'échelle de Mohs (F. Mohs - minéralogiste allemand).
Dans cette échelle, les nombres par ordre croissant désignent les minéraux disposés de telle manière que chacun des suivants est capable de laisser une égratignure sur le précédent. Les substances extrêmes sur l'échelle de Mohs sont le talc (unité de dureté 1, la plus douce) et le diamant (10, le plus dur).
- Dureté 1-2,5 (tiré avec un ongle) : volskonkoite, vermiculite, halite, gypse, glauconite, graphite, matériaux argileux, pyrolusite, talc, etc.
- Dureté >2,5-4,5 (non dessiné avec un ongle, mais dessiné avec du verre) : anhydrite, aragonite, barytine, glauconite, dolomite, calcite, magnésite, muscovite, sidérite, chalcopyrite, chabazite, etc.
- Dureté >4,5-5,5 (non étirée au verre, mais étirée au couteau en acier) : apatite, vernadite, néphéline, pyrolusite, chabazite, etc.
- Dureté >5,5-7,0 (non étirée au couteau en acier, mais étirée au quartz) : vernadite, grenat, ilménite, magnétite, pyrite, feldspaths, etc.
- Dureté >7,0 (non marqué au quartz) : diamant, grenats, corindon, etc.
La dureté des minéraux et des roches peut également être déterminée à l'aide de l'échelle de Knoop (A. Knoop - minéralogiste allemand). Dans cette échelle, les valeurs sont déterminées par la taille de l'empreinte laissée sur le minéral lorsqu'une pyramide de diamant est pressée dans son échantillon sous une certaine charge.
Ratios d'indicateurs sur les échelles de Mohs (M) et de Knoop (K) :

Unité de mesure SI - Bq(Becquerel, du nom du physicien français A.A. Becquerel).
Bq (Bq) est une unité d'activité d'un nucléide dans une source radioactive (activité isotopique). 1 Bq est égal à l'activité d'un nucléide, à laquelle un événement de désintégration se produit en 1 s.
Concentration de radioactivité : Bq/m 3 ou Bq/l.
L'activité est le nombre de désintégrations radioactives par unité de temps. L'activité par unité de masse est dite spécifique.
- Curie (Ku, Ci, Cu) est une unité d'activité d'un nucléide dans une source radioactive (activité isotopique). 1 Ku est l'activité d'un isotope dans lequel 3,7000 · 1010 événements de désintégration se produisent en 1 s. 1 Ku = 3,7000 · 1010 Bq.
- Rutherford (Рд, Rd) est une unité obsolète d'activité de nucléides (isotopes) dans les sources radioactives, du nom du physicien anglais E. Rutherford. 1 Rd = 1 106 Bq = 1/37 000 Ci.
Dose de rayonnement
La dose de rayonnement est l'énergie des rayonnements ionisants absorbée par la substance irradiée et calculée par unité de sa masse (dose absorbée). La dose s'accumule au fil du temps d'exposition. Débit de dose ≡ Dose/temps.
Unité SI de dose absorbée - Gray (Gy, Gy). L'unité extrasystémique est Rad, correspondant à l'énergie de rayonnement de 100 erg absorbée par une substance pesant 1 g.
Erg (erg - du grec : ergon - travail) est une unité de travail et d'énergie dans le système GHS non recommandé.
- 1 erg = 10 -7 J = 1,02 10 -8 kgf m = 2,39 10 -8 cal = 2,78 10 -14 kW/h.
- 1 rad = 10 -2 Gr.
- 1 rad (rad) = 100 erg/g = 0,01 Gy = 2,388 · 10 -6 cal/g = 10 -2 J/kg.
Kerma (anglais abrégé : énergie cinétique libérée dans la matière) - énergie cinétique libérée dans la matière, mesurée en gris.
La dose équivalente est déterminée en comparant le rayonnement nucléide avec le rayonnement X. Le facteur de qualité du rayonnement (K) indique combien de fois le risque d'irradiation en cas d'exposition humaine chronique (à des doses relativement faibles) pour un type de rayonnement donné est plus grand que dans le cas d'un rayonnement aux rayons X à la même dose absorbée. Pour les rayons X et les rayonnements γ, K = 1. Pour tous les autres types de rayonnement, K est établi en fonction des données radiobiologiques.
Deq = Dpogl · K.
Unité SI de dose absorbée - 1 Sv(Sievert) = 1 J/kg = 102 rem.
- BER (rem, ri - jusqu'en 1963 était défini comme l'équivalent biologique d'un rayon X) - une unité de dose équivalente de rayonnement ionisant.
- Rayons X (P, R) - unité de mesure, dose d'exposition aux rayons X et aux rayons γ. 1 P = 2,58 10 -4 C/kg.
- Coulomb (C) est une unité SI, quantité d'électricité, charge électrique. 1 rem = 0,01 J/kg.
Débit de dose équivalent - Sv/s.
Perméabilité des milieux poreux (y compris les roches et les minéraux)
Darcy (D) - du nom de l'ingénieur français A. Darcy, darsy (D) · 1 D = 1,01972 µm 2.
1 D est la perméabilité d'un tel milieu poreux, lors de la filtration d'un échantillon d'une superficie de 1 cm 2, d'une épaisseur de 1 cm et d'une perte de charge de 0,1 MPa, le débit d'un liquide d'une viscosité de 1 cP est de 1 cm 3 /s.
Tailles des particules, grains (granulés) des matériaux filtrants selon SI et normes d'autres pays
Aux États-Unis, au Canada, en Grande-Bretagne, au Japon, en France et en Allemagne, la granulométrie est estimée en mailles (eng. mesh - trou, cellule, réseau), c'est-à-dire par le nombre (nombre) de trous par pouce du tamis le plus fin à travers lequel ils peuvent faire passer les grains Et le diamètre effectif des grains correspond à la taille du trou en microns. Ces dernières années, les systèmes maillés américains et britanniques ont été utilisés plus fréquemment.
La relation entre les unités de mesure de la granulométrie (granulés) des matériaux filtrants selon SI et les normes d'autres pays :

Fraction massique
La fraction massique indique la quantité massique d'une substance contenue dans 100 parties en masse d'une solution. Unités de mesure : fractions d'unité ; intérêt (%); ppm (‰); parties par million (ppm).
Concentration et solubilité de la solution
La concentration d'une solution doit être distinguée de la solubilité - la concentration d'une solution saturée, qui est exprimée par la quantité massique d'une substance dans 100 parties en masse d'un solvant (par exemple, g/100 g).
Concentration volumique
La concentration volumique est la quantité massique d'une substance dissoute dans un certain volume de solution (par exemple : mg/l, g/m3).
Concentration molaire
La concentration molaire est le nombre de moles d'une substance donnée dissoutes dans un certain volume de solution (mol/m3, mmol/l, µmol/ml).
Concentration molale
La concentration molaire est le nombre de moles d'une substance contenue dans 1 000 g de solvant (mol/kg).
Solution normale
Une solution est dite normale si elle contient un équivalent d'une substance par unité de volume, exprimé en unités de masse : 1H = 1 mg eq/l = 1 mmol/l (indiquant l'équivalent d'une substance spécifique).
Équivalent
L'équivalent est égal au rapport de la partie de la masse d'un élément (substance) qui ajoute ou remplace une masse atomique d'hydrogène ou la moitié de la masse atomique d'oxygène dans un composé chimique à 1/12 de la masse de carbone 12. Ainsi, l'équivalent d'un acide est égal à son poids moléculaire, exprimé en grammes, divisé par la basicité (le nombre d'ions hydrogène) ; équivalent de base - poids moléculaire divisé par l'acidité (le nombre d'ions hydrogène et pour les bases inorganiques - divisé par le nombre de groupes hydroxyle) ; équivalent sel - poids moléculaire divisé par la somme des charges (valence des cations ou des anions) ; l'équivalent d'un composé participant aux réactions redox est le quotient du poids moléculaire du composé divisé par le nombre d'électrons acceptés (donnés) par un atome de l'élément réducteur (oxydant).
Relations entre les unités de mesure de la concentration des solutions
(Formule de passage d'une expression des concentrations de solution à une autre) :

Désignations acceptées :
- ρ - densité de la solution, g/cm 3 ;
- m est le poids moléculaire de la substance dissoute, en g/mol ;
- E est la masse équivalente d'un soluté, c'est-à-dire la quantité de substance en grammes qui interagit dans une réaction donnée avec un gramme d'hydrogène ou correspond à la transition d'un électron.
Selon GOST 8.417-2002 L'unité de quantité d'une substance est établie : mole, multiples et sous-multiples ( kmol, mmol, µmol).
L'unité SI de mesure de la dureté est mmol/l ; µmol/l.
Dans différents pays, les unités supprimées pour mesurer la dureté de l'eau continuent souvent à être utilisées :
- Russie et pays de la CEI - mEq/l, mcg-eq/l, g-eq/m 3 ;
- Allemagne, Autriche, Danemark et quelques autres pays du groupe des langues germaniques - 1 degré allemand - (Н° - Harte - dureté) ≡ 1 part de CaO/100 000 parts d'eau ≡ 10 mg CaO/l ≡ 7,14 mg MgO/ l ≡ 17,9 mg CaCO 3 /l ≡ 28,9 mg Ca(HCO 3) 2 /l ≡ 15,1 mg MgCO 3 /l ≡ 0,357 mmol/l.
- 1 degré français ≡ 1 heure CaCO 3 /100 mille parties d'eau ≡ 10 mg CaCO 3 /l ≡ 5,2 mg CaO/l ≡ 0,2 mmol/l.
- 1 degré anglais ≡ 1 grain/1 gallon d'eau ≡ 1 partie de CaCO 3 /70 mille parties d'eau ≡ 0,0648 g de CaCO 3 /4,546 l ≡ 100 mg de CaCO3 /7 l ≡ 7,42 mg de CaO/l ≡ 0,285 mmol /l. Parfois, le degré de dureté anglais est noté Clark.
- 1 degré américain ≡ 1 partie de CaCO 3 /1 million de parties d'eau ≡ 1 mg de CaCO 3 /l ≡ 0,52 mg de CaO/l ≡ 0,02 mmol/l.
Ici : partie - partie ; la conversion des degrés en leurs quantités correspondantes de CaO, MgO, CaCO 3, Ca(HCO 3) 2, MgCO 3 est présentée à titre d'exemple principalement pour les diplômes allemands ; Les dimensions des degrés sont liées aux composés contenant du calcium, car le calcium dans la composition des ions de dureté est généralement de 75 à 95 %, dans de rares cas de 40 à 60 %. Les nombres sont généralement arrondis à la deuxième décimale.
La relation entre les unités de dureté de l'eau :
1 mmol/l = 1 mg eq/l = 2,80°H (degrés allemands) = 5,00 degrés français = 3,51 degrés anglais = 50,04 degrés américains.
Une nouvelle unité de mesure de la dureté de l'eau est le degré de dureté russe - °Zh, défini comme la concentration d'un élément alcalino-terreux (principalement Ca 2+ et Mg 2+), numériquement égal à ½ sa mole en mg/dm 3 ( g/m3).
Les unités d'alcalinité sont mmol, µmol.
L'unité SI de conductivité électrique est µS/cm.
La conductivité électrique des solutions et sa résistance électrique inverse caractérisent la minéralisation des solutions, mais uniquement la présence d'ions. Lors de la mesure de la conductivité électrique, les substances organiques non ioniques, les impuretés neutres en suspension, les interférences faussant les résultats - gaz, etc. ne peuvent pas être prises en compte. Il est impossible par calcul de trouver avec précision la correspondance entre les valeurs de conductivité électrique spécifique et le résidu sec ou même la somme de toutes les substances déterminées séparément de la solution, puisque dans l'eau naturelle, différents ions ont une conductivité électrique différente, qui dépend simultanément de la salinité de la solution et de sa température. Pour établir une telle dépendance, il est nécessaire d'établir expérimentalement la relation entre ces quantités pour chaque objet spécifique plusieurs fois par an.
- 1 µS/cm = 1 MΩ cm ; 1 S/m = 1 Ohm·m.
Pour les solutions pures de chlorure de sodium (NaCl) dans le distillat, le rapport approximatif est :
- 1 µS/cm ≈ 0,5 mg NaCl/l.
Le même rapport (environ), compte tenu des réserves ci-dessus, peut être accepté pour la plupart des eaux naturelles avec une minéralisation jusqu'à 500 mg/l (tous les sels sont convertis en NaCl).
Lorsque la minéralisation de l'eau naturelle est de 0,8 à 1,5 g/l, vous pouvez prendre :
- 1 µS/cm ≈ 0,65 mg sels/l,
et avec minéralisation - 3-5 g/l :
- 1 µS/cm ≈ 0,8 mg de sels/l.
Teneur en impuretés en suspension dans l'eau, transparence et turbidité de l'eau
La turbidité de l'eau est exprimée en unités :
- JTU (Jackson Turbidity Unit) - Unité de turbidité Jackson ;
- FTU (Formasin Turbidity Unit, également désigné EMF) - unité de turbidité pour la formazine ;
- NTU (Nephelometric Turbidity Unit) - unité de turbidité néphélométrique.
Il est impossible de donner un rapport exact entre les unités de turbidité et la teneur en matières en suspension. Pour chaque série de déterminations, il est nécessaire de construire une courbe d'étalonnage permettant de déterminer la turbidité de l'eau analysée par rapport à l'échantillon témoin.
À titre indicatif : 1 mg/l (matières en suspension) ≡ 1 à 5 unités NTU.
Si le mélange trouble (terre de diatomées) a une granulométrie de 325 mesh, alors : 10 unités. NTU ≡ 4 unités JTU.
GOST 3351-74 et SanPiN 2.1.4.1074-01 équivalent à 1,5 unités. NTU (ou 1,5 mg/l pour la silice ou le kaolin) 2,6 unités. FTU (FEM).
La relation entre la transparence de la police et la brume :

Relation entre transparence le long de la « croix » (en cm) et turbidité (en mg/l) :

L'unité de mesure SI est mg/l, g/m3, μg/l.
Aux États-Unis et dans certains autres pays, la minéralisation est exprimée en unités relatives (parfois en grains par gallon, gr/gal) :
- ppm (parties par million) - partie par million (1 · 10 -6) d'une unité ; parfois, ppm (parties pour mille) signifie également un millième (1 · 10 -3) d'une unité ;
- ppb - (parties par milliard) milliardième (milliardième) fraction (1 · 10 -9) d'une unité ;
- ppt - (parties par billion) billionième partie (1 · 10 -12) d'une unité ;
- ‰ - ppm (également utilisé en Russie) - millième (1 · 10 -3) d'unité.
La relation entre les unités de mesure de la minéralisation : 1 mg/l = 1ppm = 1 10 3 ppb = 1 10 6 ppt = 1 10 -3 ‰ = 1 10 -4% ; 1 gr/gal = 17,1 ppm = 17,1 mg/l = 0,142 lb/1 000 gal.
Pour mesurer la salinité des eaux salées, des saumures et la salinité des condensats Il est plus correct d'utiliser des unités : mg/kg. Dans les laboratoires, les échantillons d'eau sont mesurés en volume plutôt qu'en masse, c'est pourquoi dans la plupart des cas, il est conseillé de rapporter la quantité d'impuretés à un litre. Mais pour des valeurs de minéralisation grandes ou très petites l’erreur sera sensible.
Selon SI, le volume se mesure en dm 3, mais la mesure est également autorisée en litres, car 1 l = 1,000028 dm 3. Depuis 1964 1 l est égal à 1 dm 3 (exactement).
Pour eaux salées et saumures des unités de salinité sont parfois utilisées en degrés Baume(pour minéralisation >50 g/kg) :
- 1°Be correspond à une concentration de solution égale à 1% en NaCl.
- 1% NaCl = 10 g NaCl/kg.
Résidu sec et calciné
Les résidus secs et calcinés sont mesurés en mg/l. Le résidu sec ne caractérise pas complètement la minéralisation de la solution, car les conditions de sa détermination (ébullition, séchage du résidu solide en étuve à une température de 102-110°C jusqu'à poids constant) faussent le résultat : notamment, une partie des bicarbonates (conventionnellement acceptés - la moitié) se décompose et se volatilise sous forme de CO 2.
Multiples et sous-multiples décimaux de quantités
Les multiples décimaux et sous-multiples des unités de mesure des quantités, ainsi que leurs noms et désignations, doivent être formés à l'aide des facteurs et préfixes donnés dans le tableau :

(basé sur des matériaux du site https://aqua-therm.ru/).