1. Quels mots manquent dans la phrase et sont remplacés par des lettres (a-d) ?
"La molécule d'ATP est constituée d'une base azotée (a), d'un monosaccharide à cinq carbones (b) et (c) d'un résidu acide (d)."
Les mots suivants sont remplacés par des lettres : a – adénine, b – ribose, c – trois, d – phosphorique.
2. Comparez la structure de l'ATP et la structure d'un nucléotide. Identifiez les similitudes et les différences.
En fait, l’ATP est un dérivé du nucléotide adényle de l’ARN (adénosine monophosphate ou AMP). Les molécules des deux substances comprennent la base azotée adénine et le sucre ribose à cinq carbones. Les différences sont dues au fait que le nucléotide adényle de l'ARN (comme dans tout autre nucléotide) ne contient qu'un seul résidu d'acide phosphorique et qu'il n'y a pas de liaisons à haute énergie (haute énergie). La molécule d'ATP contient trois résidus d'acide phosphorique, entre lesquels se trouvent deux liaisons à haute énergie, de sorte que l'ATP peut agir comme une batterie et un vecteur d'énergie.
3. Quel est le processus d’hydrolyse de l’ATP ? Synthèse d'ATP ? Qu'est-ce que rôle biologique ATP ?
Au cours du processus d'hydrolyse, un résidu d'acide phosphorique est éliminé de la molécule d'ATP (déphosphorylation). Dans ce cas, la liaison à haute énergie est rompue, 40 kJ/mol d'énergie sont libérés et l'ATP est converti en ADP (acide adénosine diphosphorique) :
ATP + H 2 O → ADP + H 3 PO 4 + 40 kJ
L'ADP peut subir une hydrolyse supplémentaire (ce qui se produit rarement) avec l'élimination d'un autre groupe phosphate et la libération d'une deuxième « portion » d'énergie. Dans ce cas, l'ADP est converti en AMP (acide adénosine monophosphorique) :
ADP + H 2 O → AMP + H 3 PO 4 + 40 kJ
La synthèse de l'ATP résulte de l'ajout d'un résidu d'acide phosphorique à la molécule d'ADP (phosphorylation). Ce processus se produit principalement dans les mitochondries et les chloroplastes, en partie dans le hyaloplasme des cellules. Pour former 1 mole d'ATP à partir d'ADP, il faut dépenser au moins 40 kJ d'énergie :
ADP + H 3 PO 4 + 40 kJ → ATP + H 2 O
L'ATP est un réservoir universel (batterie) et un transporteur d'énergie dans les cellules des organismes vivants. Dans presque tous les processus biochimiques se produisant dans les cellules qui ont besoin d’énergie, l’ATP est utilisé comme fournisseur d’énergie. Grâce à l'énergie de l'ATP, de nouvelles molécules de protéines, de glucides, de lipides sont synthétisées, un transport actif de substances est effectué, le mouvement des flagelles et des cils se produit, la division cellulaire se produit, les muscles travaillent, une température corporelle constante est maintenue au chaud. animaux à sang, etc.
4. Quelles connexions sont appelées macroergiques ? Quelles fonctions les substances contenant des liaisons à haute énergie peuvent-elles remplir ?
Les liaisons macroergiques sont celles dont la rupture libère une grande quantité d'énergie (par exemple, la rupture de chaque liaison ATP macroergique s'accompagne de la libération de 40 kJ/mol d'énergie). Les substances contenant des liaisons à haute énergie peuvent servir de batteries, de supports et de fournisseurs d'énergie pour divers processus vitaux.
5. Formule générale ATP - C 10 H 16 N 5 O 13 P 3. Lorsqu’une mole d’ATP est hydrolysée en ADP, 40 kJ d’énergie sont libérées. Quelle quantité d'énergie sera libérée lors de l'hydrolyse de 1 kg d'ATP ?
● Calculez la masse molaire de l'ATP :
M (C 10 H 16 N 5 O 13 P 3) = 12 × 10 + 1 × 16 + 14 × 5 + 16 × 13 + 31 × 3 = 507 g/mol.
● Lorsque 507 g d'ATP (1 mole) sont hydrolysés, 40 kJ d'énergie sont libérés.
Cela signifie que lors de l'hydrolyse de 1 000 g d'ATP, les éléments suivants seront libérés : 1 000 g × 40 kJ : 507 g ≈ 78,9 kJ.
Réponse : Lorsque 1 kg d'ATP est hydrolysé en ADP, environ 78,9 kJ d'énergie seront libérés.
6. Des molécules d'ATP marquées au phosphore radioactif 32 R au niveau du dernier (troisième) résidu d'acide phosphorique ont été introduites dans une cellule, et des molécules d'ATP marquées au 32 R au niveau du premier résidu (le plus proche du ribose) ont été introduites dans l'autre cellule. Après 5 minutes, la teneur en ions phosphate inorganiques marqués au 32 R a été mesurée dans les deux cellules : où était-elle la plus élevée et pourquoi ?
Le dernier (troisième) résidu d'acide phosphorique est facilement clivé lors de l'hydrolyse de l'ATP, et le premier (le plus proche du ribose) n'est pas clivé même pendant l'hydrolyse en deux étapes de l'ATP en AMP. Par conséquent, la teneur en phosphate inorganique radioactif sera plus élevée dans la cellule dans laquelle l’ATP, marqué au dernier (troisième) résidu d’acide phosphorique, a été introduit.
Énergie activité musculaire
Comme déjà indiqué, les deux phases de l'activité musculaire - contraction et relaxation - se produisent avec l'utilisation obligatoire d'énergie, qui est libérée lors de l'hydrolyse de l'ATP.
Cependant, les réserves d'ATP dans les cellules musculaires sont insignifiantes (au repos, la concentration d'ATP dans les muscles est d'environ 5 mmol/l) et elles sont suffisantes pour le travail musculaire pendant 1 à 2 s. Par conséquent, pour garantir une activité musculaire plus longue, les réserves d’ATP doivent être reconstituées dans les muscles. La formation d'ATP dans les cellules musculaires directement pendant travail physique appelée resynthèse d’ATP et s’accompagne d’une consommation d’énergie.
Ainsi, lorsque les muscles fonctionnent, deux processus s'y déroulent simultanément : l'hydrolyse de l'ATP, qui fournit l'énergie nécessaire à la contraction et à la relaxation, et la régénération. Synthèse d'ATP, reconstituant la perte de cette substance. Si seule l’énergie chimique de l’ATP est utilisée pour assurer la contraction et la relaxation musculaire, alors l’énergie chimique d’une grande variété de composés est adaptée à la resynthèse de l’ATP : glucides, graisses, acides aminés et créatine phosphate.
Structure et rôle biologique de l'ATP
L'adénosine triphosphate (ATP) est un nucléotide. La molécule d'ATP (acide adénosine triphosphorique) est constituée de la base azotée adénine, du sucre ribose à cinq carbones et de trois résidus d'acide phosphorique reliés par une liaison à haute énergie. Lorsqu’il est hydrolysé, une grande quantité d’énergie est libérée. L'ATP est le principal macroerg de la cellule, un accumulateur d'énergie sous forme d'énergie de liaisons chimiques à haute énergie.
Dans des conditions physiologiques, c'est-à-dire dans les conditions qui existent dans une cellule vivante, la dégradation d'une mole d'ATP (506 g) s'accompagne de la libération de 12 kcal, soit 50 kJ d'énergie.
Voies de formation d’ATP
Oxydation aérobie (respiration tissulaire)
Synonymes : phosphorylation oxydative, phosphorylation respiratoire, phosphorylation aérobie.
Cette voie se produit dans les mitochondries.
Faire du vélo acides tricarboxyliques a été découvert pour la première fois par le biochimiste anglais G. Krebs (Fig. 4).
La première réaction est catalysée par l'enzyme citrate synthase, dans laquelle le groupe acétyle de l'acétyl-CoA se condense avec l'oxaloacétate, entraînant la formation d'acide citrique. Apparemment, dans cette réaction, le citril-CoA lié à l’enzyme se forme comme produit intermédiaire. Puis ce dernier s’hydrolyse spontanément et de manière irréversible pour former du citrate et du HS-CoA.
À la suite de la deuxième réaction, l'acide citrique obtenu subit une déshydratation pour former de l'acide cis-aconitique qui, en ajoutant une molécule d'eau, devient de l'acide isocitrique (isocitrate). Ces réactions réversibles d'hydratation-déshydratation sont catalysées par l'enzyme aconitate hydratase (aconitase). En conséquence, un mouvement mutuel de H et OH se produit dans la molécule de citrate.
Riz. 4. Cycle de l'acide tricarboxylique (cycle de Krebs)
La troisième réaction semble limiter la vitesse du cycle de Krebs. L'acide isocitrique est déshydrogéné en présence d'isocitrate déshydrogénase dépendante du NAD. Au cours de la réaction isocitrate déshydrogénase, l’acide isocitrique est simultanément décarboxylé. L'isocitrate déshydrogénase dépendante du NAD est une enzyme allostérique qui nécessite l'ADP comme activateur spécifique. De plus, l’enzyme a besoin d’ions pour présenter son activité.
Au cours de la quatrième réaction, une décarboxylation oxydative de l’acide α-cétoglutarique se produit pour former le composé à haute énergie succinyl-CoA. Le mécanisme de cette réaction est similaire à la réaction de décarboxylation oxydative du pyruvate en acétyl-CoA ; Le complexe α-cétoglutarate déshydrogénase a une structure similaire à celle du complexe pyruvate déshydrogénase. Dans les deux cas, 5 coenzymes participent à la réaction : TPP, amide d'acide lipoïque, HS-CoA, FAD et NAD+.
La cinquième réaction est catalysée par l'enzyme succinyl-CoA synthétase. Au cours de cette réaction, le succinyl-CoA, avec la participation du GTP et du phosphate inorganique, est transformé en acide succinique (succinate). Dans le même temps, la formation d'une liaison phosphate à haute énergie du GTP se produit en raison de la liaison thioéther à haute énergie du succinyl-CoA.
À la suite de la sixième réaction, le succinate est déshydrogéné en acide fumarique. L'oxydation du succinate est catalysée par la succinate déshydrogénase.
dans une molécule dans laquelle le coenzyme FAD est étroitement lié (de manière covalente) à la protéine. À son tour, la succinate déshydrogénase est étroitement liée à la membrane mitochondriale interne.
La septième réaction est réalisée sous l'influence de l'enzyme fumarate hydratase (fumarase). L'acide fumarique obtenu est hydraté, le produit de la réaction est l'acide malique (malate).
Enfin, lors de la huitième réaction du cycle de l'acide tricarboxylique, sous l'influence de la malate déshydrogénase mitochondriale NAD-dépendante, le L-malate est oxydé en oxaloacétate.
Au cours d'un tour de cycle, l'oxydation d'une molécule d'acétyl-CoA dans le cycle de Krebs et le système de phosphorylation oxydative peuvent produire 12 molécules d'ATP.
Oxydation anaérobie
Synonymes : phosphorylation du substrat, synthèse anaérobie d'ATP. En passant dans le cytoplasme, l'hydrogène séparé rejoint une autre substance. Selon le substrat, on distingue deux voies de resynthèse anaérobie de l'ATP : la créatine phosphate (créatine kinase, alactique) et glycolytique (glycolyse, lactate). Dans le cas nerveux, le substrat est la créatine phosphate, dans le second cas, le glucose.
Ces voies se produisent sans la participation de l'oxygène.
Dans n'importe quelle cellule de notre corps, des millions de substances biologiques circulent réactions chimiques. Ils sont catalysés par diverses enzymes, qui nécessitent souvent de l’énergie. Où la cellule l'obtient-elle ? On peut répondre à cette question si l'on considère la structure de la molécule d'ATP - l'une des principales sources d'énergie.
L'ATP est une source d'énergie universelle
ATP signifie adénosine triphosphate, ou adénosine triphosphate. La substance est l’une des deux sources d’énergie les plus importantes de toute cellule. La structure de l'ATP et son rôle biologique sont étroitement liés. La plupart des réactions biochimiques ne peuvent se produire qu'avec la participation de molécules d'une substance, cela est particulièrement vrai. Cependant, l'ATP est rarement directement impliquée dans la réaction : pour qu'un processus se produise, l'énergie contenue précisément dans l'adénosine triphosphate est nécessaire.
La structure des molécules de la substance est telle que les liaisons formées entre les groupes phosphate portent grande quantitéénergie. Par conséquent, de telles liaisons sont également appelées macroergiques ou macroénergétiques (macro = plusieurs, grande quantité). Le terme a été introduit pour la première fois par le scientifique F. Lipman, qui a également proposé d'utiliser le symbole ̴ pour les désigner.
Il est très important que la cellule maintienne un niveau constant d’adénosine triphosphate. Cela est particulièrement vrai pour les cellules des tissus musculaires et les fibres nerveuses, car elles sont les plus dépendantes de l'énergie et nécessitent une teneur élevée en adénosine triphosphate pour remplir leurs fonctions.
La structure de la molécule d'ATP
L'adénosine triphosphate est composée de trois éléments : le ribose, l'adénine et les résidus

Ribose- un glucide appartenant au groupe des pentoses. Cela signifie que le ribose contient 5 atomes de carbone, qui sont enfermés dans un cycle. Le ribose se connecte à l'adénine via une liaison β-N-glycosidique sur le 1er atome de carbone. Des résidus d'acide phosphorique sur le 5ème atome de carbone sont également ajoutés au pentose.
L'adénine est une base azotée. Selon la base azotée attachée au ribose, on distingue également le GTP (guanosine triphosphate), le TTP (thymidine triphosphate), le CTP (cytidine triphosphate) et l'UTP (uridine triphosphate). Toutes ces substances ont une structure similaire à celle de l'adénosine triphosphate et remplissent à peu près les mêmes fonctions, mais elles sont beaucoup moins courantes dans la cellule.
Résidus d'acide phosphorique. Un maximum de trois résidus d'acide phosphorique peuvent être attachés au ribose. S'il y en a deux ou un seul, alors la substance est appelée ADP (diphosphate) ou AMP (monophosphate). C'est entre les résidus de phosphore que se concluent des liaisons macroénergétiques, après la rupture desquelles 40 à 60 kJ d'énergie sont libérées. Si deux liaisons sont rompues, 80, moins souvent, 120 kJ d'énergie sont libérées. Lorsque la liaison entre le ribose et le résidu phosphore est rompue, seulement 13,8 kJ sont libérés, il n'y a donc que deux liaisons à haute énergie dans la molécule de triphosphate (P ̴ P ̴ P), et dans la molécule d'ADP il y en a une (P ̴ P).
Ce sont les caractéristiques structurelles de l’ATP. Du fait qu'une liaison macroénergétique se forme entre les résidus d'acide phosphorique, la structure et les fonctions de l'ATP sont interconnectées.
La structure de l'ATP et le rôle biologique de la molécule. Fonctions supplémentaires de l'adénosine triphosphate
En plus de l’énergie, l’ATP peut remplir de nombreuses autres fonctions dans la cellule. Avec d'autres nucléotides triphosphates, le triphosphate est impliqué dans la construction des acides nucléiques. Dans ce cas, ATP, GTP, TTP, CTP et UTP sont des fournisseurs de bases azotées. Cette propriété est utilisée dans les processus et la transcription.
L'ATP est également nécessaire au fonctionnement des canaux ioniques. Par exemple, le canal Na-K pompe 3 molécules de sodium hors de la cellule et pompe 2 molécules de potassium dans la cellule. Ce courant ionique est nécessaire pour maintenir une charge positive sur la surface externe de la membrane, et ce n'est qu'avec l'aide de l'adénosine triphosphate que le canal peut fonctionner. Il en va de même pour les canaux protoniques et calciques.
L'ATP est le précurseur du deuxième messager AMPc (adénosine monophosphate cyclique) - l'AMPc transmet non seulement le signal reçu par les récepteurs membranaires cellulaires, mais est également un effecteur allostérique. Les effecteurs allostériques sont des substances qui accélèrent ou ralentissent les réactions enzymatiques. Ainsi, l'adénosine triphosphate cyclique inhibe la synthèse d'une enzyme qui catalyse la dégradation du lactose dans les cellules bactériennes.
La molécule d’adénosine triphosphate elle-même peut également être un effecteur allostérique. De plus, dans de tels processus, l'ADP agit comme un antagoniste de l'ATP : si le triphosphate accélère la réaction, alors le diphosphate l'inhibe, et vice versa. Ce sont les fonctions et la structure de l’ATP.

Comment se forme l’ATP dans une cellule ?
Les fonctions et la structure de l'ATP sont telles que les molécules de la substance sont rapidement utilisées et détruites. La synthèse des triphosphates est donc un processus important dans la formation d’énergie dans la cellule.
Il existe trois méthodes les plus importantes pour la synthèse de l'adénosine triphosphate :
1. Phosphorylation du substrat.
2. Phosphorylation oxydative.
3. Photophosphorylation.
La phosphorylation du substrat est basée sur de multiples réactions se produisant dans le cytoplasme cellulaire. Ces réactions sont appelées glycolyse - étape anaérobie. À la suite d'un cycle de glycolyse, à partir d'une molécule de glucose, deux molécules sont synthétisées, qui sont ensuite utilisées pour produire de l'énergie, et deux ATP sont également synthétisées.
- C 6 H 12 O 6 + 2ADP + 2Pn --> 2C 3 H 4 O 3 + 2ATP + 4H.
Respiration cellulaire
La phosphorylation oxydative est la formation d'adénosine triphosphate par transfert d'électrons le long de la chaîne de transport d'électrons membranaire. À la suite de ce transfert, un gradient de protons se forme sur un côté de la membrane et, à l’aide de l’ensemble intégral protéique de l’ATP synthase, des molécules sont construites. Le processus se déroule sur la membrane mitochondriale.

La séquence d'étapes de glycolyse et de phosphorylation oxydative dans les mitochondries constitue un processus commun appelé respiration. Après cycle completÀ partir d'une molécule de glucose dans une cellule, 36 molécules d'ATP sont formées.
Photophosphorylation
Le processus de photophosphorylation est le même que la phosphorylation oxydative avec une seule différence : des réactions de photophosphorylation se produisent dans les chloroplastes de la cellule sous l'influence de la lumière. L'ATP est produite au cours de la phase lumineuse de la photosynthèse, le principal processus de production d'énergie des plantes vertes, des algues et de certaines bactéries.
Lors de la photosynthèse, les électrons traversent la même chaîne de transport d’électrons, entraînant la formation d’un gradient de protons. La concentration de protons d’un côté de la membrane est à l’origine de la synthèse de l’ATP. L'assemblage des molécules est réalisé par l'enzyme ATP synthase.

La cellule moyenne contient 0,04 % d'adénosine triphosphate en poids. Cependant, le plus grande importance observé dans les cellules musculaires : 0,2-0,5 %.
Il y a environ 1 milliard de molécules d'ATP dans une cellule.
Chaque molécule ne vit pas plus d'une minute.
Une molécule d'adénosine triphosphate est renouvelée 2 000 à 3 000 fois par jour.
Au total, le corps humain synthétise 40 kg d'adénosine triphosphate par jour et la réserve d'ATP est à tout moment de 250 g.

Conclusion
La structure de l’ATP et le rôle biologique de ses molécules sont étroitement liés. La substance joue un rôle clé dans les processus vitaux, car les liaisons à haute énergie entre les résidus de phosphate contiennent une énorme quantité d'énergie. L'adénosine triphosphate a de nombreuses fonctions dans la cellule et il est donc important de la maintenir concentration constante substances. La décomposition et la synthèse se produisent à grande vitesse, car l'énergie des liaisons est constamment utilisée dans les réactions biochimiques. C'est une substance essentielle pour toute cellule du corps. C’est probablement tout ce que l’on peut dire sur la structure de l’ATP.
Envoyer votre bon travail dans la base de connaissances est simple. Utilisez le formulaire ci-dessous
Les étudiants, étudiants diplômés, jeunes scientifiques qui utilisent la base de connaissances dans leurs études et leur travail vous seront très reconnaissants.
Posté sur http://www.allbest.ru/
- Introduction
- 1.1 Propriétés chimiques de l'ATP
- 1.2 Propriétés physiques ATP
- 2.1
- 3.1 Rôle dans la cellule
- 3.2 Rôle dans la fonction enzymatique
- 3.4 Autres fonctions de l'ATP
- Conclusion
- Bibliographie
Liste des symboles
ATP - adénosine triphosphate
ADP - adénosine diphosphate
AMP - adénosine monophosphate
ARN - acide ribonucléique
ADN - acide désoxyribonucléique
NAD - nicotinamide adénine dinucléotide
PVC - acide pyruvique
G-6-P - phosphoglucose isomérase
F-6-F - fructose-6-phosphate
TPP - pyrophosphate de thiamine
FAD - phényladénine dinucléotide
Fn - phosphate illimité
G - entropie
RNR - ribonucléotide réductase
Introduction
La principale source d'énergie pour tous les êtres vivants habitant notre planète est l'énergie du soleil, qui est utilisée directement uniquement par les cellules des plantes vertes, les algues, les bactéries vertes et violettes. Dans ces cellules de gaz carbonique et de l'eau lors de la photosynthèse, des substances organiques se forment (glucides, graisses, protéines, acides nucléiques, etc.). En mangeant des plantes, les animaux obtiennent des substances organiques sous forme finie. L'énergie stockée dans ces substances passe avec elles dans les cellules des organismes hétérotrophes.
Dans les cellules des organismes animaux, l'énergie des composés organiques lors de leur oxydation est convertie en énergie ATP. (Le dioxyde de carbone et l'eau libérés dans ce cas sont à nouveau utilisés par les organismes autotrophes pour les processus de photosynthèse.) Tous les processus vitaux sont réalisés en utilisant l'énergie de l'ATP : biosynthèse de composés organiques, mouvement, croissance, division cellulaire, etc.
Le sujet de la formation et de l'utilisation de l'ATP dans le corps n'est pas nouveau depuis longtemps, mais il est rare que vous trouviez une discussion complète des deux dans une seule source et encore moins souvent une analyse de ces deux processus à la fois et dans différents organismes.
À cet égard, la pertinence de nos travaux est devenue une étude approfondie de la formation et de l'utilisation de l'ATP dans les organismes vivants, car ce sujet n’est pas étudié au niveau approprié dans la littérature scientifique populaire.
Le but de notre travail était :
· étude des mécanismes de formation et des modes d'utilisation de l'ATP dans l'organisme des animaux et des humains.
Les tâches suivantes nous ont été confiées :
· Étudier la nature chimique et les propriétés de l'ATP ;
· Analyser les voies de formation de l'ATP dans les organismes vivants ;
· Envisager des façons d'utiliser l'ATP dans les organismes vivants ;
· Considérer Valeur ATP pour le corps humain et animal.
Chapitre 1. Nature chimique et propriétés de l'ATP
1.1 Propriétés chimiques de l'ATP
L'adénosine triphosphate est un nucléotide qui joue un rôle extrêmement important dans le métabolisme de l'énergie et des substances dans les organismes ; Tout d’abord, le composé est connu comme une source d’énergie universelle pour tous. processus biochimiques, se produisant dans les systèmes vivants. L'ATP a été découverte en 1929 par Karl Lohmann et en 1941, Fritz Lipmann a montré que l'ATP est le principal vecteur d'énergie dans la cellule.
Nom systématique de l'ATP :
9-en-D-ribofuranosyladénine-5"-triphosphate, ou
9-en-D-ribofuranosyl-6-amino-purine-5"-triphosphate.
Chimiquement, l'ATP est l'ester triphosphate de l'adénosine, qui est un dérivé de l'adénine et du ribose.
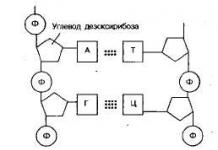
La base azotée purique - l'adénine - est reliée par une liaison β-N-glycosidique au carbone 1" du ribose. Trois molécules d'acide phosphorique sont séquentiellement attachées au carbone 5" du ribose, désignées respectivement par les lettres : b, c et d.
La structure de l'ATP est similaire à celle du nucléotide adénine qui fait partie de l'ARN, sauf qu'au lieu d'un acide phosphorique, l'ATP contient trois résidus d'acide phosphorique. Les cellules ne sont pas capables de contenir des acides en quantités notables, mais seulement leurs sels. Par conséquent, l'acide phosphorique entre dans l'ATP sous forme de résidu (au lieu du groupe OH de l'acide, il y a un atome d'oxygène chargé négativement).
Sous l'action d'enzymes, la molécule d'ATP subit facilement une hydrolyse, c'est-à-dire qu'elle se fixe sur une molécule d'eau et se décompose pour former de l'acide adénosine diphosphorique (ADP) :
ATP + H2O ADP + H3PO4.
L'élimination d'un autre résidu d'acide phosphorique convertit l'ADP en acide adénosine monophosphorique AMP :
ADP + H2O AMP + H3PO4.
Ces réactions sont réversibles, c'est-à-dire que l'AMP peut se transformer en ADP puis en ATP, accumulant ainsi de l'énergie. La rupture d'une liaison peptidique régulière ne libère que 12 kJ/mol d'énergie. Et les liaisons qui attachent les résidus d'acide phosphorique sont de haute énergie (on les appelle aussi haute énergie) : la destruction de chacune d'entre elles libère 40 kJ/mol d'énergie. L’ATP joue donc un rôle central dans les cellules en tant qu’accumulateur d’énergie biologique universel. Les molécules d'ATP sont synthétisées dans les mitochondries et les chloroplastes (seule une petite quantité est synthétisée dans le cytoplasme), puis pénètrent dans divers organites de la cellule, fournissant de l'énergie pour tous les processus vitaux.
En raison de l'énergie de l'ATP, la division cellulaire se produit, le transfert actif de substances à travers les membranes cellulaires et le maintien du potentiel électrique membranaire pendant le processus de transfert. influx nerveux, ainsi que la biosynthèse de composés de haut poids moléculaire et le travail physique.
Avec une charge accrue (par exemple, lors de la course à pied sur de courtes distances), les muscles travaillent exclusivement grâce à l'apport d'ATP. Dans les cellules musculaires, cette réserve est suffisante pour plusieurs dizaines de contractions, puis la quantité d'ATP doit être reconstituée. La synthèse de l'ATP à partir de l'ADP et de l'AMP est due à l'énergie libérée lors de la dégradation des glucides, des lipides et d'autres substances. Effectuer un travail mental nécessite également une grande quantité d’ATP. Pour cette raison, les personnes souffrant de travail mental ont besoin d'une quantité accrue de glucose, dont la dégradation assure la synthèse de l'ATP.
1.2 Propriétés physiques de l'ATP
L'ATP est constitué d'adénosine et de ribose, ainsi que de trois groupes phosphate. L'ATP est hautement soluble dans l'eau et assez stable dans les solutions à pH 6,8-7,4, mais est rapidement hydrolysé à pH extrême. Par conséquent, l’ATP est mieux stocké dans des sels anhydres.
L'ATP est une molécule instable. Dans l'eau non tamponnée, il s'hydrolyse en ADP et en phosphate. En effet, la force des liaisons entre les groupes phosphate de l’ATP est inférieure à la force des liaisons hydrogène (liaisons d’hydratation) entre ses produits (ADP + phosphate) et l’eau. Ainsi, si l’ATP et l’ADP sont en équilibre chimique dans l’eau, la quasi-totalité de l’ATP finira par être convertie en ADP. Un système loin de l’équilibre contient de l’énergie libre de Gibbs et est capable d’effectuer un travail. Les cellules vivantes maintiennent le rapport ATP/ADP à un point dix ordres de grandeur par rapport à l'équilibre, avec une concentration en ATP mille fois supérieure à la concentration en ADP. Ce déplacement de la position d’équilibre signifie que l’hydrolyse de l’ATP dans la cellule libère une grande quantité d’énergie libre.
Les deux liaisons phosphate de haute énergie (celles qui relient les phosphates adjacents) dans une molécule d'ATP sont responsables de la teneur élevée en énergie de cette molécule. L'énergie stockée dans l'ATP peut être libérée par hydrolyse. Situé en aval du sucre ribose, le groupe g-phosphate a une énergie d'hydrolyse plus élevée que le b- ou le b-phosphate. Les liaisons formées après l'hydrolyse ou la phosphorylation d'un résidu ATP ont une énergie inférieure à celle des autres liaisons ATP. Au cours de l’hydrolyse ou de la phosphorylation de l’ATP catalysée par des enzymes, l’énergie libre disponible peut être utilisée par les systèmes vivants pour effectuer leur travail.
Tout système instable de molécules potentiellement réactives peut potentiellement servir de moyen de stocker de l'énergie libre si les cellules ont maintenu leur concentration loin du point d'équilibre de la réaction. Cependant, comme pour la plupart des biomolécules polymères, la décomposition de l'ARN, de l'ADN et de l'ATP en monomères simples implique à la fois une libération d'énergie et d'entropie, ce qui augmente les considérations à la fois à la concentration standard et à celles trouvées dans la cellule.
La quantité standard d'énergie libérée à la suite de l'hydrolyse de l'ATP peut être calculée à partir de changements d'énergie non associés aux conditions naturelles (standard), puis en corrigeant la concentration biologique. La variation nette de l'énergie thermique (enthalpie) à température et pression standard pour la décomposition de l'ATP en ADP et phosphates inorganiques est de 20,5 kJ/mol, avec une variation d'énergie libre de 3,4 kJ/mol. L'énergie libérée par la dégradation du phosphate ou du pyrophosphate de l'ATP jusqu'à la norme d'État 1 M est :
ATP + H 2 O > ADP + P i DG ? = - 30,5 kJ/mol (-7,3 kcal/mol)
ATP + H 2 O > AMP + PP je DG ? = - 45,6 kJ/mol (-10,9 kcal/mol)
Ces valeurs peuvent être utilisées pour calculer les changements d’énergie dans des conditions physiologiques et ATP/ADP cellulaire. Cependant, une signification plus représentative appelée charge énergétique fonctionne plus souvent. Les valeurs sont données pour l'énergie libre de Gibbs. Ces réactions dépendent d'un certain nombre de facteurs, notamment la force ionique totale et la présence de métaux alcalino-terreux tels que les ions Mg 2+ et Ca 2+. Dans des conditions normales, la DG est d'environ -57 kJ/mol (-14 kcal/mol).
énergie de la batterie biologique aux protéines
Chapitre 2. Voies de formation de l'ATP
Dans l’organisme, l’ATP est synthétisée par phosphorylation de l’ADP :
ADP + H 3 PO 4 + énergie> ATP + H2O.
La phosphorylation de l'ADP est possible de deux manières : la phosphorylation du substrat et la phosphorylation oxydative (en utilisant l'énergie des substances oxydantes). La majeure partie de l'ATP se forme sur les membranes mitochondriales lors de la phosphorylation oxydative par l'ATP synthase H-dépendante. La phosphorylation du substrat de l'ATP ne nécessite pas la participation d'enzymes membranaires, elle se produit lors de la glycolyse ou par transfert d'un groupe phosphate à partir d'autres composés à haute énergie.
Les réactions de phosphorylation de l'ADP et l'utilisation ultérieure de l'ATP comme source d'énergie forment un processus cyclique qui constitue l'essence du métabolisme énergétique.
Dans l’organisme, l’ATP est l’une des substances les plus fréquemment renouvelées. Ainsi, chez l’homme, la durée de vie d’une molécule d’ATP est inférieure à 1 minute. Au cours de la journée, une molécule d'ATP subit en moyenne 2 000 à 3 000 cycles de resynthèse ( corps humain synthétise environ 40 kg d'ATP par jour), c'est-à-dire que pratiquement aucune réserve d'ATP n'est créée dans le corps et que pour une vie normale, il est nécessaire de synthétiser constamment de nouvelles molécules d'ATP.
La phosphorylation oxydative -
Cependant, les glucides sont le plus souvent utilisés comme substrat. Ainsi, les cellules cérébrales ne sont pas capables d’utiliser d’autres substrats pour se nourrir que les glucides.
Les glucides précomplexes sont décomposés en glucides simples, conduisant à la formation de glucose. Le glucose est un substrat universel dans le processus de respiration cellulaire. L'oxydation du glucose se divise en 3 étapes :
1. glycolyse ;
2. décarboxylation oxydative et cycle de Krebs ;
3. phosphorylation oxydative.
Dans ce cas, la glycolyse est une phase courante pour les respiration anaérobie.
2 .1.1 GLicoLiz- un processus enzymatique de dégradation séquentielle du glucose dans les cellules, accompagné de la synthèse d'ATP. La glycolyse en conditions aérobies conduit à la formation d'acide pyruvique (pyruvate), la glycolyse en conditions anaérobies conduit à la formation d'acide lactique (lactate). La glycolyse est la principale voie de catabolisme du glucose chez les animaux.
La voie glycolytique comprend 10 réactions séquentielles, chacune étant catalysée par une enzyme distincte.
Le processus de glycolyse peut être divisé en deux étapes. La première étape, qui se produit avec la consommation d'énergie de 2 molécules d'ATP, consiste en la division d'une molécule de glucose en 2 molécules de glycéraldéhyde-3-phosphate. Au deuxième stade, une oxydation du glycéraldéhyde-3-phosphate dépendante du NAD se produit, accompagnée de la synthèse d'ATP. La glycolyse elle-même est un processus complètement anaérobie, c'est-à-dire qu'elle ne nécessite pas la présence d'oxygène pour que les réactions se produisent.
La glycolyse est l’un des processus métaboliques les plus anciens, connu dans presque tous les organismes vivants. Vraisemblablement, la glycolyse est apparue il y a plus de 3,5 milliards d’années chez les procaryotes primordiaux.
Le résultat de la glycolyse est la conversion d'une molécule de glucose en deux molécules d'acide pyruvique (PVA) et la formation de deux équivalents réducteurs sous forme de coenzyme NADH.
L’équation complète de la glycolyse est la suivante :
C 6 H 12 O 6 + 2NAD + + 2ADP + 2P n = 2NAD H + 2PVK + 2ATP + 2H 2 O + 2H +.
En l'absence ou en carence d'oxygène dans la cellule, l'acide pyruvique subit une réduction en acide lactique, alors l'équation générale de la glycolyse sera la suivante :
C 6 H 12 O 6 + 2ADP + 2P n = 2 lactate + 2ATP + 2H 2 O.
Ainsi, lors de la dégradation anaérobie d'une molécule de glucose, le rendement net total en ATP est de deux molécules obtenues dans des réactions de phosphorylation du substrat de l'ADP.
Dans les organismes aérobies, les produits finaux de la glycolyse subissent d'autres transformations dans les cycles biochimiques liés à la respiration cellulaire. En conséquence, après l'oxydation complète de tous les métabolites d'une molécule de glucose au dernier stade de la respiration cellulaire - la phosphorylation oxydative, qui se produit sur les mitochondries. chaîne respiratoire en présence d'oxygène, 34 ou 36 molécules d'ATP supplémentaires sont synthétisées pour chaque molécule de glucose.
La première réaction de glycolyse est la phosphorylation d'une molécule de glucose, qui se produit avec la participation de l'enzyme hexokinase spécifique aux tissus avec la dépense énergétique d'1 molécule d'ATP ; une forme active de glucose se forme - glucose-6-phosphate (G-6-F):
Pour que la réaction se produise, la présence d'ions Mg 2+ dans le milieu est nécessaire, avec lesquels la molécule d'ATP est liée de manière complexe. Cette réaction est irréversible et constitue la première clé réaction glycolyse.
La phosphorylation du glucose a deux objectifs : d'une part, du fait que la membrane plasmique, perméable à la molécule de glucose neutre, ne laisse pas passer les molécules de G-6-P chargées négativement, le glucose phosphorylé est enfermé à l'intérieur de la cellule. Deuxièmement, lors de la phosphorylation, le glucose est converti en forme active, capable de participer à des réactions biochimiques et d'être inclus dans les cycles métaboliques.
L'isoenzyme hépatique de l'hexokinase, la glucokinase, joue un rôle important dans la régulation de la glycémie.
Dans la réaction suivante ( 2 ) par l'enzyme phosphoglucoisomérase G-6-P est converti en fructose-6-phosphate (F-6-F):
Aucune énergie n'est nécessaire pour cette réaction et la réaction est complètement réversible. Sur à ce stade le fructose peut également être impliqué dans le processus de glycolyse par phosphorylation.
Ensuite, deux réactions se succèdent presque immédiatement : la phosphorylation irréversible du fructose-6-phosphate ( 3 ) et clivage aldolique réversible du résultat fructose-1,6-biphosphate (F-1.6-bF) en deux trioses ( 4 ).
La phosphorylation du P-6-P est réalisée par la phosphofructokinase avec dépense d'énergie d'une autre molécule d'ATP ; c'est la deuxième clé réaction glycolyse, sa régulation détermine l'intensité de la glycolyse dans son ensemble.
Clivage aldol F-1.6-bF se produit sous l'action de la fructose-1,6-bisphosphate aldolase :
À la suite de la quatrième réaction, phosphate de dihydroxyacétone Et glycéraldéhyde-3-phosphate, et le premier est presque immédiatement sous l'influence phosphotriose isomérase va au deuxième ( 5 ), qui participe à d'autres transformations :
Chaque molécule de glycéraldéhyde phosphate est oxydée par NAD+ en présence de déshydrogénases glycéraldéhyde phosphate avant 1,3- detphosphoglyce- taux (6 ):
Ensuite avec 1,3-diphosphoglycérate contenant une liaison à haute énergie en position 1, l'enzyme phosphoglycérate kinase transfère un résidu d'acide phosphorique à la molécule d'ADP (réaction 7 ) - une molécule d'ATP se forme :
Il s'agit de la première réaction de phosphorylation du substrat. A partir de ce moment, le processus de dégradation du glucose cesse d'être non rentable en termes d'énergie, puisque les coûts énergétiques de la première étape sont compensés : 2 molécules d'ATP sont synthétisées (une pour chaque 1,3-diphosphoglycérate) au lieu des deux dépensées en les réactions 1 Et 3 . Pour que cette réaction se produise, la présence d'ADP dans le cytosol est nécessaire, c'est-à-dire que lorsqu'il y a un excès d'ATP dans la cellule (et un manque d'ADP), sa vitesse diminue. Puisque l’ATP, qui n’est pas métabolisé, n’est pas déposé dans la cellule mais est simplement détruit, cette réaction est un régulateur important de la glycolyse.
Puis séquentiellement : la phosphoglycérol mutase se forme 2-phospho- glycérate (8 ):
Formes d'énolase phosphoénolpyruvate (9 ):
Enfin, la deuxième réaction de phosphorylation du substrat de l'ADP se produit avec la formation de la forme énol du pyruvate et de l'ATP ( 10 ):
La réaction se produit sous l'action de la pyruvate kinase. C'est la dernière réaction clé de la glycolyse. L'isomérisation de la forme énol du pyruvate en pyruvate se produit de manière non enzymatique.
Depuis sa formation F-1.6-bF Seules les réactions qui libèrent de l'énergie se produisent 7 Et 10 , dans lequel le substrat se trouve Phosphorylation de l'ADP.
Régulation glycolyse
Il existe des réglementations locales et générales.
La régulation locale s'effectue en modifiant l'activité des enzymes sous l'influence de divers métabolites à l'intérieur de la cellule.
La régulation de la glycolyse dans son ensemble, immédiatement pour tout l'organisme, se produit sous l'influence d'hormones qui, en influençant les molécules de messagers secondaires, modifient le métabolisme intracellulaire.
L'insuline joue un rôle important dans la stimulation de la glycolyse. Le glucagon et l'adrénaline sont les inhibiteurs hormonaux les plus importants de la glycolyse.
L'insuline stimule la glycolyse par :
· activation de la réaction hexokinase ;
· stimulation de la phosphofructokinase ;
· stimulation de la pyruvate kinase.
D'autres hormones influencent également la glycolyse. Par exemple, la somatotropine inhibe les enzymes glycolytiques et les hormones thyroïdiennes sont des stimulants.
La glycolyse est régulée en plusieurs étapes clés. Réactions catalysées par l'hexokinase ( 1 ), la phosphofructokinase ( 3 ) et la pyruvate kinase ( 10 ) se caractérisent par une diminution significative de l'énergie libre et sont pratiquement irréversibles, ce qui leur permet d'être des points de régulation efficaces de la glycolyse.
La glycolyse est une voie catabolique d'une importance exceptionnelle. Il fournit de l’énergie pour les réactions cellulaires, notamment la synthèse des protéines. Les produits intermédiaires de la glycolyse sont utilisés dans la synthèse des graisses. Le pyruvate peut également être utilisé pour synthétiser l'alanine, l'aspartate et d'autres composés. Grâce à la glycolyse, les performances mitochondriales et la disponibilité en oxygène ne limitent pas la puissance musculaire lors de charges extrêmes à court terme.
2.1.2 Décarboxylation oxydative - l'oxydation du pyruvate en acétyl-CoA se produit avec la participation d'un certain nombre d'enzymes et de coenzymes, structurellement unies en un système multienzymatique appelé complexe pyruvate déshydrogénase.
Au stade I de ce processus, le pyruvate perd son groupe carboxyle à la suite d'une interaction avec le pyrophosphate de thiamine (TPP) dans le centre actif de l'enzyme pyruvate déshydrogénase (E 1). Au stade II, le groupe oxyéthyle du complexe E 1 -TPP-CHOH-CH 3 est oxydé pour former un groupe acétyle, qui est simultanément transféré en amide d'acide lipoïque (coenzyme) associé à l'enzyme dihydrolipoylacétyltransférase (E 2). Cette enzyme catalyse l'étape III - le transfert du groupe acétyle en coenzyme CoA (HS-KoA) avec la formation du produit final acétyl-CoA, qui est un composé à haute énergie (macroergique).
Au stade IV, la forme oxydée du lipoamide est régénérée à partir du complexe dihydrolipoamide-E 2 réduit. Avec la participation de l'enzyme dihydrolipoyl déshydrogénase (E 3), l'hydrogène est transféré des groupes sulfhydryle réduits du dihydrolipoamide au FAD, qui agit comme un groupe prothétique de cette enzyme et y est étroitement lié. Au stade V, la dihydro-lipoyl déshydrogénase FADH 2 réduite transfère l'hydrogène au coenzyme NAD pour former NADH + H +.
Le processus de décarboxylation oxydative du pyruvate se produit dans la matrice mitochondriale. Il implique (dans le cadre d'un complexe multienzymatique complexe) 3 enzymes (pyruvate déshydrogénase, dihydrolipoyl acétyltransférase, dihydrolipoyl déshydrogénase) et 5 coenzymes (TPF, amide d'acide lipoïque, coenzyme A, FAD et NAD), dont trois sont relativement fermement associées aux enzymes. (TPF-E 1, lipoamide-E 2 et FAD-E 3), et deux sont facilement dissociés (HS-KoA et NAD).
Riz. 1 Mécanisme d'action du complexe pyruvate déshydrogénase
E 1 - pyruvate déshydrogénase; E 2 - dihydrolipoylacétyltransférase; E 3 - dihydrolipoyl déshydrogénase; Les chiffres dans les cercles indiquent les étapes du processus.
Toutes ces enzymes, qui ont une structure sous-unitaire, et les coenzymes sont organisées en un seul complexe. Par conséquent, les produits intermédiaires sont capables d’interagir rapidement les uns avec les autres. Il a été démontré que les chaînes polypeptidiques des sous-unités de la dihydrolipoyl acétyltransférase qui composent le complexe constituent le noyau du complexe, autour duquel se situent la pyruvate déshydrogénase et la dihydrolipoyl déshydrogénase. Il est généralement admis que le complexe enzymatique natif est formé par auto-assemblage.
La réaction globale catalysée par le complexe pyruvate déshydrogénase peut être représentée comme suit :
Pyruvate + NAD + + HS-CoA -> Acétyl-CoA + NADH + H + + CO 2.
La réaction s'accompagne d'une diminution significative de l'énergie libre standard et est pratiquement irréversible.
L'acétyl-CoA formé lors de la décarboxylation oxydative subit une oxydation supplémentaire avec formation de CO 2 et de H 2 O. L'oxydation complète de l'acétyl-CoA se produit dans le cycle de l'acide tricarboxylique (cycle de Krebs). Ce processus, ainsi que la décarboxylation oxydative du pyruvate, se produisent dans les mitochondries des cellules.
2 .1.3 Faire du vélotricarboniqueaigreT (faire du vélo Crébsa, cithareépais faire du vélo) - partie centrale la voie générale du catabolisme, un processus aérobie biochimique cyclique au cours duquel la conversion des composés à deux et trois carbones formés comme produits intermédiaires dans les organismes vivants lors de la dégradation des glucides, des graisses et des protéines se produit en CO 2. Dans ce cas, l'hydrogène libéré est envoyé à la chaîne respiratoire des tissus, où il est ensuite oxydé en eau, participant directement à la synthèse de la source d'énergie universelle - l'ATP.
Le cycle de Krebs est une étape clé dans la respiration de toutes les cellules utilisatrices d’oxygène, à l’intersection de nombreuses voies métaboliques dans le corps. En plus du rôle énergétique important, le cycle a également une fonction plastique importante, c'est-à-dire qu'il est une source importante de molécules précurseurs, à partir desquelles, au cours d'autres transformations biochimiques, sont synthétisés des composés importants pour la vie de la cellule, tels que acides aminés, glucides, acides gras, etc.
Cycle de transformation citronacides dans les cellules vivantes a été découvert et étudié par le biochimiste allemand Sir Hans Krebs, pour ce travail il (avec F. Lipman) a reçu prix Nobel(1953).
Chez les eucaryotes, toutes les réactions du cycle de Krebs se produisent à l'intérieur des mitochondries, et les enzymes qui les catalysent, sauf une, sont à l'état libre dans la matrice mitochondriale, à l'exception de la succinate déshydrogénase, qui est localisée sur la membrane mitochondriale interne, noyée dans la bicouche lipidique. Chez les procaryotes, les réactions du cycle se déroulent dans le cytoplasme.
L'équation générale pour un tour du cycle de Krebs est :
Acétyl-CoA > 2CO 2 + CoA + 8e ?
Régulation faire du véloUN:
Le cycle de Krebs est régulé « par un mécanisme de rétroaction négative » : en présence d'une grande quantité de substrats (acétyl-CoA, oxaloacétate), le cycle fonctionne activement, et lorsqu'il y a un excès de produits de réaction (NAD, ATP), il est inhibé. La régulation s'effectue également à l'aide d'hormones : la principale source d'acétyl-CoA est le glucose, donc les hormones qui favorisent la dégradation aérobie du glucose contribuent au fonctionnement du cycle de Krebs. Ces hormones sont :
· l'insuline ;
· adrénaline.
Le glucagon stimule la synthèse du glucose et inhibe les réactions du cycle de Krebs.
En règle générale, le travail du cycle de Krebs n'est pas interrompu en raison de réactions anaplérotiques qui reconstituent le cycle avec des substrats :
Pyruvate + CO 2 + ATP = Oxaloacétate (substrat du cycle de Krebs) + ADP + Fn.
Emploi ATP synthases
Le processus de phosphorylation oxydative est réalisé par le cinquième complexe de la chaîne respiratoire mitochondriale - Proton ATP synthase, constitué de 9 sous-unités de 5 types :
3 sous-unités (d,e,f) contribuent à l'intégrité de l'ATP synthase
· Une sous-unité est l'unité fonctionnelle de base. Il a 3 conformations :
· Conformation L - attache l'ADP et le phosphate (entre dans la mitochondrie à partir du cytoplasme à l'aide de supports spéciaux)
Conformation T - le phosphate rejoint l'ADP et l'ATP se forme
· Conformation O - L'ATP est séparé de la sous-unité b et transféré à la sous-unité b.
· Pour qu'une sous-unité change de conformation, un proton d'hydrogène est nécessaire, puisque la conformation change 3 fois, 3 protons d'hydrogène sont nécessaires. Les protons sont pompés depuis l'espace intermembranaire des mitochondries sous l'influence du potentiel électrochimique.
· la sous-unité b transporte l'ATP vers le transporteur membranaire, qui « jette » l'ATP dans le cytoplasme. En retour, le même transporteur transporte l’ADP depuis le cytoplasme. La membrane interne des mitochondries contient également un transporteur de phosphate du cytoplasme vers la mitochondrie, mais un proton d'hydrogène est nécessaire à son fonctionnement. Ces transporteurs sont appelés translocases.
Total sortie
Pour synthétiser 1 molécule d’ATP, il faut 3 protons.
Inhibiteurs oxydant phosphorylation
Les inhibiteurs bloquent le complexe V :
· Oligomycine – bloque les canaux protoniques de l'ATP synthase.
· Atractyloside, cyclophylline - bloquent les translocases.
Sectionneurs oxydant phosphorylation
Sectionneurs- des substances lipophiles capables d'accepter des protons et de les transférer à travers la membrane interne des mitochondries, en contournant le complexe V (son canal protonique). Sectionneurs :
· Naturel- les produits de peroxydation lipidique, Les acides gras avec une longue chaîne; de fortes doses d'hormones thyroïdiennes.
· Artificiel- dinitrophénol, éther, dérivés de la vitamine K, anesthésiques.
2.2 Phosphorylation du substrat
Substrat UN précisphosphoryle Et itinérant ( biochimique), synthèse de composés phosphorés riches en énergie grâce à l'énergie des réactions redox de glycolyse (catalysées par la phosphoglycéraldéhyde déshydrogénase et l'énolase) et lors de l'oxydation de l'acide a-cétoglutarique dans le cycle de l'acide tricarboxylique (sous l'action de l'a-cétoglutarate déshydrogénase et succinate thiokinase). Des cas de S. f. ont été décrits pour des bactéries. lors de l'oxydation de l'acide pyruvique.C. f., contrairement à la phosphorylation dans la chaîne de transport d'électrons, n'est pas inhibé par les poisons « découplants » (par exemple le dinitrophénol) et n'est pas associé à la fixation d'enzymes dans les membranes mitochondriales. Contribution de S. f. la contribution au pool d'ATP cellulaire dans des conditions aérobies est nettement inférieure à la contribution de la phosphorylation dans la chaîne de transport d'électrons.
Chapitre 3. Façons d'utiliser l'ATP
3.1 Rôle dans la cellule
Le rôle principal de l’ATP dans l’organisme est associé à la fourniture d’énergie pour de nombreuses réactions biochimiques. En tant que porteur de deux liaisons à haute énergie, l’ATP sert de source directe d’énergie pour de nombreux processus biochimiques et physiologiques énergivores. Ce sont toutes des réactions de synthèse de substances complexes dans l'organisme : mise en œuvre d'un transfert actif de molécules à travers membranes biologiques, notamment pour créer un potentiel électrique transmembranaire ; mise en œuvre de la contraction musculaire.
Comme on le sait dans la bioénergie des organismes vivants, deux points principaux sont importants :
a) l'énergie chimique est stockée grâce à la formation d'ATP couplée à des réactions cataboliques exergoniques d'oxydation de substrats organiques ;
b) l'énergie chimique est utilisée par la dégradation de l'ATP, associée à des réactions endergoniques d'anabolisme et à d'autres processus nécessitant de l'énergie.
La question se pose de savoir pourquoi la molécule ATP remplit son rôle central en bioénergétique. Pour le résoudre, considérons la structure de l’ATP Structure ATP - (à pH 7,0 tétracharge anion) .
L'ATP est un composé thermodynamiquement instable. L'instabilité de l'ATP est déterminée, d'une part, par la répulsion électrostatique dans la région d'un amas de charges négatives du même nom, ce qui conduit à une tension dans toute la molécule, mais la liaison est la plus forte - P - O - P, et d'autre part, par une résonance spécifique. Conformément à ce dernier facteur, il existe une compétition entre les atomes de phosphore pour les électrons mobiles non partagés de l'atome d'oxygène situé entre eux, puisque chaque atome de phosphore possède une partie charge positive en raison de l'influence significative des récepteurs électroniques des groupes P=O et P - O-. Ainsi, la possibilité de l'existence de l'ATP est déterminée par la présence d'une quantité suffisante d'énergie chimique dans la molécule pour compenser ces stress physico-chimiques. La molécule d'ATP contient deux liaisons phosphoanhydride (pyrophosphate) dont l'hydrolyse s'accompagne d'une diminution significative de l'énergie libre (à pH 7,0 et 37 o C).
ATP + H 2 O = ADP + H 3 PO 4 G0I = - 31,0 KJ/mol.
ADP + H 2 O = AMP + H 3 PO 4 G0I = - 31,9 KJ/mol.
L’un des problèmes centraux de la bioénergie est la biosynthèse de l’ATP, qui dans la nature se produit par phosphorylation de l’ADP.
La phosphorylation de l'ADP est un processus endergonique et nécessite une source d'énergie. Comme indiqué précédemment, deux de ces sources d'énergie prédominent dans la nature : énergie solaire et l'énergie chimique des composés organiques réduits. Les plantes vertes et certains micro-organismes sont capables de transformer l'énergie des quanta de lumière absorbés en énergie chimique, qui est dépensée pour la phosphorylation de l'ADP au stade lumineux de la photosynthèse. Ce processus de régénération de l’ATP est appelé phosphorylation photosynthétique. La transformation de l'énergie d'oxydation des composés organiques en liaisons macroénergétiques de l'ATP dans des conditions aérobies se produit principalement par phosphorylation oxydative. L'énergie libre nécessaire à la formation d'ATP est générée dans la chaîne respiratoire oxydative des mitochondries.
Un autre type de synthèse d'ATP est connu, appelé phosphorylation du substrat. Contrairement à la phosphorylation oxydative associée au transfert d'électrons, les donneurs du groupe phosphoryle activé (- PO3 H2), nécessaires à la régénération de l'ATP, sont des intermédiaires des processus de glycolyse et du cycle de l'acide tricarboxylique. Dans tous ces cas, les processus oxydatifs conduisent à la formation de composés à haute énergie : 1,3-diphosphoglycérate (glycolyse), succinyl-CoA (cycle de l'acide tricarboxylique), qui, avec la participation d'enzymes appropriées, sont capables de folyler l'ADP et formant de l'ATP. La transformation de l'énergie au niveau du substrat est le seul moyen de synthèse de l'ATP dans les organismes anaérobies. Ce processus de synthèse d'ATP permet de supporter un travail intense les muscles squelettiques pendant les périodes de manque d’oxygène. Il faut rappeler qu’il s’agit de la seule voie de synthèse de l’ATP dans les globules rouges matures dépourvus de mitochondries.
Un rôle particulièrement important dans la bioénergétique de la cellule est joué par le nucléotide adényle, auquel sont attachés deux résidus d'acide phosphorique. Cette substance est appelée acide adénosine triphosphorique (ATP). L'énergie est stockée dans les liaisons chimiques entre les résidus d'acide phosphorique de la molécule d'ATP, qui est libérée lors de la séparation du phosphorite organique :
ATP = ADP+P+E,
où F est une enzyme, E est l’énergie libératrice. Dans cette réaction, de l'acide adénosine phosphorique (ADP) se forme - le reste de la molécule d'ATP et du phosphate organique. Toutes les cellules utilisent l'énergie ATP pour les processus de biosynthèse, le mouvement, la production de chaleur, l'influx nerveux, la luminescence (par exemple les bactéries luminescentes), c'est-à-dire pour tous les processus vitaux.
L'ATP est un accumulateur d'énergie biologique universel. L'énergie lumineuse contenue dans les aliments consommés est stockée dans les molécules d'ATP.
L’apport d’ATP dans la cellule est faible. Ainsi, la réserve d'ATP dans le muscle est suffisante pour 20 à 30 contractions. Avec un travail intense mais de courte durée, les muscles travaillent exclusivement en raison de la dégradation de l'ATP qu'ils contiennent. Après avoir terminé le travail, une personne respire fortement - pendant cette période, les glucides et d'autres substances sont décomposés (l'énergie est accumulée) et l'apport d'ATP dans les cellules est rétabli.
Le rôle de l’ATP comme transmetteur dans les synapses est également connu.
3.2 Rôle dans la fonction enzymatique
Une cellule vivante est loin de l’équilibre système chimique: après tout, l'approche d'un système vivant vers l'équilibre signifie sa désintégration et sa mort. Le produit de chaque enzyme est généralement rapidement consommé car il est utilisé comme substrat par une autre enzyme dans la voie métabolique. Plus important encore, un grand nombre de réactions enzymatiques impliquent la dégradation de l’ATP en ADP et en phosphate inorganique. Pour que cela soit possible, le pool d’ATP doit à son tour être maintenu à un niveau éloigné de l’équilibre, de sorte que le rapport entre la concentration d’ATP et la concentration de ses produits d’hydrolyse soit élevé. Ainsi, le pool d’ATP joue le rôle d’une « batterie » qui maintient le transfert constant d’énergie et d’atomes dans la cellule le long de voies métaboliques déterminées par la présence d’enzymes.
Considérons donc le processus d'hydrolyse de l'ATP et son effet sur le fonctionnement des enzymes. Imaginons un processus biosynthétique typique dans lequel deux monomères - A et B - doivent se combiner dans une réaction de déshydratation (également appelée condensation), accompagnée de la libération d'eau :
A - N + B - OH - AB + H2O
La réaction inverse, appelée hydrolyse, dans laquelle une molécule d’eau décompose un composé A à B lié de manière covalente, sera presque toujours énergétiquement favorable. Cela se produit par exemple lors de la dégradation hydrolytique des protéines, acides nucléiques et les polysaccharides en sous-unités.
La stratégie générale par laquelle les cellules A - B sont formées avec A - H et B - OH comprend une séquence de réactions en plusieurs étapes, à la suite de laquelle n Liant la synthèse énergétiquement défavorable des composés nécessaires avec une réaction bénéfique équilibrée se produit.
L'hydrolyse de l'ATP correspond-elle à une valeur négative importante ? G, par conséquent, l'hydrolyse de l'ATP joue souvent le rôle d'une réaction énergétiquement favorable, grâce à laquelle des réactions de biosynthèse intracellulaire sont effectuées.
Sur le chemin de A - H et B - OH - A - B, associé à l'hydrolyse de l'ATP, l'énergie de l'hydrolyse convertit d'abord B - OH en un intermédiaire à haute énergie, qui réagit ensuite directement avec A - H, formant A - B. Un mécanisme simple pour ce processus implique le transfert du phosphate de l'ATP vers B - OH avec la formation de B - OPO 3, ou B - O - P, et dans ce cas, la réaction totale se produit en seulement deux étapes :
1) B-OH + ATP-B-B-P + ADP
2) A - N + B - O - R - A - B + R
Étant donné que le composé intermédiaire B - O - P formé lors de la réaction est à nouveau détruit, les réactions globales peuvent être décrites à l'aide des équations suivantes :
3) A-N + B - OH - A - B et ATP - ADP + P
La première réaction énergétiquement défavorable s’avère possible car elle est associée à la seconde réaction énergétiquement favorable (hydrolyse de l’ATP). Un exemple de réactions biosynthétiques couplées de ce type est la synthèse de l'acide aminé glutamine.
La valeur G de l'hydrolyse de l'ATP en ADP et en phosphate inorganique dépend de la concentration de toutes les substances en réaction et se situe généralement, pour les conditions cellulaires, entre - 11 et - 13 kcal/mol. La réaction d'hydrolyse de l'ATP peut enfin être utilisée pour réaliser une réaction thermodynamiquement défavorable avec une valeur G d'environ +10 kcal/mol, bien entendu en présence d'une séquence réactionnelle appropriée. Cependant, pour de nombreuses réactions de biosynthèse, même cela est insuffisant ? G = - 13 kcal/mol. Dans ces cas et dans d’autres, la voie d’hydrolyse de l’ATP est modifiée de sorte que l’AMP et le PP (pyrophosphate) se forment en premier. Dans l'étape suivante, le pyrophosphate subit également une hydrolyse ; le changement total d'énergie libre de l'ensemble du processus est d'environ - 26 kcal/mol.
Comment l’énergie issue de l’hydrolyse du pyrophosphate est-elle utilisée dans les réactions biosynthétiques ? L'une des manières peut être démontrée par l'exemple de la synthèse ci-dessus du composé A - B avec A - H et B - OH. À l'aide de l'enzyme appropriée, B - OH peut réagir avec l'ATP et se transformer en un composé à haute énergie B - O - P - P. La réaction comprend désormais trois étapes :
1) B - OH + ATP - B - B - P - P + AMP
2) A - N + B - O - R - R - A - B + RR
3) PP + H2O-2P
La réaction totale peut être représentée comme suit :
A - H + B - OH - A - B et ATP + H2O - AMP + 2P
Étant donné que l'enzyme accélère toujours la réaction catalysée dans le sens direct et inverse, le composé A - B peut se décomposer en réagissant avec le pyrophosphate (réaction, l'inverse de l'étape 2). Cependant, la réaction énergétiquement favorable de l’hydrolyse du pyrophosphate (étape 3) permet de maintenir la stabilité Connexions A-B du fait que la concentration en pyrophosphate reste très faible (cela évite que la réaction inverse de l'étape 2 ne se produise). Ainsi, l’énergie de l’hydrolyse du pyrophosphate garantit que la réaction se déroule dans le sens direct. Un exemple de réaction biosynthétique importante de ce type est la synthèse de polynucléotides.
3.3 Rôle dans la synthèse de l'ADN, de l'ARN et des protéines
Dans tous les organismes connus, les désoxyribonucléotides qui composent l'ADN sont synthétisés par l'action des enzymes ribonucléotide réductase (RNR) sur les ribonucléotides correspondants. Ces enzymes réduisent le résidu de sucre otribose en désoxyribose en éliminant l'oxygène des groupes hydroxyles 2", des substrats diphosphates de ribonucléoside et des produits diphosphates de désoxyribonucléoside. Toutes les enzymes réductases utilisent un mécanisme radical sulfhydryle commun dépendant des résidus réactifs de cystéine qui sont oxydés pour former des liaisons disulfure. pendant la réaction.L'enzyme PHP est traitée par réaction avec la thiorédoxine ou la glutarédoxine.
La régulation du RHP et des enzymes associées maintient un équilibre les uns par rapport aux autres. Une très faible concentration inhibe la synthèse et la réparation de l'ADN et est mortelle pour la cellule, tandis qu'un rapport anormal est mutagène en raison de la probabilité accrue d'inclusion de l'ADN polymérase lors de la synthèse de l'ADN.
Lors de la synthèse des acides nucléiques d'ARN, l'adénosine dérivée de l'ATP est l'un des quatre nucléotides incorporés directement dans les molécules d'ARN par l'ARN polymérase. Énergie, cette polymérisation se produit avec l'élimination du pyrophosphate (deux groupes phosphate). Ce processus est similaire dans la biosynthèse de l'ADN, sauf que l'ATP est réduit en désoxyribonucléotide dATP, avant d'être incorporé à l'ADN.
DANS la synthèse écureuil. Les synthétases aminoacyl-ARNt utilisent les enzymes ATP comme source d'énergie pour attacher une molécule d'ARNt à son acide aminé spécifique, formant ainsi un aminoacyl-ARNt, prêt à être transféré aux ribosomes. L'énergie devient disponible grâce à l'hydrolyse de l'ATP par l'adénosine monophosphate (AMP), qui élimine deux groupes phosphate.
L'ATP est utilisé pour de nombreuses fonctions cellulaires, notamment le travail de transport des substances en mouvement à travers les membranes cellulaires. Il est également utilisé pour les travaux mécaniques, fournissant l’énergie nécessaire à la contraction musculaire. Il fournit de l'énergie non seulement au muscle cardiaque (pour la circulation sanguine) et aux muscles squelettiques (par exemple, pour les mouvements corporels importants), mais également aux chromosomes et aux flagelles afin qu'ils puissent remplir leurs nombreuses fonctions. Le rôle majeur de l'ATP est dans le travail chimique, fournissant l'énergie nécessaire à la synthèse de plusieurs milliers de types de macromolécules nécessaires à l'existence d'une cellule.
L'ATP est également utilisé comme interrupteur marche-arrêt pour contrôler les réactions chimiques et envoyer des informations. La forme des chaînes protéiques qui produisent les éléments constitutifs et autres structures utilisées dans la vie est principalement déterminée par de faibles liaisons chimiques qui disparaissent et se restructurent facilement. Ces circuits peuvent raccourcir, allonger et changer de forme en réponse à l’entrée ou à la sortie d’énergie. Les changements dans les chaînes modifient la forme de la protéine et peuvent également modifier sa fonction ou la rendre active ou inactive.
Les molécules d'ATP peuvent se lier à une partie d'une molécule protéique, provoquant le glissement ou le léger mouvement d'une autre partie de la même molécule, ce qui la fait changer de conformation, inactivant la molécule. Une fois éliminé, l’ATP fait revenir la protéine à sa forme originale et elle est donc à nouveau fonctionnelle.
Le cycle peut être répété jusqu'à ce que la molécule revienne, agissant efficacement à la fois comme un interrupteur marche/arrêt. L’ajout de phosphore (phosphorylation) et l’élimination du phosphore d’une protéine (déphosphorylation) peuvent servir d’interrupteur marche/arrêt.
3.4 Autres fonctions de l'ATP
Rôle V métabolisme, la synthèse Et actif transport
Ainsi, l’ATP transfère de l’énergie entre des réactions métaboliques spatialement séparées. L'ATP est la principale source d'énergie pour la plupart des fonctions cellulaires. Cela implique la synthèse de macromolécules, notamment d’ADN et d’ARN, et de protéines. L'ATP joue également un rôle important dans le transport des macromolécules à travers les membranes cellulaires, comme l'exocytose et l'endocytose.
Rôle V structure cellules Et mouvement
L'ATP participe au maintien de la structure cellulaire en facilitant l'assemblage et le démontage des éléments du cytosquelette. En raison de ce processus, l’ATP est nécessaire à la contraction des filaments d’actine et la myosine est nécessaire à la contraction musculaire. Ce dernier processus constitue l’un des besoins énergétiques de base des animaux et est essentiel au mouvement et à la respiration.
Rôle V signal systèmes
Dansextracellulairesignalsystèmes
L'ATP est également une molécule de signalisation. L'ATP, l'ADP ou l'adénosine sont reconnus comme des récepteurs purinergiques. Les récepteurs purinos pourraient être les récepteurs les plus abondants dans les tissus des mammifères.
Chez l’homme, ce rôle de signalisation est important dans les systèmes nerveux central et périphérique. L'activité dépend de la libération d'ATP par les synapses, les axones et les cellules gliales par activation purinergique des récepteurs membranaires.
Dansintracellulairesignalsystèmes
L'ATP est essentiel dans les processus de transduction du signal. Il est utilisé par les kinases comme source de groupes phosphate dans leur réaction de transfert de phosphate. Les kinases sur des supports tels que les protéines membranaires ou les lipides constituent une forme courante de signal. La phosphorylation des protéines par les kinases peut activer cette cascade, comme la cascade des protéines kinases activées par les mitogènes.
L'ATP est également utilisé par l'adénylate cyclase et est converti en une deuxième molécule messagère appelée AMP, qui est impliquée dans le déclenchement des signaux calciques pour libérer le calcium des réserves intracellulaires. [38] Cette forme de signal est particulièrement importante dans le fonctionnement cérébral, bien qu'elle soit impliquée dans la régulation de nombreux autres processus cellulaires.
Conclusion
1. Adénosine triphosphate - un nucléotide qui joue un rôle extrêmement important dans l'échange d'énergie et de substances dans les organismes ; Tout d’abord, ce composé est connu comme une source universelle d’énergie pour tous les processus biochimiques se produisant dans les systèmes vivants. Chimiquement, l'ATP est l'ester triphosphate de l'adénosine, qui est un dérivé de l'adénine et du ribose. La structure de l'ATP est similaire à celle du nucléotide adénine qui fait partie de l'ARN, sauf qu'au lieu d'un acide phosphorique, l'ATP contient trois résidus d'acide phosphorique. Les cellules ne sont pas capables de contenir des acides en quantités notables, mais seulement leurs sels. Par conséquent, l'acide phosphorique entre dans l'ATP sous forme de résidu (au lieu du groupe OH de l'acide, il y a un atome d'oxygène chargé négativement).
2. Dans l’organisme, l’ATP est synthétisée par phosphorylation de l’ADP :
ADP + H 3 PO 4 + énergie> ATP + H2O.
La phosphorylation de l'ADP est possible de deux manières : la phosphorylation du substrat et la phosphorylation oxydative (en utilisant l'énergie des substances oxydantes).
La phosphorylation oxydative - l'un des composants les plus importants de la respiration cellulaire, conduisant à la production d'énergie sous forme d'ATP. Les substrats de la phosphorylation oxydative sont les produits de dégradation des composés organiques – protéines, graisses et glucides. Le processus de phosphorylation oxydative a lieu sur les crêtes des mitochondries.
Substrat UN précisphosphoryle Et itinérant ( biochimique), synthèse de composés phosphorés riches en énergie grâce à l'énergie des réactions redox de glycolyse et lors de l'oxydation de l'acide a-cétoglutarique dans le cycle de l'acide tricarboxylique.
3. Le rôle principal de l'ATP dans le corps est associé à la fourniture d'énergie pour de nombreuses réactions biochimiques. En tant que porteur de deux liaisons à haute énergie, l’ATP sert de source directe d’énergie pour de nombreux processus biochimiques et physiologiques énergivores. Dans la bioénergétique des organismes vivants, les éléments suivants sont importants : l'énergie chimique est stockée grâce à la formation d'ATP, couplée à des réactions cataboliques exergoniques d'oxydation des substrats organiques ; L'énergie chimique est utilisée par la dégradation de l'ATP, associée à des réactions endergoniques d'anabolisme et à d'autres processus nécessitant de l'énergie.
4. Avec une charge accrue (par exemple, lors de la course à pied sur de courtes distances), les muscles travaillent exclusivement grâce à l'apport d'ATP. Dans les cellules musculaires, cette réserve est suffisante pour plusieurs dizaines de contractions, puis la quantité d'ATP doit être reconstituée. La synthèse de l'ATP à partir de l'ADP et de l'AMP est due à l'énergie libérée lors de la dégradation des glucides, des lipides et d'autres substances. Effectuer un travail mental nécessite également une grande quantité d’ATP. Pour cette raison, les personnes souffrant de travail mental ont besoin d'une quantité accrue de glucose, dont la dégradation assure la synthèse de l'ATP.
En plus de l'énergie, l'ATP remplit un certain nombre d'autres fonctions tout aussi importantes dans l'organisme :
· Avec d'autres nucléosides triphosphates, l'ATP est le produit de départ de la synthèse des acides nucléiques.
· De plus, l'ATP joue un rôle important dans la régulation de nombreux processus biochimiques. En tant qu'effecteur allostérique d'un certain nombre d'enzymes, l'ATP, rejoignant leurs centres de régulation, améliore ou supprime leur activité.
· L'ATP est également un précurseur direct pour la synthèse de l'adénosine monophosphate cyclique, un messager secondaire de la transmission du signal hormonal dans la cellule.
Le rôle de l’ATP comme transmetteur dans les synapses est également connu.
Bibliographie
1. Lemeza, N.A. Un manuel de biologie pour les candidats aux universités / L.V. Kamlyuk N.D. Lisov. - Mn. : Unipress, 2011 - 624 p.
2. Lodish, H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J. Molecular Cell Biology, 5e éd. - New York : WH Freeman, 2004.
3. Romanovsky, Yu.M. Convertisseurs d'énergie moléculaire des cellules vivantes. Proton ATP synthase - un moteur moléculaire rotatif / Yu.M. Romanovsky A.N. Tikhonov // UFN. - 2010. - T.180. - P.931 - 956.
4. Voet D, Voet JG. Biochimie Vol 1 3e éd. - Wiley : Hoboken, New Jersey. - N-Y : W. H. Freeman and Company, 2002. - 487 frotter.
5. chimie générale. Chimie biophysique. Chimie des éléments biogéniques. M. : lycée, 1993
6. Vershubsky, A.V. Biophysique. / UN V. Vershubsky, V.I. Priklonsky, A.N. Tikhonov. - M : 471-481.
7. Alberts B. Biologie moléculaire des cellules en 3 volumes. / Alberts B., Bray D., Lewis J. et autres M. : Mir, 1994.1558 p.
8. Nikolaev A. Ya. Chimie biologique - M. : Medical Information Agency LLC, 1998.
9. Berg, J. M. Biochemistry, édition internationale. / Berg, J.M, Tymoczko, J.L, Stryer, L. - New York : WH Freeman, 2011 ; p287.
10. Knorre D.G. Chimie biologique : Manuel. pour la chimie, le biol. Et chérie. spécialiste. les universités - 3e éd., rév. / Knorre D.G., Mysina S.D. - M. : Plus haut. école, 2000. - 479 p. : ill.
11. Eliot, V. Biochimie et biologie moléculaire / V. Eliot, D. Eliot. - M. : Maison d'édition de l'Institut de recherche en chimie biomédicale de l'Académie russe des sciences médicales, LLC "Materik-alpha", 1999, - 372 p.
12. Shina CL, K., 7 Areieh, W. Sur l'énergie de l'hydrolyse de l'ATP en solution. Journal de chimie physique B, 113 (47), (2009).
13. Berg, J. M. Biochimie / J. M. Berg : J. L. Tymoczko, L. Stryer. - N-Y : W. H. Freeman and Company, 2002. - 1514 p.
...Documents similaires
Composés organiques dans le corps humain. Structure, fonctions et classification des protéines. Acides nucléiques (polynucléotides), caractéristiques structurelles et propriétés de l'ARN et de l'ADN. Les glucides dans la nature et dans le corps humain. Les lipides sont des graisses et des substances apparentées.
résumé, ajouté le 06/09/2009
Le processus de synthèse des protéines et leur rôle dans la vie des organismes vivants. Fonctions et Propriétés chimiques acides aminés. Raisons de leur carence dans le corps humain. Types d'aliments contenant des acides essentiels. Acides aminés synthétisés dans le foie.
présentation, ajouté le 23/10/2014
Fonctions énergétiques, de stockage et de soutien des glucides. Propriétés des monosaccharides comme principale source d'énergie dans le corps humain ; glucose. Les principaux représentants des disaccharides ; saccharose. Polysaccharides, formation d'amidon, métabolisme des glucides.
rapport, ajouté le 30/04/2010
Fonctions métaboliques dans le corps : fournir aux organes et aux systèmes l'énergie générée lors de la dégradation des nutriments ; transformation de molécules produits alimentaires en blocs de construction ; formation d'acides nucléiques, de lipides, de glucides et d'autres composants.
résumé, ajouté le 20/01/2009
Le rôle et l'importance des protéines, des graisses et des glucides pour le déroulement normal de tous les processus vitaux. Composition, structure et propriétés clés des protéines, des graisses et des glucides, leur les tâches les plus importantes et fonctions dans le corps. Principales sources de ces nutriments.
présentation, ajouté le 11/04/2013
Caractéristiques de la structure des molécules de cholestérol en tant que composant important membrane cellulaire. Etude des mécanismes de régulation du métabolisme du cholestérol dans le corps humain. Analyse des caractéristiques de l'apparition d'un excès de lipoprotéines de basse densité dans le sang.
résumé, ajouté le 17/06/2012
Métabolisme des protéines, des lipides et des glucides. Types de nutrition humaine : alimentation omnivore, séparée et pauvre en glucides, végétarisme, régime alimentaire cru. Le rôle des protéines dans le métabolisme. Manque de graisse dans le corps. Modifications du corps résultant de changements dans le type de régime alimentaire.
travail de cours, ajouté le 02/02/2014
Prise en compte de la participation du fer aux processus oxydatifs et à la synthèse du collagène. Familiarisation avec l'importance de l'hémoglobine dans les processus de formation du sang. Vertiges, essoufflement et troubles métaboliques dus à une carence en fer dans le corps humain.
présentation, ajouté le 08/02/2012
Propriétés du fluor et du fer. Besoin quotidien du corps. Fonctions du fluorure dans l'organisme, influence, dose létale, interaction avec d'autres substances. Le fer dans le corps humain, ses sources. Conséquences de la carence en fer pour l'organisme et de son excès.
présentation, ajouté le 14/02/2017
Les protéines comme sources alimentaires, leurs principales fonctions. Acides aminés impliqués dans la création des protéines. Structure de la chaîne polypeptidique. Transformations des protéines dans le corps. Protéines complètes et incomplètes. Structure des protéines, propriétés chimiques, réactions qualitatives.
Les aliments qui pénètrent dans le corps humain subissent des transformations chimiques complexes, c'est-à-dire subit partiellement une oxydation ou une décomposition anaérobie. La dégradation anaérobie libère l'énergie chimique nécessaire au mouvement, ainsi qu'à la synthèse des substances nécessaires à l'organisme.
Le métabolisme dans les organismes vivants se compose de deux processus interconnectés :
- anabolisme
- catabolisme
Anabolisme ou assimilation– synthèse à partir de composés plus simples et plus complexes basés sur ceux entrant dans l’organisme à partir de environnement externe substances.
Par exemple, la matière organique des plantes vertes est formée par la photosynthèse à partir du dioxyde de carbone et de l’eau.
Catabolisme ou dissimilation– un processus opposé à l’anabolisme. Au cours du catabolisme, les composés complexes sont décomposés en composés plus simples, qui sont ensuite libérés sous forme de produits finaux dans l'environnement.
Dans le catabolisme, la principale source de glucides sont les glucides qui sont décomposés par les enzymes hydrolytiques. Si chez les plantes, lors de la germination des graines, l'amidon est hydrolysé par l'enzyme amylase, formant le disaccharide maltose, alors chez les animaux, sous l'influence de l'amylase salivaire et pancréatique, formant du maltose. Ensuite, le maltose, sous l'action de l'enzyme maltase, est transformé en glucose qui, à la suite de la fermentation, de la glycolyse et de la respiration, est finalement décomposé en dioxyde de carbone et en eau. L’énergie libérée lors de ces processus s’accumule dans le corps. Il a été établi que la combustion d'un gramme de glucides libère 4,1 kcal (17,22 kJ).
Le catabolisme des graisses et des protéines commence également par leur dégradation hydrolytique sous l'influence d'enzymes spécifiques, avec la formation dans le premier cas d'acides gras libres et de glycérol, dans le second de peptides et d'acides aminés de faible poids moléculaire.
Le métabolisme ou métabolisme peut être divisé en trois étapes :
- La première est la digestion, qui consiste en la transformation mécanique et chimique des aliments dans les organes digestifs et en l’absorption des nutriments.
- La deuxième étape est le métabolisme intermédiaire, qui comprend les processus de dégradation et de synthèse des substances. Ce processus s'accompagne de la formation de produits métaboliques intermédiaires et finaux. Par exemple, le glucose subit un certain nombre de transformations intermédiaires avant d'être converti en produits finaux de l'échange de CO2 et H2O.
- La troisième étape est la libération des produits métaboliques du corps avec l'air expiré, l'urine, etc. Les substances qui influencent le cours des réactions métaboliques sont appelées métabolites. Ceux-ci comprennent les acides aminés, les acides gras, les sucres, les bases azotées et d'autres composés.
Le métabolisme ou métabolisme est inextricablement lié à la transformation de l'énergie. Un organisme vivant a constamment besoin d’énergie provenant de l’environnement extérieur. Il a été constaté que lors de la photosynthèse, c'est-à-dire En convertissant l'énergie de la lumière solaire, cette dernière est stockée sous forme d'énergie chimique potentielle dans les substances organiques. L'énergie chimique potentielle, formée à la suite de la dégradation des glucides, des graisses et d'autres composés de haut poids moléculaire, s'accumule ou s'accumule dans des composés à haute énergie.
Dans les processus d'échange, l'énergie est libérée comme suit. Premièrement, les substances de haut poids moléculaire se décomposent par hydrolyse en substances de faible poids moléculaire ; par exemple, les polysaccharides - aux monosaccharides ; protéines – aux acides aminés; les graisses – aux acides gras et au glycérol. Dans le même temps, l'énergie libérée lors de la décomposition hydrolytique de ces substances est très insignifiante. Ensuite, une grande quantité d’énergie est libérée lors du processus de glycolyse, d’oxydation des acides gras et des acides aminés. Parmi les produits d'hydrolyse, trois ont une importance énergétique primordiale : l'acétylcoenzyme A, l'acide B-cétoglutarique et l'acide oxaloacétique. Ces substances subissent une oxydation via le cycle de l'acide di-tricarboxylique (cycle de Krebs). Environ les 2/3 de l'énergie sont libérés dans le cycle de Krebs.
L'ATP capture et stocke l'énergie libérée lors de la dégradation des composés organiques de haut poids moléculaire dans le corps. Dans le même temps, l'ATP est synthétisée dans la cellule et l'énergie s'accumule dans ses liaisons phosphorées. Lors de la synthèse des protéines, ainsi que lors du fonctionnement des organes et des muscles, la dégradation de l'ATP se produit au niveau des liaisons macroergiques avec libération d'énergie. L'énergie résultante sert de source de synthèse ainsi que de processus moteurs.
De ce qui précède, il s'ensuit que l'ATP est un lien entre deux processus opposés, où il accumule de l'énergie lors de la dégradation des substances et la libère lors de l'assimilation.
Le rôle biologique de l’ATP dans l’énergie métabolique peut être illustré à l’aide de l’exemple d’un cœur qui bat. Lorsqu'il interagit avec les protéines contractiles musculaires, l'ATP fournit l'énergie nécessaire pour contracter le cœur et pousser le sang dans le système circulatoire. Dans le même temps, pour le bon fonctionnement du cœur, une reconstitution constante de la quantité d'ATP est nécessaire. Si le cœur ne reçoit pas la quantité requise de matière nutritionnelle et de « carburant » (glucides et produits de leur dégradation), ainsi que l'oxygène nécessaire à la formation d'ATP, il y a alors une perturbation du fonctionnement du cœur.
La quantité d'ATP nécessaire au fonctionnement de divers organes est produite dans les organismes cellulaires - les mitochondries en cours de phosphorylation oxydative.