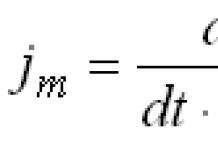3.4. Les noms doivent être écrits dans l'ordre suivant : prénom, patronyme, nom de famille (ou - initiales, nom de famille, mais il n'est pas permis de transférer les initiales séparément du nom de famille à la ligne suivante).
4. Formules et unités de quantités
4.1. Les formules sont écrites sur une ligne séparée et centrées. Une ligne libre doit être laissée au-dessus et en dessous de chaque formule.
4.2. Après la formule, placez une liste de tous les symboles acceptés dans la formule avec un décodage de leurs significations et une indication de la dimension (si nécessaire). Les désignations des lettres sont données dans le même ordre dans lequel elles sont données dans la formule.
4.3. Les formules sont numérotées consécutivement tout au long de l'ouvrage en utilisant des chiffres arabes. Dans ce cas, le numéro de formule est indiqué entre parenthèses à l’extrême droite de la ligne. Une formule signifie –
4.4. Dans les formules, en tant que symboles de grandeurs physiques, les désignations établies par les normes nationales pertinentes (GOST 8.417) doivent être utilisées. Explications des symboles et des coefficients numériques inclus dans la formule, s'ils n'ont pas été expliqués précédemment
V texte, doit être indiqué directement sous la formule et doit correspondre au type et à la taille de la police adoptée lors de l'écriture de la formule elle-même. Les explications pour chaque symbole doivent être données sur une nouvelle ligne dans l'ordre dans lequel les symboles sont donnés dans la formule.
4.6. La première ligne de l’explication doit commencer en retrait par le mot « où » sans deux points après. Panneaux« – » (tiret) sont situés sur la même ligne verticale.
Par exemple,
VAN = ∑ |
−Je, |
|||
(1+r) |
||||
t = 1 |
où NPV est la valeur actuelle nette ;
CF – flux de trésorerie total pendant la période t ; I – montant de l'investissement ;
r – taux d'actualisation ; n – nombre de périodes.
4.7. Les signes de ponctuation avant et après la formule sont placés selon leur signification. Les formules qui se succèdent et ne sont pas séparées par du texte sont séparées par une virgule.
4.8. Si la formule ne tient pas sur une ligne, une partie de celle-ci est transférée sur une autre ligne uniquement sur le signe mathématique de la ligne principale, assurez-vous de répéter le signe dans la deuxième ligne. Lorsque vous transférez une formule vers le signe de multiplication, utilisez le signe « × ». Lors de l'écriture de formules, ce n'est pas autorisé
lignes de rupture. Dans une formule multiligne, le numéro de formule est placé contre la dernière ligne.
4.9. Les lettres, images ou signes conventionnels doivent être conformes à ceux adoptés dans les normes de l'État (GOST 8.417).
4.10. S'il est nécessaire d'utiliser des symboles, des images ou des signes qui ne sont pas établis par les normes en vigueur, ils doivent être expliqués dans le texte ou dans la liste des symboles.
4.11. Le texte doit utiliser des unités standardisées de grandeurs physiques, leurs noms et désignations conformément à GOST
4.12. L'unité de quantité physique à partir du nombre est indiquée séparée par un espace, comprenant des pourcentages, par exemple 5 m, 99,4 %.
4.13. Les intervalles de valeurs sous la forme « de et vers » sont écrits sous forme de tirets sans espaces. Par exemple, 8-11% ou s. 5-7, etc.
4.14. Lors de la référence à du matériel numérique, seuls des chiffres arabes doivent être utilisés, à l'exception de la numérotation généralement acceptée des trimestres et des semestres, qui sont indiqués par des chiffres romains. Les nombres cardinaux dans le texte sont donnés sans fin de casse.
5. Conception des illustrations
L'illustration doit avoir un titre placé en dessous. Si nécessaire, des données explicatives (texte sous la figure) sont également placées sous l'illustration.
Les illustrations sont désignées par le mot « Fig ». et sont numérotés séquentiellement en chiffres arabes à l'intérieur du chapitre, à l'exception des illustrations données en annexe. Le numéro de l’illustration est placé sous la légende explicative. Il n’y a pas de point à la fin du titre de l’illustration.
Le numéro de l’illustration doit être composé du numéro de chapitre et du numéro d’ordre de l’illustration, séparés par un point. Par exemple : Fig. 1.2. Deuxième dessin du premier chapitre.
Un exemple de conception d'un dessin avec une légende est donné
Riz. 1.2. Parts de facteurs influençant l'efficacité du flux de documents
6. Conception des tableaux
6.1. Le matériel numérique, la comparaison et l'identification de certains modèles sont présentés sous forme de tableaux. Un tableau est une méthode de présentation d'informations dans laquelle le matériel numérique ou textuel est regroupé en colonnes délimitées les unes des autres par des lignes verticales et horizontales.
6.2. Selon le contenu, les tableaux sont divisés en analytiques et non analytiques. Les tableaux analytiques sont le résultat du traitement et de l’analyse d’indicateurs numériques. Après de tels tableaux, une généralisation est faite comme une nouvelle connaissance (inférentielle), qui est introduite dans le texte avec les mots : « le tableau nous permet de conclure que... », « d'après le tableau il est clair que... » , "le tableau permet de conclure que..." et ainsi de suite. Souvent, de tels tableaux permettent d'identifier et de formuler certains modèles. Les tableaux non analytiques contiennent généralement des données statistiques brutes qui sont nécessaires uniquement à des fins d'information ou de déclaration. Il est recommandé que ces tableaux soient inclus en annexe.
6.3. Typiquement, un tableau est constitué des éléments suivants : numéro de série, en-tête thématique, barre latérale, en-têtes de colonnes verticales (en-tête de tableau), colonnes horizontales et verticales.
6.4. Tous les tableaux, s'il y en a plusieurs, sont numérotés en chiffres arabes, sans indication du signe dièse, à l'intérieur du chapitre. Le numéro est placé dans le coin supérieur droit au-dessus du titre du tableau après le mot « Tableau... », par exemple :
Tableau 1.2, tableau 2.1.9. Le numéro du tableau indique : le premier chiffre est le numéro du chapitre, le deuxième chiffre est le numéro d'ordre du tableau dans le chapitre. Il n'y a pas de point à la fin du numéro de tableau. Les tableaux sont dotés de titres thématiques, placés au centre de la page et écrits en majuscules sans point à la fin. Les noms des tables ne sont pas affichés en gras.
6.5. Le tableau s'étend sur une seule page. Si le tableau ne tient pas sur une page, il est alors transféré sur d'autres, tandis que le titre du tableau est placé sur la première page, et sur les pages suivantes, l'en-tête du tableau doit être répété et en dessous doit être placé l'inscription : « Suite du tableau 1.2. » Si l'en-tête du tableau est encombrant, il est permis de ne pas le répéter. Dans ce cas, les colonnes sont numérotées et leur numérotation est répétée sur les pages suivantes.
6.6. Le tableau ne doit pas contenir de colonnes vides. Si des données numériques ou autres ne sont pas indiquées dans la colonne, un tiret est inséré.
6.7. Le tableau est placé après la première mention de celui-ci dans le texte. Il est permis de placer le tableau le long du côté long de la feuille de manière à ce qu'il puisse être lu dans le sens des aiguilles d'une montre, le numéro de page étant placé au milieu inférieur de la partie courte de la feuille.
6.8. Le numéro de colonne n’est pas inclus dans les tableaux.
6.9. Les abréviations non standard ne sont pas autorisées dans les titres des tableaux. Dans les noms de graphes, les inscriptions sont écrites au nominatif, singulier.
6.10. Il est permis d'utiliser une taille de police et un espacement plus petits dans le tableau que dans le texte (taille en points 12, interligne simple). Les lignes horizontales et verticales délimitant les lignes du tableau ne peuvent être tracées si leur absence ne rend pas difficile l'utilisation du tableau.
6.11. Les titres des colonnes et des lignes du tableau doivent être écrits avec une lettre majuscule et les sous-titres des colonnes avec une lettre minuscule s'ils forment une phrase avec le titre, ou avec une lettre majuscule s'ils ont une signification indépendante. Il n'y a pas de points à la fin des titres et sous-titres des tableaux. Les titres et sous-titres des colonnes sont indiqués au singulier. Le titre de chaque colonne doit être situé directement au-dessus.
6.12. Les nombres dans les colonnes des tableaux doivent être placés de manière à ce que les chiffres des nombres de toute la colonne soient situés les uns au-dessus des autres s'ils se rapportent au même indicateur. Dans une colonne, le même nombre de décimales doit être respecté pour toutes les valeurs.
6.13. Toutes les données présentées dans le tableau doivent être fiables, homogènes et comparables, et leur regroupement doit être basé sur des caractéristiques essentielles. Sous le tableau (pas en bas de page !), vous devez indiquer la source (voir tableau 1.2.).
Ainsi, les tableaux statistiques et les chiffres contenus dans le texte doivent être correctement formatés. L'exigence générale est la suivante : si un tableau, un diagramme ou un graphique est supprimé du texte, sa signification et la source des données doivent être parfaitement claires. Ainsi,
Il est possible d'établir le type de formule chimique à l'aide de données structurelles (c'est-à-dire en utilisant un modèle de structure ou sa projection - dessin) d'une autre manière, en comptant le nombre d'atomes de chaque type (élément chimique) par cellule unitaire . Par exemple, dans la structure de la fluorite CaF 2, les huit ions F - sont situés à l'intérieur de la cellule unitaire, c'est-à-dire qu'ils appartiennent uniquement à cette cellule. L'emplacement des ions Ca 2+ est différent : certains d'entre eux sont localisés aux huit sommets de la cellule cubique de la structure minérale, l'autre partie - au centre de ses six faces. Puisque chacun des huit ions Ca 2+ « sommet » appartient simultanément à huit cellules unitaires voisines - les cubes, alors seule une partie de chacune d'elles appartient à la cellule d'origine. Ainsi, la contribution des atomes de Ca « sommet » à la cellule initiale sera égale à 1 Ca (1/8 x 8 = 1 Ca). Chacun des six atomes de Ca situés au centre des faces d'une cellule cubique appartient simultanément à deux cellules voisines. La contribution des six atomes de Ca centrant les faces du cube sera donc égale à 1/2 x 6 = 3 Ca. En conséquence, il y aura 1 + 3 = 4 atomes de Ca par maille unitaire. Le calcul montre qu'il y a quatre atomes de Ca et huit atomes de F. Cela confirme le type de formule chimique (AX 2) du minéral - CaF 2, où il y a deux fois moins d'atomes de Ca que d'atomes de F. Il est facile de arriver à des résultats similaires si l'on déplace l'origine des coordonnées de la cellule unitaire de sorte que tous les atomes soient dans une cellule. La détermination du nombre d'atomes dans une cellule de Bravais permet, en plus du type de formule chimique, d'obtenir une autre constante utile - la nombre d'unités de formule, désigné par la lettre Z Pour les substances simples constituées d'atomes d'un élément ( Cu, Fe, Se, etc.), le nombre d'unités de formule correspond au nombre d'atomes dans la maille unitaire. Pour les substances moléculaires simples (I 2, S 8, etc.) et les composés moléculaires (CO 2, realgar As 4 S 4), le nombre Z est égal au nombre de molécules dans la cellule. Dans la grande majorité des composés inorganiques et intermétalliques (NaCl, CaF 2, CuAu, etc.), il n'y a pas de molécules, et dans ce cas, au lieu du terme « nombre de molécules », le terme « nombre d'unités de formule » est utilisé . Dans notre exemple, pour la fluorite 4, puisque quatre atomes de Ca et huit atomes de F par cellule de Bravais équivaudront à quatre unités de formule « CaF 2 ». Le nombre d'unités de formule peut être déterminé expérimentalement lors du processus d'examen aux rayons X de la fluorine 4. substance. Si la structure ne contient pas de microdéfauts tels que des lacunes dans la position des atomes ou le remplacement de certaines particules par d'autres, ainsi que des macrodéfauts (fissures, inclusions, vides interblocs), alors dans l'erreur expérimentale Z devrait s'avérer être un nombre entier . En déterminant Z expérimentalement et en l'arrondissant à un nombre entier, nous pouvons calculer la densité d'un monocristal idéal, appelée densité des rayons X.
N'importe lequel la mesure associé à la recherche de valeurs numériques grandeurs physiques, avec leur aide, les schémas des phénomènes étudiés sont déterminés.
Concept grandeurs physiques, Par exemple, la force, le poids, etc., sont le reflet des caractéristiques objectivement existantes d'inertie, d'extension, etc., inhérentes aux objets matériels. Ces caractéristiques existent en dehors et indépendamment de notre conscience, ne dépendant pas de la personne, de la qualité des moyens et méthodes utilisés dans les mesures.
Les grandeurs physiques qui caractérisent un objet matériel dans des conditions données ne sont pas créées par des mesures, mais sont simplement déterminées à l'aide de celles-ci. Mesure Pour toute grandeur, cela signifie déterminer sa relation numérique avec une autre grandeur homogène, qui est prise comme unité de mesure.
Basé sur ceci, la mesure est le processus de comparaison d'une quantité donnée avec une certaine valeur de celle-ci, qui est considérée comme unité de mesure.
Formule pour la relation entre la quantité pour laquelle l'unité dérivée est établie et les quantités A, B, C, ... unités ils s'installent indépendamment, vue générale :
Où k- coefficient numérique (dans un cas donné k=1).
La formule pour connecter une unité dérivée avec des unités de base ou autres est appelée formuledimensions, et les exposants dimensions Pour faciliter l'utilisation pratique des unités, des concepts tels que les unités multiples et sous-multiples ont été introduits.
Unité multiple- une unité qui est un nombre entier de fois plus grande qu'une unité système ou non système. Une unité multiple est formée en multipliant l’unité de base ou dérivée par le nombre 10 à la puissance positive appropriée.
unité sous-multiple- une unité qui est un nombre entier de fois plus petit qu'une unité système ou non système. Une unité sous-multiple est formée en multipliant l’unité de base ou dérivée par le nombre 10 à la puissance négative correspondante.
Définition du terme « unité de mesure ».
Unification de l'unité de mesure traite d'une science appelée métrologie. Traduit exactement, c’est la science de la mesure.
En consultant le Dictionnaire International de Métrologie, nous constatons que unité est une grandeur scalaire réelle définie et acceptée par convention, avec laquelle il est facile de comparer toute autre grandeur du même genre et d'exprimer leur relation à l'aide d'un nombre.
Une unité de mesure peut également être considérée comme une grandeur physique. Cependant, il existe une différence très importante entre une grandeur physique et une unité de mesure : une unité de mesure a une valeur numérique fixe et convenue. Cela signifie que différentes unités de mesure sont possibles pour la même grandeur physique.
Par exemple, le poids peut avoir les unités suivantes : kilogramme, gramme, livre, poud, centner. La différence entre eux est claire pour tout le monde.
La valeur numérique d'une grandeur physique est représentée en utilisant le rapport entre la valeur mesurée et la valeur standard, qui est unité de mesure. Le nombre dont l'unité de mesure est indiquée est numéro nommé.
Il existe des unités de base et dérivées.
Unités de base défini pour les grandeurs physiques sélectionnées comme base dans un système particulier de grandeurs physiques.
Ainsi, le Système International d'Unités (SI) est basé sur le Système International d'Unités, dans lequel les grandeurs de base sont sept grandeurs : longueur, masse, temps, courant électrique, température thermodynamique, quantité de matière et intensité lumineuse. Cela signifie qu'en SI, les unités de base sont les unités de quantités indiquées ci-dessus.
Taille de l'unité de base sont établis par accord au sein d'un système d'unités spécifique et sont fixés soit à l'aide de normes (prototypes), soit en fixant les valeurs numériques des constantes physiques fondamentales.
Unités dérivées déterminé par la méthode de base consistant à utiliser les connexions entre les grandeurs physiques qui sont établies dans le système de grandeurs physiques.
Il existe un grand nombre de systèmes d'unités différents. Ils diffèrent à la fois par les systèmes de grandeurs sur lesquels ils se basent et par le choix des unités de base.
Habituellement, l'État, par le biais de lois, établit un certain système d'unités dont l'utilisation est préférable ou obligatoire dans le pays. Dans la Fédération de Russie, les principales unités de quantités sont le système SI.
Systèmes d'unités de mesure.
Systèmes métriques.
- MKGSS,
Systèmes d'unités de mesure naturelles.
- Système atomique d'unités,
- Unités Planck
- Système géométrique d'unités,
- Unités Lorentz-Heaviside.
Systèmes de mesures traditionnels.
- Système de mesures russe,
- Système de mesures anglais,
- Système de mesures français,
- Système de mesures chinois,
- Système de mesures japonais,
- Déjà obsolète (grec ancien, romain antique, égyptien ancien, babylonien ancien, hébreu ancien).
Unités de mesure regroupées par grandeurs physiques.
- Unités de masse (masse),
- Unités de température (température),
- Unités de distance (distance),
- Unités de surface (superficie),
- Unités de volume (volume),
- Unités de mesure de l'information (informations),
- Unités de temps (temps),
- Unités de pression (pression),
- Unités de flux thermique (flux thermique).
Mots clés du résumé : formule chimique, indice, coefficient, composition qualitative et quantitative, unité de formule.
est un enregistrement conventionnel de la composition d'une substance à l'aide de symboles et d'indices chimiques.
Le nombre dans la formule en bas à droite du signe de l'élément s'appelle indice. L'indice désigne le nombre d'atomes d'un élément qui composent une substance donnée.
Si vous devez désigner non pas une, mais plusieurs molécules (ou atomes individuels), alors avant la formule chimique (ou le signe), mettez le numéro correspondant, appelé coefficient. Par exemple, trois molécules d'eau sont désignées 3H2O, cinq atomes de fer - 5Fe. Indice 1 dans les formules chimiques et le coefficient 1 N'écrivez pas avant les symboles chimiques et les formules.
Les formules présentées dans la figure se lisent comme ceci : trois-cuprum-chlore-deux, cinq-aluminium-deux-o-trois, trois-ferrum-chlore-trois . Enregistrer 5H 2 O(cinq-cendres-deux-o) doit être compris comme suit : cinq molécules d'eau sont formées de dix atomes d'hydrogène et de cinq atomes d'oxygène.
Une formule chimique montre de quels atomes de quels éléments une substance est constituée (c'est-à-dire composition qualitative de la substance); et quel est le rapport des atomes de ces éléments (c.-à-d. composition quantitative de la substance).

Unité de formule
Formules chimiques de substances ayant une structure non moléculaire, par exemple FeS, ne décrivent pas la composition de la molécule ; mais montrez seulement le rapport des éléments qui forment une substance donnée.
Ainsi, le réseau cristallin du sel de table est chlorure de sodium n'est pas constitué de molécules, mais de . Pour chaque ion sodium chargé positivement, il existe un ion chlorure chargé négativement. Il s'avère que le rapport des indices dans l'enregistrement NaCl coïncide avec la relation ; dans lequel des éléments chimiques se combinent les uns avec les autres pour former une substance. En ce qui concerne les substances qui ont une structure non moléculaire, il est plus correct d'appeler une telle entrée non pas une formule, mais unité de formule.