Les synapses sont des structures de communication formées par la terminaison d'une fibre nerveuse et la membrane des fibres musculaires adjacentes (nerf présynaptique et membranes musculaires postsynaptiques).
La transmission neuromusculaire se déroule en deux étapes : la première au niveau de l'axone, la seconde au niveau de la membrane synaptique (Fig. 6).
Sur le site des terminaisons axonales, trois processus séquentiels se produisent.
- 1. Synthèse de l'acétylcholine à partir de l'acétate avec formation d'acétylcoenzyme A avant le transfert du groupe acétate en choline sous l'action de la choline acétylase.
- 2. L'accumulation d'acétylcholine dans les vésicules synaptiques se produit probablement de trois manières différentes. Les vésicules situées plus près de la membrane synaptique contiennent apparemment des quanta utilisables immédiatement ou constituant une réserve fonctionnelle. Dans les vésicules synaptiques restantes, les quanta accumulés sont mobilisés, probablement après épuisement de la réserve fonctionnelle. Enfin, l'excès d'acétylcholine non utilisé par la stimulation nerveuse assure le réapprovisionnement des vésicules synaptiques.
- 3. La libération d'acétylcholine résulte de la rupture de certaines vésicules synaptiques sous l'influence d'un influx nerveux moteur. L'acétylcholine pénètre en quelques millisecondes à travers l'espace synaptique et se lie aux protéines réceptrices situées dans les vésicules de la membrane postsnaptique.
La deuxième étape se déroule au niveau de la membrane postsynaptique. Cette membrane, étant au repos, est polarisée du fait de la présence d'ions Na+ en surface et d'ions K+ en profondeur. Cet arrangement fournit un équilibre appelé potentiel de repos. La différence de potentiel entre les surfaces externe et interne de la membrane au repos est de 90 mV. L'entrée de l'acétylcholine dans les récepteurs modifie la perméabilité de la membrane aux ions, entraînant une modification de la répartition des ions des deux côtés de la membrane. Dans ce cas, Na+ pénètre intensément dans les profondeurs, et K, au contraire, se déplace vers la surface. L’équilibre électrique est perturbé, la membrane se dépolarise et le potentiel de repos devient le potentiel de la plaque terminale du nerf moteur. Si le potentiel nerveux moteur atteint un seuil de 30 mV, alors il se propage et provoque un relâchement musculaire dû à la dépolarisation.
Fig.6. Mécanisme de transmission neuromusculaire
Lorsqu’une impulsion nerveuse atteint la terminaison axonale, des canaux Ca2+ voltage-dépendants s’ouvrent sur la membrane présynaptique dépolarisée. L'entrée de Ca2+ dans l'extension axonale (membrane présynaptique) favorise la libération de neurotransmetteurs chimiques sous forme de vésicules (vésicules) depuis la terminaison axonale. Les médiateurs (dans la synapse neuromusculaire, il s'agit toujours de l'acétylcholine) sont synthétisés dans le soma de la cellule nerveuse et sont transportés par transport axonal jusqu'à l'extrémité de l'axone, où ils jouent leur rôle. L'émetteur diffuse à travers la fente synaptique et se lie à des récepteurs spécifiques sur la membrane post-synaptique. Le médiateur de la synapse neuromusculaire étant l’acétylcholine, les récepteurs de la membrane postsynaptique sont appelés récepteurs cholinergiques. À la suite de ce processus, des canaux Na+ chimiosensibles s'ouvrent sur la membrane postsynaptique, ce qui entraîne une dépolarisation dont l'ampleur est différente et dépend de la quantité de médiateur libéré. Le plus souvent, un processus local se produit, appelé potentiel de plaque d'extrémité (EPP). Avec une augmentation de la fréquence de stimulation de la fibre nerveuse, la dépolarisation de la membrane présynaptique augmente et, par conséquent, la quantité de médiateur libéré et le nombre de canaux Na+ chimiosensibles activés sur la membrane postsynaptique augmentent. Ainsi, des EPP apparaissent qui, en termes d'amplitude de dépolarisation, se résument à un niveau seuil, après quoi, sur la membrane des fibres musculaires entourant la synapse, un AP apparaît, qui a la capacité de se propager le long de la membrane des fibres musculaires. La sensibilité de la membrane postsynaptique est régulée par l'activité de l'enzyme acétylcholinestérase (ACCh-E), qui hydrolyse l'émetteur ACh en ses composants constitutifs (acétyle et choline) et le renvoie à la plaque présynaptique pour la resynthèse. Sans retrait de l'émetteur, une dépolarisation à long terme se développe sur la membrane postsynaptique, ce qui entraîne une perturbation de la conduction de l'excitation dans la synapse - dépression synaptique. Ainsi, la connexion synaptique assure la transmission unilatérale de l'excitation du nerf au muscle, mais tous ces processus prennent du temps (délai synaptique), ce qui conduit à une faible labilité de la synapse par rapport à la fibre nerveuse.
Ainsi, la synapse neuromusculaire est un endroit « avantageux » où des médicaments pharmacologiques peuvent être appliqués, modifiant la sensibilité du récepteur et l’activité enzymatique. Ces phénomènes se produiront souvent dans le cabinet médical : par exemple, en cas d'intoxication à la toxine botulique, la libération du médiateur ACH est bloquée (lissage des rides en médecine esthétique), le blocage des récepteurs cholinergiques (médicaments de type curare, bungarotoxine) perturbe la ouverture des canaux Na+ sur la membrane postsynaptique. Les composés organophosphorés (de nombreux insecticides) interfèrent avec l'efficacité de l'ACh-E et provoquent une dépolarisation à long terme de la membrane postsynaptique. En clinique, des bloqueurs neuromusculaires spécifiques sont utilisés : blocage des récepteurs cholinergiques avec des médicaments de type curare, de la succinylcholine et d'autres inhibiteurs compétitifs qui déplacent l'ACh du récepteur cholinergique. Dans la myasthénie grave, en raison d'un déficit des récepteurs cholinergiques de la membrane postsynaptique (en raison de leur destruction autolytique), une faiblesse musculaire progressive apparaît, pouvant aller jusqu'à l'arrêt complet des contractions musculaires (arrêt respiratoire). Dans ce cas, des bloqueurs de l'ACh-E sont utilisés, ce qui entraîne une augmentation de la durée de liaison du médiateur à moins de récepteurs cholinergiques et augmente légèrement l'amplitude de dépolarisation de la membrane postsynaptique.
La stimulation des récepteurs provoque la transformation de l'énergie d'influence du stimulus en influx nerveux, dont la transmission dans le système nerveux s'effectue à l'aide synapses.
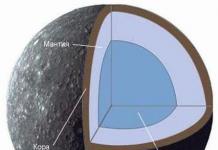
Structures fonctionnelles de la membrane cellulaire. La membrane cellulaire (membrane cellulaire) est une fine plaque lipoprotéique, la teneur en lipides est d'environ 40 %, la teneur en protéines est de 60 %. Schématiquement, une membrane cellulaire peut être représentée comme suit : la membrane est constituée d'une double couche de molécules phospholipidiques, recouverte à l'intérieur d'une couche de molécules protéiques, et à l'extérieur d'une couche de molécules glucidiques complexes. La membrane cellulaire contient des tubules très fins - les canaux ioniques, avoir de la sélectivité. Il existe des canaux qui ne laissent passer qu'un seul ion (sodium, potassium, calcium, chlore) ou plusieurs.
Potentiel de repos et potentiel d’action. Au repos dans le protoplasme d'une cellule nerveuse, la concentration en ions potassium est plus de 30 fois supérieure à la concentration de ces ions dans la solution externe. La membrane est pratiquement imperméable au sodium, tandis que le potassium la traverse. La diffusion des ions potassium du protoplasme vers le liquide externe est très élevée, ce qui confère à la membrane externe une charge positive et à la membrane interne une charge négative. Ainsi, la concentration en ions potassium est le principal facteur qui forme et détermine la valeur potentiel de repos(PP).
Lorsqu'une cellule est exposée à une irritation, la perméabilité de la membrane aux ions sodium augmente fortement et devient environ 10 fois supérieure à la perméabilité aux ions potassium. Par conséquent, le flux d'ions potassium chargés positivement du protoplasme vers la solution externe diminue et le flux d'ions sodium chargés positivement de la solution externe vers le protoplasme de la cellule augmente. Cela mène à recharger membranes, la surface externe se charge électronégativement et la surface interne devient chargée positivement ( phase de dépolarisation).
L’augmentation de la perméabilité de la membrane aux ions sodium dure très peu de temps. Suite à cela, des processus de réduction se produisent dans la cellule, conduisant au fait que la perméabilité aux ions sodium diminue à nouveau et que sa perméabilité aux ions potassium augmente. Et à la suite de ces deux processus, la membrane externe acquiert à nouveau une charge positive et la membrane interne acquiert une charge négative ( phase de repolarisation).
Une augmentation instantanée de la perméabilité aux ions sodium et leur pénétration dans la cellule suffit à changer le signe du potentiel membranaire et se produit potentiel d'action (PA), qui se propage le long de l'axone à une vitesse assez élevée, la durée du PA est généralement de 1 à 3 ms.
Transmission synaptique d'informations. L'endroit où l'excitation est transférée d'un neurone à un autre est appelé synapse(traduit du grec - contact). Une synapse est constituée des membranes de deux neurones voisins ( membranes présynaptiques et post-synaptiques) et l'espace entre eux, appelé fente synaptique.
Il existe des synapses axo-somatiques, formées par les membranes de l'axone et le corps (soma) d'un autre neurone, axo-dendritique, constituées de la membrane de l'axone et des dendrites d'un autre neurone, axo-axonal, dans lesquelles l'axone se rapproche de l'axone d'un autre neurone. La synapse entre les axones et les fibres musculaires s'appelle plaque neuromusculaire.
L'influx nerveux le long de l'axone atteint l'extrémité de l'axone et provoque l'ouverture des canaux calciques sur la membrane présynaptique. Ici, sur la membrane présynaptique se trouvent vésicules(bulles) contenant des substances biologiquement actives - médiateurs.
L'ouverture des canaux calciques entraîne dépolarisation sur la membrane présynaptique. Le calcium se lie aux protéines qui forment la membrane des vésicules dans lesquelles le médiateur est stocké. Ensuite, les vésicules éclatent et tout leur contenu pénètre dans la fente synaptique. Ensuite, les molécules médiatrices se lient à des molécules protéiques spéciales ( récepteurs), qui sont situés sur la membrane d'un autre neurone - sur la membrane post-synaptique.
Lorsque les molécules émettrices se lient aux récepteurs, des canaux pour les ions sodium et potassium s'ouvrent sur la membrane postsynaptique, provoquant un changement de potentiel (dépolarisation). Ce potentiel est appelé - potentiel post-synaptique (PSP). Selon la nature des canaux ioniques ouverts, des potentiels post-synaptiques excitateurs (EPSP) ou inhibiteurs (IPSP) apparaissent.
Ainsi, l'excitation (AP) d'un neurone au niveau de la synapse passe d'une impulsion électrique à une impulsion chimique (libération d'un émetteur depuis les vésicules).
Le temps entre le début de la dépolarisation présynaptique et la réponse postsynaptique est de 0,5 ms, c'est-à-dire retard synaptique.
Principaux médiateurs : acétylcholine, monoamines (sérotonine, histamine), catécholamines (dopamine, noradrénaline, adrénaline), acides aminés (glutamate, glycine, aspartate, acide gamma-aminobutyrique - GABA, alanine), peptides, vasopressine, ocytocine, adénosine, ATP, etc.
Moelle épinière
Moelle épinière, en apparence, il s'agit d'un long brin cylindrique, aplati d'avant en arrière. À cet égard, le diamètre transversal de la moelle épinière est plus grand que celui antéropostérieur.
La moelle épinière est située dans le canal rachidien et passe dans le cerveau au niveau du bord inférieur du foramen magnum. À cet endroit, des racines émergent de la moelle épinière (son bord supérieur), formant les nerfs spinaux droit et gauche. Le bord inférieur de la moelle épinière correspond au niveau de 1 à 11 vertèbres lombaires. En dessous de ce niveau, le sommet du cône médullaire de la moelle épinière se prolonge par un mince filum terminal. Le filum terminale dans ses parties supérieures contient encore du tissu nerveux et constitue un rudiment de l'extrémité caudale de la moelle épinière. Cette partie du filum terminal, appelée interne, est entourée par les racines des nerfs spinaux lombaires et sacrés et, avec elles, se situe dans un sac borgne formé par la dure-mère de la moelle épinière. Chez un adulte, la partie interne du filum terminale a une longueur d'environ 15 cm. Au-dessous du niveau de la 2e vertèbre sacrée, le filum terminale est une formation de tissu conjonctif qui prolonge les trois membranes de la moelle épinière et est appelée la partie externe du filum terminale. La longueur de cette partie est d'environ 8 cm et se termine au niveau du corps de la 2ème vertèbre coccygienne, fusionnée avec son périoste.
La longueur de la moelle épinière chez un adulte est en moyenne de 43 cm (chez les hommes 45 cm, chez les femmes 41-42 cm), le poids - environ 34-38 g, soit environ 2% de la masse du cerveau.
Dans les régions cervicale et lombo-sacrée de la moelle épinière, on retrouve deux épaississements notables : l'épaississement cervical et l'épaississement lombo-sacré. La formation d'épaississements s'explique par le fait que les membres supérieurs et inférieurs sont innervés respectivement par les parties cervicale et lombo-sacrée de la moelle épinière. Dans ces sections de la moelle épinière, il y a un plus grand nombre de cellules nerveuses et de fibres que dans les autres sections. Dans les parties inférieures, la moelle épinière se rétrécit progressivement et forme le cône médullaire.
Sur la surface antérieure de la moelle épinière, la fissure médiane antérieure est visible, qui fait saillie dans le tissu de la moelle épinière plus profondément que la barbe médiane postérieure. Ces rainures constituent les limites qui divisent la moelle épinière en deux moitiés symétriques. Dans les profondeurs du sillon médian postérieur se trouve un septum médian postérieur glial pénétrant presque toute l'épaisseur de la substance blanche. Ce septum s'étend jusqu'à la surface postérieure de la matière grise de la moelle épinière.
Sur la face antérieure de la moelle épinière, de chaque côté de la fissure antérieure, court la barbe antérolatérale. C'est le site de sortie de la moelle épinière des racines antérieures (motrices) des nerfs spinaux et la limite à la surface de la moelle épinière entre les moelles antérieure et latérale. Sur la surface postérieure de chaque moitié de la moelle épinière se trouve un sillon postérolatéral, site de pénétration des racines sensorielles postérieures des nerfs spinaux dans la moelle épinière. Cette rainure sert de limite entre les funicules latéraux et postérieurs.
Le cortex antérieur est constitué de processus de cellules nerveuses motrices (motrices) situées dans la corne antérieure de la matière grise de la moelle épinière. La racine dorsale est sensible, représentée par un ensemble de processus centraux de cellules pseudounipolaires pénétrant dans la moelle épinière, dont les corps forment le ganglion spinal, qui se trouve à la jonction de la racine dorsale avec la racine antérieure. Sur toute la longueur de la moelle épinière, 31 paires de racines émergent de chaque côté. Les racines antérieures et postérieures situées au bord interne du foramen intervertébral se rejoignent, fusionnent et forment le nerf spinal. Ainsi, 31 paires de nerfs spinaux sont formées à partir des racines. La section de la moelle épinière correspondant à deux paires de racines (deux antérieures et deux postérieures) est appelée segmenton.
Il est très important pour un médecin de connaître les relations topographiques des segments de la moelle épinière avec la colonne vertébrale (squelette des segments). La longueur de la moelle épinière est nettement inférieure à la longueur de la colonne vertébrale, donc le numéro de série de tout segment de la moelle épinière et le niveau de sa position, à partir de la région cervicale inférieure, ne correspondent pas au numéro de série de la vertèbre du même nom. La position des segments par rapport aux vertèbres peut être déterminée de la manière suivante. Les segments cervicaux supérieurs sont situés au niveau des corps vertébraux correspondant à leur numéro d'ordre. Les segments cervicaux inférieurs et thoraciques supérieurs se situent une vertèbre plus haut que les corps des vertèbres correspondantes. Dans la région thoracique moyenne, cette différence entre le segment correspondant de la moelle épinière et le corps vertébral augmente de 2 vertèbres, dans la région thoracique inférieure - de 3. Les segments lombaires de la moelle épinière se situent dans le canal rachidien au niveau de les corps des 10e, 11e vertèbres thoraciques, les segments sacrés et coccygiens - par niveau de 12 vertèbres thoraciques et 1 vertèbre lombaire.
La moelle épinière est constituée de cellules nerveuses et de fibres de matière grise qui, en coupe transversale, ressemblent à la lettre B ou à un papillon aux ailes déployées. Au-delà de la périphérie de la matière grise se trouve la substance blanche, formée uniquement de fibres nerveuses.
La matière grise de la moelle épinière contient un canal central. C'est un vestige de la cavité du tube neural et contient du liquide céphalo-rachidien. L'extrémité supérieure du canal communique avec le 9ème ventricule et l'extrémité inférieure, légèrement en expansion, forme un ventricule terminal aveuglément terminé. Les parois du canal central de la moelle épinière sont tapissées d'épendyme, autour duquel se trouve une substance centrale gélatineuse (grise). Chez un adulte, le canal central est envahi par diverses parties de la moelle épinière, et parfois sur toute sa longueur.
La matière grise le long de la moelle épinière à droite et à gauche du canal central forme des colonnes grises symétriques. Antérieures et postérieures au canal central de la moelle épinière, ces colonnes grises sont reliées entre elles par de fines plaques de matière grise, appelées commissures antérieure et postérieure.
Dans chaque colonne de matière grise, on distingue sa partie antérieure - la colonne antérieure et sa partie postérieure - la colonne postérieure. Derrière le niveau du col inférieur, se trouvent tous les segments thoraciques et les deux segments lombaires supérieurs de la moelle épinière.
La matière grise de chaque côté forme une saillie latérale – une colonne latérale. Dans d'autres parties de la moelle épinière (au-dessus du 8ème segment cervical et en dessous du 2ème segment lombaire), il n'y a pas de colonnes latérales.
Derrière la section transversale de la moelle épinière, les colonnes de matière grise de chaque côté ont l'apparence de cornes. Il existe une corne antérieure plus large et une corne postérieure étroite1, correspondant aux colonnes antérieure et postérieure. La corne latérale correspond à la colonne intermédiaire latérale (autonome) de matière grise.
Les cornes antérieures contiennent de grosses cellules de racines nerveuses - des neurones moteurs (efférents). Ces neurones forment 5 noyaux : deux latéraux (antérolatéral et postérolatéral), deux médiaux (antéromédial et postéromédial) et un noyau central. Les cornes postérieures de la moelle épinière sont représentées majoritairement par des cellules plus petites. Les racines dorsales ou sensorielles contiennent des processus centraux de cellules pseudounipolaires situées dans les ganglions spinaux (sensibles).
La matière grise des cornes dorsales de la moelle épinière est hétérogène. La majeure partie des cellules nerveuses de la corne dorsale forment son propre noyau. Dans la substance blanche immédiatement adjacente au sommet de la corne postérieure de la substance grise, on distingue une zone frontalière. En avant de cette dernière dans la substance grise se trouve une zone spongieuse, qui doit son nom à la présence dans cette section d'un réseau glial à grande boucle contenant des cellules nerveuses. Une substance gélatineuse constituée de petites cellules nerveuses est sécrétée encore plus en avant. Les processus des cellules nerveuses de la substance gélatineuse, la zone spongieuse et les cellules en touffes dispersées de manière diffuse dans la matière grise communiquent avec plusieurs segments voisins. En règle générale, ils se terminent par des synapses avec des neurones situés dans les cornes antérieures de leur segment, ainsi qu'au-dessus et en dessous des segments. Dirigés des cornes postérieures de la matière grise vers les cornes antérieures, les processus de ces cellules sont situés le long de la périphérie de la matière grise, formant une étroite bordure de matière blanche à proximité. Ces faisceaux de fibres nerveuses sont appelés faisceaux intrinsèques antérieur, latéral et postérieur. Les cellules de tous les noyaux des cornes dorsales de la matière grise sont, en règle générale, des neurones intercalaires (intermédiaires ou conducteurs). Les neurites s'étendant des cellules nerveuses, dont l'ensemble constitue les noyaux central et thoracique des cornes dorsales, sont dirigés dans la substance blanche de la moelle épinière vers le cerveau.
La zone intermédiaire de matière grise de la moelle épinière est située entre les cornes antérieure et postérieure. Ici, du 8ème segment cervical au 2ème segment lombaire, il y a une saillie de matière grise - la corne latérale.
Dans la partie médiale de la base de la corne latérale, on remarque un noyau difficile constitué de grosses cellules nerveuses, bien délimité par une couche de matière blanche. Ce noyau s'étend sur toute la colonne postérieure de matière grise sous la forme d'un cordon cellulaire (noyau de Clark). Le plus grand diamètre de ce noyau se situe au niveau de 11 segments thoraciques à 1 segment lombaire. Les cornes latérales contiennent les centres de la partie sympathique du système nerveux autonome sous la forme de plusieurs groupes de petites cellules nerveuses réunies dans la substance intermédiaire latérale (grise). Les axones de ces cellules traversent la corne antérieure et sortent de la moelle épinière en tant que partie intégrante des racines ventrales.
Dans la zone intermédiaire se trouve une substance intermédiaire centrale (grise), dont les processus cellulaires participent à la formation du tractus spinocérébelleux. Au niveau des segments cervicaux de la moelle épinière, entre les cornes antérieure et postérieure, et au niveau des segments thoraciques supérieurs, entre les cornes latérales et postérieures, une formation réticulaire est localisée dans la substance blanche adjacente à la substance grise. . La formation réticulaire ressemble ici à de fines barres de matière grise se croisant dans différentes directions et se compose de cellules nerveuses dotées d'un grand nombre de processus.
La matière grise de la moelle épinière avec les racines postérieures et antérieures des nerfs spinaux et ses propres faisceaux de matière blanche bordant la matière grise forme son propre appareil, ou segmentaire, de la moelle épinière. L'objectif principal de l'appareil segmentaire, en tant que partie phylogénétiquement la plus ancienne de la moelle épinière, est de réaliser des réactions innées (réflexes) en réponse à une stimulation (interne ou externe). I. P. Pavlov a défini ce type d'activité de l'appareil segmentaire de la moelle épinière par le terme « réflexes inconditionnés ».
La matière blanche, comme indiqué, est localisée à l’extérieur de la matière grise. Les sillons de la moelle épinière divisent la substance blanche en trois cordons situés symétriquement à droite et à gauche. La moelle antérieure est située entre la fissure médiane antérieure et le sillon latéral antérieur. Dans la substance blanche postérieure à la fissure médiane antérieure, on distingue la commissure blanche antérieure, qui relie les cordons antérieurs des côtés droit et gauche. Le funicule postérieur est situé entre les sillons médians postérieurs et latéraux postérieurs. Le funicule latéral est la zone de substance blanche située entre les sillons latéraux antérieur et postérieur.
Mécanismes d'interaction entre les cellules nerveuses
Les cellules nerveuses fonctionnent en étroite coopération les unes avec les autres.
La signification de l'influx nerveux. Toutes les interactions entre les cellules nerveuses s'effectuent en raison de deux mécanismes : 1) l'influence des champs électriques des cellules nerveuses (influences électrotoniques) et 2) l'influence de l'influx nerveux.
Les premiers se propagent à de très petites zones du cerveau. La charge électrique d'une cellule nerveuse crée un champ électrique autour d'elle, dont les oscillations provoquent des modifications des champs électriques des neurones voisins, ce qui entraîne des modifications de leur excitabilité, de leur labilité et de leur conductivité. . Le champ électrique d'un neurone a une étendue relativement petite - environ 100 microns ; il décroît rapidement à mesure qu'il s'éloigne de la cellule et ne peut affecter que les neurones voisins.
Le deuxième mécanisme permet non seulement des interactions immédiates, mais également la transmission d'influences neuronales sur de longues distances. C'est à l'aide de l'influx nerveux que les zones éloignées et isolées du cerveau sont unies en un système commun fonctionnant de manière synchrone, nécessaire aux formes complexes d'activité corporelle. L’influx nerveux est donc le principal moyen de communication entre les neurones. La vitesse élevée de propagation des impulsions et leur impact local sur un point sélectionné du cerveau contribuent à la transmission rapide et précise des informations dans le système nerveux. Dans les interactions interneurones, un code de fréquence est utilisé, c'est-à-dire que les changements dans l'état fonctionnel et la nature des réponses d'une cellule nerveuse sont codés par des changements dans la fréquence des impulsions (potentiels d'action) qu'elle envoie à une autre cellule nerveuse. Le nombre total d'impulsions envoyées par une cellule nerveuse par unité de temps, ou son activité impulsionnelle totale, est un indicateur physiologique important de l'activité d'un neurone.
Les principaux éléments d'une synapse chimique : fente synaptique, vésicules (vésicules synaptiques), neurotransmetteurs, récepteurs.
Synapse(grec σύναψις, de συνάπτειν - étreinte, serrer, serrer la main) - le lieu de contact entre deux neurones ou entre un neurone et la cellule effectrice recevant le signal. Il sert à transmettre un influx nerveux entre deux cellules, et lors de la transmission synaptique, l'amplitude et la fréquence du signal peuvent être ajustées. La transmission des impulsions s'effectue chimiquement à l'aide de médiateurs ou électriquement par le passage d'ions d'une cellule à l'autre.
Le terme a été introduit en 1897 par le physiologiste anglais Charles Sherrington. Cependant, Sherrington lui-même a affirmé avoir reçu l'idée du terme lors d'une conversation avec le physiologiste Michael Foster.
Classifications des synapses

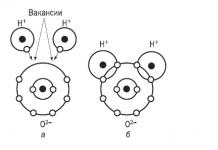
Les principaux éléments d'une synapse électrique (ephaps) : a - connexion à l'état fermé ; b - connexion à l'état ouvert ; c - connexon intégré dans la membrane ; d - monomère de connexine, e - membrane plasmique ; f - espace intercellulaire ; g - un espace de 2 à 4 nanomètres dans la synapse électrique ; h - canal de connexion hydrophile.
Selon le mécanisme de transmission de l'influx nerveux
produit chimique est un lieu de contact étroit entre deux cellules nerveuses, pour la transmission d'un influx nerveux à travers lequel la cellule source libère dans l'espace intercellulaire une substance spéciale, un neurotransmetteur, dont la présence dans la fente synaptique excite ou inhibe la cellule réceptrice .
électrique (ephaps) - un lieu de contact plus étroit entre une paire de cellules, où leurs membranes sont reliées à l'aide de formations protéiques spéciales - les connexons (chaque connexon est constitué de six sous-unités protéiques). La distance entre les membranes cellulaires de la synapse électrique est de 3,5 nm (la distance intercellulaire habituelle est de 20 nm). La résistance du liquide extracellulaire étant faible (dans ce cas), les impulsions traversent la synapse sans délai. Les synapses électriques sont généralement excitatrices.
synapses mixtes - Le potentiel d'action présynaptique produit un courant qui dépolarise la membrane postsynaptique d'une synapse chimique typique où les membranes pré- et post-synaptiques ne sont pas étroitement adjacentes les unes aux autres. Ainsi, au niveau de ces synapses, la transmission chimique constitue un mécanisme de renforcement nécessaire.
Les synapses chimiques sont les plus courantes. Les synapses électriques sont moins courantes dans le système nerveux des mammifères que les synapses chimiques.
Par localisation et affiliation aux structures modifier le texte wiki]
neuromusculaire
neurosécrétoire (axo-vasal)
récepteur-neuronal
axo-dendritique- avec des dendrites, dont
axo-épineux- avec des épines dendritiques, des excroissances sur les dendrites ;
périphérique
central
axo-somatique- avec les corps des neurones ;
axo-axonal- entre les axones ;
dendro-dendritique- entre les dendrites ;

Divers emplacements des synapses chimiques
Par neurotransmetteur
y compris les adrénergiques contenant de l'adrénaline ou de la noradrénaline ;
aminergique, contenant des amines biogènes (par exemple, sérotonine, dopamine) ;
cholinergique, contenant de l'acétylcholine;
purinergique, contenant des purines;
peptidergique, contenant des peptides.
Dans le même temps, un seul émetteur n'est pas toujours produit au niveau de la synapse. Habituellement, le médiator principal est libéré avec un autre qui joue le rôle de modulateur.
Par signe d'action
stimulant
frein.
Si les premiers contribuent à l'apparition d'une excitation dans la cellule postsynaptique (dans celles-ci, à la suite de l'arrivée d'une impulsion, se produit une dépolarisation de la membrane, qui peut provoquer un potentiel d'action dans certaines conditions), alors les seconds, sur le au contraire, arrêter ou empêcher son apparition et empêcher la propagation ultérieure de l’impulsion. Les synapses glycinergiques (médiateur - glycine) et GABAergiques (médiateur - acide gamma-aminobutyrique) sont généralement inhibitrices.
Les synapses inhibitrices sont de deux types : 1) une synapse, dans les terminaisons présynaptiques de laquelle est libéré un émetteur, hyperpolarisant la membrane postsynaptique et provoquant l'apparition d'un potentiel postsynaptique inhibiteur ; 2) synapse axo-axonale, assurant l'inhibition présynaptique. Synapse cholinergique (s. cholinergica) - une synapse dans laquelle l'acétylcholine est le médiateur.
Présent sur certaines synapses condensation post-synaptique- zone dense aux électrons constituée de protéines. En fonction de leur présence ou de leur absence, les synapses sont distinguées asymétrique Et symétrique. On sait que toutes les synapses glutamatergiques sont asymétriques et que les synapses GABAergiques sont symétriques.
Dans les cas où plusieurs extensions synaptiques sont en contact avec la membrane postsynaptique, plusieurs synapses.
Les formes spéciales de synapses comprennent appareil épineux, dans lequel de courtes saillies simples ou multiples de la membrane postsynaptique de la dendrite entrent en contact avec l'extension synaptique. Les appareils de la colonne vertébrale augmentent considérablement le nombre de contacts synaptiques sur un neurone et, par conséquent, la quantité d'informations traitées. Les synapses non vertébrales sont appelées synapses sessiles. Par exemple, toutes les synapses GABAergiques sont sessiles.
Potentiel d'action ou influx nerveux, une réponse spécifique qui se produit sous la forme d'une onde excitatrice et s'écoule tout au long du trajet nerveux. Cette réaction est une réponse à un stimulus. La tâche principale est de transmettre les données du récepteur au système nerveux, puis de diriger ces informations vers les muscles, les glandes et les tissus souhaités. Après le passage de l’impulsion, la partie superficielle de la membrane devient chargée négativement, tandis que sa partie interne reste positive. Ainsi, une impulsion nerveuse est un changement électrique transmis séquentiellement.
L'effet excitant et sa répartition dépendent de la nature physico-chimique. L’énergie nécessaire à ce processus est générée directement dans le nerf lui-même. Cela est dû au fait que le passage d'une impulsion entraîne la formation de chaleur. Une fois passé, l'état d'atténuation ou de référence commence. Pendant seulement une fraction de seconde, le nerf ne peut pas conduire un stimulus. La vitesse à laquelle l'impulsion peut être délivrée varie de 3 m/s à 120 m/s.
Les fibres traversées par l'excitation possèdent une gaine spécifique. Grosso modo, ce système ressemble à un câble électrique. La composition de la membrane peut être de la myéline ou non. Le composant le plus important de la gaine de myéline est la myéline, qui joue le rôle de diélectrique.
La vitesse de l'impulsion dépend de plusieurs facteurs, par exemple de l'épaisseur des fibres : plus elle est épaisse, plus la vitesse se développe rapidement. Un autre facteur augmentant la vitesse de conduction est la myéline elle-même. Mais en même temps, il n'est pas localisé sur toute la surface, mais par sections, comme enchaînées. Ainsi, entre ces zones, il y a celles qui restent « nues ». Ils provoquent une fuite de courant de l’axone.
Un axone est un processus utilisé pour transmettre des données d’une cellule aux autres. Ce processus est régulé par une synapse – une connexion directe entre les neurones ou un neurone et une cellule. Il existe également ce qu'on appelle un espace synaptique ou fente. Lorsqu’une impulsion irritante arrive sur un neurone, des neurotransmetteurs (molécules d’une composition chimique) sont libérés lors de la réaction. Ils traversent l’ouverture synaptique pour finalement atteindre les récepteurs du neurone ou de la cellule vers lesquels les données doivent être transmises. Les ions calcium sont nécessaires à la conduction de l'influx nerveux, car sans cela, le neurotransmetteur ne peut pas être libéré.
Le système autonome est assuré principalement par des tissus non myélinisés. L’excitation se propage à travers eux constamment et continuellement.
Le principe de transmission est basé sur l'apparition d'un champ électrique, de sorte qu'un potentiel apparaît qui irrite la membrane de la section adjacente et ainsi de suite dans toute la fibre.
Dans ce cas, le potentiel d'action ne bouge pas, mais apparaît et disparaît au même endroit. La vitesse de transmission à travers ces fibres est de 1 à 2 m/s. 
Lois de conduite
Il existe quatre lois fondamentales en médecine :
- Valeur anatomique et physiologique. L'excitation n'est effectuée que s'il n'y a pas de violation de l'intégrité de la fibre elle-même. Si l'unité n'est pas assurée, par exemple en raison d'une infraction ou d'une consommation de drogue, alors la conduction de l'influx nerveux est impossible.
- Conduction isolée de l'irritation. L'excitation peut être transmise le long de la fibre nerveuse, sans se propager aux fibres voisines.
- Conduction bilatérale. Le chemin de conduction des impulsions ne peut être que de deux types : centrifuge et centripète. Mais en réalité, la direction se produit dans l'une des options.
- Implémentation non décrémentale. Les impulsions ne s'apaisent pas, c'est-à-dire qu'elles s'exécutent sans décrémentation.
Chimie de la conduction des impulsions
Le processus d’irritation est également contrôlé par les ions, principalement le potassium, le sodium et certains composés organiques. La concentration de ces substances est différente, la cellule est chargée négativement à l'intérieur d'elle-même et positivement à la surface. Ce processus sera appelé différence de potentiel. Lorsqu'une charge négative oscille, par exemple lorsqu'elle diminue, une différence de potentiel est provoquée et ce processus est appelé dépolarisation.

La stimulation d'un neurone entraîne l'ouverture de canaux sodiques au site de stimulation. Cela peut faciliter l’entrée de particules chargées positivement dans la cellule. En conséquence, la charge négative est réduite et un potentiel d'action ou une impulsion nerveuse apparaît. Après cela, les canaux sodiques se referment.
On constate souvent que c'est l'affaiblissement de la polarisation qui favorise l'ouverture des canaux potassiques, ce qui provoque la libération d'ions potassium chargés positivement. Cette action réduit la charge négative à la surface des cellules.
Le potentiel de repos ou l'état électrochimique est restauré lorsque les pompes potassium-sodium sont activées, à l'aide desquelles les ions sodium quittent la cellule et les ions potassium y pénètrent.
En conséquence, nous pouvons dire que lorsque les processus électrochimiques reprennent, des impulsions se produisent qui se propagent le long des fibres.
Sensibilité extéroceptive
Premier neurone
Les impulsions de tous les récepteurs périphériques pénètrent dans la moelle épinière par la racine dorsale, qui est constituée d'un grand nombre de fibres qui sont les axones des cellules pseudounipolaires du ganglion intervertébral (spinal). Le but de ces fibres est différent.
Certains d'entre eux, pénétrant dans la corne postérieure, traversent le diamètre de la moelle épinière jusqu'aux cellules de la corne antérieure (le premier motoneurone), agissant ainsi comme la partie afférente de l'arc réflexe spinal des réflexes cutanés.
Deuxième neurone
Une autre partie des fibres se termine dans les cellules de la colonne de Clarke, d'où le deuxième neurone se dirige vers les sections dorsales des colonnes latérales de la moelle épinière appelées fascicule dorsal spinocérébelleux de Flexig. Le troisième groupe de fibres se termine au niveau des cellules de la substance gélatineuse de la corne dorsale. De là, les seconds neurones, formant le tractus spinothalamique, font une transition devant le canal central de la moelle épinière dans la commissure grise antérieure vers le côté opposé et le long des colonnes latérales, puis, dans le cadre de la boucle médiale, atteindre le thalamus visuel.
Troisième neurone
Le troisième neurone va du thalamus optique en passant par la cuisse postérieure de la capsule interne jusqu'à l'extrémité corticale de l'analyseur cutané (gyrus central postérieur). La douleur et la température extéroceptives, ainsi que des stimuli en partie tactiles, sont transmis le long de cette voie. Cela signifie que la sensibilité extéroceptive de la moitié gauche du corps s'effectue le long de la moitié droite de la moelle épinière et de la moitié droite - le long de la gauche.
Sensibilité proprioceptive
Premier neurone
La sensibilité proprioceptive a des relations différentes. Associé à la transmission de ces irritations, le quatrième groupe de fibres de la racine dorsale, étant entré dans la moelle épinière, ne pénètre pas dans la matière grise de la corne dorsale, mais remonte directement le long des colonnes postérieures de la moelle épinière sous le nom de le fascicule doux (Gaull) et dans les régions cervicales - le fascicule en forme de coin (Burdach) . De courtes collatérales s'étendent à partir de ces fibres, qui se rapprochent des cellules des cornes antérieures, constituant ainsi la partie afférente des réflexes proprioceptifs de la colonne vertébrale. Les fibres les plus longues de la racine dorsale sous la forme du premier neurone (périphérique, s'étendant cependant sur une longue distance dans le système nerveux central - le long de la moelle épinière) s'étendent jusqu'aux parties inférieures de la moelle allongée, où elles se terminent par les cellules du noyau du faisceau de Gaulle et du noyau du faisceau de Burdach.
Deuxième neurone
Les axones de ces cellules, formant le deuxième neurone des conducteurs de la sensibilité proprioceptive, se déplacent bientôt de l'autre côté, occupant avec ce croisement la région interolive de la moelle allongée, appelée raphé. Après avoir fait la transition vers le côté opposé, ces conducteurs forment une boucle médiale, située d'abord dans la couche interolive de la moelle allongée, puis dans les parties dorsales du pont. Après avoir traversé les pédoncules cérébraux, ces fibres pénètrent dans le thalamus visuel, au niveau des cellules duquel se termine le deuxième neurone des conducteurs de la sensibilité proprioceptive.
Troisième neurone
Les cellules du thalamus optique constituent le début du troisième neurone, à travers lequel les stimuli sont transportés à travers la partie postérieure de la cuisse postérieure de la capsule interne jusqu'au gyrus central postérieur et en partie jusqu'au gyrus central antérieur (analyseurs moteurs et cutanés). Ici, dans les cellules du cortex, se produit l'analyse et la synthèse des irritations apportées, et nous ressentons le toucher, le mouvement et d'autres types d'irritations proprioceptives. Ainsi, la stimulation musculaire et en partie tactile de la moitié droite du corps se propage le long de la moitié droite de la moelle épinière, effectuant la transition vers le côté opposé uniquement dans la moelle allongée.