Эрчим хүч ялгарах замаар органик бодисыг энгийн бодис болгон задалж, ATP-д хадгалах нь энергийн солилцоо юм. Үүнд бэлтгэл, хүчилтөрөгчгүй, хүчилтөрөгч гэсэн гурван үе шат орно.
Бэлтгэл үе шатанд энерги ялгардаг ч ATP-д хадгалагдахгүй, харин дулаан хэлбэрээр тараагддаг.
Хүчилтөрөгчгүй үе шат нь цитоплазмд тохиолддог бөгөөд глюкозын молекул бүрийг пирувийн хүчлийн хоёр молекул болгон задлахад хүргэдэг. Энэ тохиолдолд бага хэмжээний энерги ялгардаг тул зөвхөн хоёр ATP молекул нийлэгждэг.
Эрчим хүчний солилцооны хүчилтөрөгчийн үе шат нь митохондрид тохиолддог. Энд пирувийн хүчлийг нүүрстөрөгчийн давхар исэл, ус болгон исэлдүүлж, их хэмжээний энерги ялгарч, 36 орчим ATP молекул нийлэгждэг.
Уургийн биосинтез ба өөхний нийлэгжилт нь энгийн нэгдлүүдээс илүү нарийн төвөгтэй бодисууд нийлэгждэг хуванцар бодисын солилцоог хэлдэг. Ийм үйл явц нь энерги ялгаруулж биш харин түүний хэрэглээтэй холбоотой байдаг. Энд ATP нь ADP болон фосфорын хүчилд задардаг эрчим хүчний нийлүүлэгчийн үүрэг гүйцэтгэдэг.
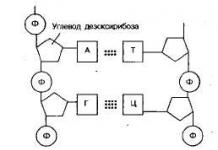
Биологийн хувьд ATP товчлол нь органик бодисыг (мономер) илэрхийлдэг. аденозин трифосфат(аденозин трифосфорын хүчил). Химийн бүтцийн хувьд энэ нь нуклеозид трифосфат юм.
ATP агуулдаг рибоз, аденин, гурван фосфорын хүчлийн үлдэгдэл. Фосфатууд бие биетэйгээ дараалан холбогддог. Түүгээр ч барахгүй сүүлийн хоёр нь өндөр энергитэй холбоо гэж нэрлэгддэг бөгөөд тасрах нь эсийг их хэмжээний эрчим хүчээр хангадаг.
Тиймээс ATP нь эсэд үйлчилдэг эрчим хүчний функц.
Ихэнх ATP молекулууд эсийн амьсгалын урвалын үед митохондрид үүсдэг. Эсэд олон тооны аденозин трифосфорын хүчлийн молекулууд байнга нийлэгжиж, задардаг.
Фосфатын бүлгийг зайлуулах нь гол төлөв ферментийн оролцоотойгоор явагддаг АТФазаба гидролизийн урвал (ус нэмэх):
ATP + H2O = ADP + H3PO4 + E,
Энд E нь эсийн янз бүрийн процесст ордог ялгарсан энерги (бусад органик бодисын нийлэгжилт, тэдгээрийн тээвэрлэлт, эрхтэн ба эсийн хөдөлгөөн, терморегуляция гэх мэт).
Төрөл бүрийн эх сурвалжаас харахад ялгарах энергийн хэмжээ 30-60 кЖ / моль хооронд хэлбэлздэг.
ADP нь аль хэдийн хоёр фосфорын хүчлийн үлдэгдэл агуулсан аденозин дифосфат юм.
Ихэнхдээ фосфатыг дахин нэмж ATP үүсгэдэг.
ADP + H3PO4 = ATP + H2O - E.
Энэ урвал нь энерги шингээх үед үүсдэг бөгөөд түүний хуримтлал нь хэд хэдэн ферментийн урвал ба ион дамжуулах үйл явцын үр дүнд үүсдэг (гол төлөв матриц ба митохондрийн дотоод мембран дээр). Эцсийн эцэст энерги нь ADP-тэй хавсарсан фосфатын бүлэгт хуримтлагддаг.
Гэсэн хэдий ч өндөр энергитэй холбоотой өөр нэг фосфат нь ADP-ээс салж, AMP (аденозин монофосфат) үүсдэг.
AMP нь РНХ-ийн нэг хэсэг юм. Тиймээс аденозин трифосфорын хүчлийн өөр нэг үүрэг бол олон тооны органик нэгдлүүдийг нийлэгжүүлэх түүхий эдийн эх үүсвэр болдог.
Тиймээс ATP-ийн бүтцийн онцлог, түүний функциональ хэрэглээ нь зөвхөн бодисын солилцооны үйл явцад эрчим хүчний эх үүсвэр болгон эсийг химийн энергийг хүлээн авах нэгдсэн, бүх нийтийн системтэй болгох боломжийг олгодог.
Холбоотой нийтлэл: Эрчим хүчний солилцооны үе шатууд
Фосфоржих үйл явц нь киназа ферментийн оролцоотойгоор фосфорилын бүлгийг нэг нэгдлээс нөгөөд шилжүүлэх урвал юм. ATP нь исэлдэлтийн болон субстратын фосфоржилтоор нийлэгждэг.
Исэлдэлтийн фосфоржилт нь биоорганик бодисын исэлдэлтийн явцад ялгарах энергийг ашиглан ADP-д органик бус фосфат нэмж ATP-ийн нийлэгжилтийг хэлнэ.
ADP + ~P → ATP
Нүүрс усны солилцооны завсрын бүтээгдэхүүн нь ADP фосфорилын бүлгийг өндөр энергитэй холбоогоор дамжуулдаг фосфоэнолпирувийн хүчил юм.
2.
Хоёр дахь үе шат. Тээвэрлэлтийн дараа мономерууд (биорганик нэгдлүүдийн задралын бүтээгдэхүүн) эсэд орж, исэлдэлтэнд ордог.
Түлшний молекулууд (амин хүчил, глюкоз, өөх тос) исэлдэлтийн үр дүнд ацетил-Ко-А нэгдэл үүсдэг. Энэ үе шатанд хүнсний бодисын энергийн 30 орчим хувь нь ялгардаг.
Гурав дахь үе шат - Кребсын мөчлөг нь биохимийн исэлдэлтийн урвалын хаалттай систем юм. Цикл нь аэробик исэлдэлтийн үндсэн урвалуудыг дэвшүүлж, туршилтаар баталсан Английн биохимич Ханс Кребсийн нэрээр нэрлэгдсэн юм. Судалгааныхаа төлөө Кребс Нобелийн шагнал хүртсэн (1953).
Цикл нь өөр хоёр нэртэй:



II.

Энэ үйл явц нь аконитаза ферментээр катализлагдсан шингэн алдалтын урвал юм.
Энэ үйл явц нь аконитаза ферментээр катализлагдсан чийгшүүлэх урвал юм.

IV.

4 ба 5-р урвалууд нь изоцитратдегидрогеназаар катализлагдсан исэлдэлтийн декарбоксилжилт, завсрын бүтээгдэхүүн болох оксалосукцинат юм.
Энэ урвал нь мөн исэлдэлтийн декарбоксилжих урвал, i.e. Энэ бол хоёр дахь исэлдэлтийн урвал юм:
α-оксоглутарат + NAD + CoA Сукцинил-КоА + CO2 + NADH


VII.
GTP + ADP ATP + ДНБ


X. Дөрөв дэх исэлдэлтийн урвал:

Циклийн дөрвөн урвал нь редокс бөгөөд ферментүүд - NAD ба FAD коэнзим агуулсан дегидрогеназаар катализ болдог. Коэнзимүүд үүссэн H+ ба ē-г барьж амьсгалын замын гинжин хэлхээнд (биологийн исэлдэлтийн гинж) шилжүүлдэг. Амьсгалын гинжин хэлхээний элементүүд нь митохондрийн дотоод мембран дээр байрладаг.
Амьсгалын гинж нь исэлдэлтийн урвалын систем бөгөөд энэ үед амьсгалын үр дүнд биед нэвтэрч буй H+ ба ē нь O2 руу аажмаар шилждэг.
ATP нь амьсгалын замын гинжин хэлхээнд үүсдэг. Гинжин дэх гол тээвэрлэгч ē нь төмөр, зэс агуулсан уураг (цитохром), коэнзим Q (ubiquinone) юм. Гинжинд 5 цитохром байдаг (b1, c1, c, a, a3).
b1, c1, c цитохромуудын протезийн бүлэг нь төмөр агуулсан гем юм. Эдгээр цитохромын үйл ажиллагааны механизм нь ē ба H+ шилжүүлгийн үр дүнд исэлдсэн болон бууруулсан төлөвт аль алинд нь байж болох хувьсах валент бүхий төмрийн атом агуулдаг.
Цитохром a, a3 нь амьсгалын замын гинжин хэлхээний сүүлчийн холбоос болох цитохром оксидазын цогцолборыг үүсгэдэг.
Цитохром оксидаз нь төмрөөс гадна хувьсах валенттай зэс агуулдаг. Цитохром a3-аас молекулын O2 руу ē-г зөөвөрлөхөд процесс явагдана
Өмнөх9101112131415161718192021222324Дараагийн
ДЭЛГЭРЭНГҮЙГ ҮЗЭХ:

Санал хүсэлт
Танин мэдэхүй
Хүсэл зориг нь үйлдэлд, эерэг үйлдэл нь эерэг хандлагыг бий болгодог.
Таны зорилго таныг үйлдэл хийхээс өмнө юу хүсч байгаагаа хэрхэн мэддэг.
Компаниуд дадал зуршлыг хэрхэн урьдчилан таамаглаж, түүнийг хэрхэн удирддаг
Эдгээх зуршил
Гомдолоос өөрийгөө хэрхэн ангижруулах вэ
Эрэгтэй хүний зан чанаруудын талаархи зөрчилдөөнтэй үзэл бодол
Өөртөө итгэх итгэлийн сургалт
"Сармистай манжингийн салат"
Натюрморт ба түүний дүрслэх боломжууд
Өргөдөл, мумио хэрхэн авах вэ? Шилажит үс, нүүр, хугарал, цус алдалт гэх мэт.
Хэрхэн хариуцлага хүлээж сурах вэ
Хүүхэдтэй харилцах харилцаанд яагаад хил хязгаар хэрэгтэй байдаг вэ?
Хүүхдийн хувцасны тусгал элементүүд
Насаа яаж давах вэ?
Урт наслахад туслах найман өвөрмөц арга
БЖИ-ээр таргалалтын ангилал (ДЭМБ)
Бүлэг 3. Эрэгтэй хүний эмэгтэй хүнтэй хийсэн гэрээ

Хүний биеийн тэнхлэг ба хавтгай - Хүний бие нь байр зүйн тодорхой хэсэг, эрхтэн, булчин, судас, мэдрэл гэх мэт хэсгүүдээс бүрддэг.
 Хана цүүцлэх, хаалт хайчлах - Байшинд цонх, хаалга хүрэлцэхгүй бол үзэсгэлэнтэй өндөр үүдний танхим зөвхөн төсөөлөлд л байдаг тул та гудамжнаас шатаар байшин руу авирах хэрэгтэй.
Хана цүүцлэх, хаалт хайчлах - Байшинд цонх, хаалга хүрэлцэхгүй бол үзэсгэлэнтэй өндөр үүдний танхим зөвхөн төсөөлөлд л байдаг тул та гудамжнаас шатаар байшин руу авирах хэрэгтэй.
 Хоёрдугаар эрэмбийн дифференциал тэгшитгэл (урьдчилан таамаглаж болох үнэ бүхий зах зээлийн загвар) - Зах зээлийн энгийн загварт эрэлт нийлүүлэлт нь зөвхөн тухайн бүтээгдэхүүний одоогийн үнээс хамаарна гэж үздэг.
Хоёрдугаар эрэмбийн дифференциал тэгшитгэл (урьдчилан таамаглаж болох үнэ бүхий зах зээлийн загвар) - Зах зээлийн энгийн загварт эрэлт нийлүүлэлт нь зөвхөн тухайн бүтээгдэхүүний одоогийн үнээс хамаарна гэж үздэг.
Бие дэх ATP синтезийн замууд
Фосфоржих үйл явц нь киназа ферментийн оролцоотойгоор фосфорилын бүлгийг нэг нэгдлээс нөгөөд шилжүүлэх урвал юм.
ATP нь исэлдэлтийн болон субстратын фосфоржилтоор нийлэгждэг. Исэлдэлтийн фосфоржилт нь биоорганик бодисын исэлдэлтийн явцад ялгарах энергийг ашиглан ADP-д органик бус фосфат нэмж ATP-ийн нийлэгжилтийг хэлнэ.
ADP + ~P → ATP
Субстратын фосфоржилт нь ATP-ийн нийлэгжилтэнд өндөр энергитэй ADP холбоо бүхий фосфорилын бүлгийг шууд шилжүүлэх явдал юм.
Субстратын фосфоржилтын жишээ:
1. Нүүрс усны солилцооны завсрын бүтээгдэхүүн нь фосфоэнолпирувийн хүчил бөгөөд ADP фосфорилын бүлгийг өндөр энергитэй холбоогоор дамжуулдаг.
 |
Кребсийн мөчлөгийн завсрын бүтээгдэхүүн болох өндөр энергитэй сукцинил-Ко-А-ийн ADP-тэй харилцан үйлчлэлцэж АТФ-ын нэг молекул үүсдэг.
Бие махбодид энерги ялгарах, ATP синтезийн үндсэн гурван үе шатыг авч үзье.
Эхний үе шатанд (бэлтгэл) хоол боловсруулах, шингээх үйл явц орно.
Энэ үе шатанд хүнсний нэгдлүүдийн энергийн 0.1% нь ялгардаг.
Хоёр дахь үе шат. Тээвэрлэлтийн дараа мономерууд (биорганик нэгдлүүдийн задралын бүтээгдэхүүн) эсэд орж, исэлдэлтэнд ордог. Түлшний молекулууд (амин хүчил, глюкоз, өөх тос) исэлдэлтийн үр дүнд ацетил-Ко-А нэгдэл үүсдэг. Энэ үе шатанд хүнсний бодисын энергийн 30 орчим хувь нь ялгардаг.
Гурав дахь үе шат - Кребсын мөчлөг нь биохимийн исэлдэлтийн урвалын хаалттай систем юм.
Цикл нь аэробик исэлдэлтийн үндсэн урвалуудыг дэвшүүлж, туршилтаар баталсан Английн биохимич Ханс Кребсийн нэрээр нэрлэгдсэн юм. Судалгааныхаа төлөө Кребс Нобелийн шагнал хүртсэн (1953). Цикл нь өөр хоёр нэртэй:
- трикарбоксилын хүчлийн мөчлөг, учир нь энэ нь трикарбоксилын хүчлийн хувирлын урвалыг агуулдаг (гурван карбоксилын бүлэг агуулсан хүчил);
- нимбэгийн хүчлийн мөчлөг, учир нь мөчлөгийн эхний урвал нь нимбэгийн хүчил үүсэх явдал юм.
Кребсийн мөчлөг нь 10 урвалаас бүрдэх ба тэдгээрийн дөрөв нь исэлдэлтийн урвал юм.
Урвалын явцад энергийн 70% нь ялгардаг.
Энэ мөчлөгийн биологийн үүрэг нь маш чухал бөгөөд учир нь энэ нь бүх гол хүнсний исэлдэлтийн задралын нийтлэг төгсгөл юм.
Энэ нь эс дэх исэлдэлтийн гол механизм бөгөөд үүнийг бодисын солилцооны "тогоо" гэж нэрлэдэг. Түлшний молекулууд (нүүрс ус, амин хүчил, өөх тосны хүчил) исэлдэх явцад бие нь ATP хэлбэрээр эрчим хүчээр хангагдана.Түлшний молекулууд ацетил-Ко-А болж хувирсны дараа Кребсийн циклд ордог.
Үүнээс гадна трикарбоксилын хүчлийн мөчлөг нь биосинтетик процессын завсрын бүтээгдэхүүнийг нийлүүлдэг. Энэ мөчлөг нь митохондрийн матрицад тохиолддог.
 Кребсийн мөчлөгийн хариу урвалыг авч үзье.
Кребсийн мөчлөгийн хариу урвалыг авч үзье.
Цикл нь дөрвөн нүүрстөрөгчийн бүрэлдэхүүн хэсэг болох оксалоацетат ба хоёр нүүрстөрөгчийн бүрэлдэхүүн хэсэг болох ацетил-Ко-А-ийн конденсацаас эхэлдэг.
Урвал нь цитрат синтазагаар катализ болж, альдол конденсацын дараа гидролиз үүсдэг. Завсрын бүтээгдэхүүн нь цитрил-Ко-А бөгөөд цитрат болон КоА болж гидролизд ордог.
Энэ бол анхны исэлдэлтийн урвал юм.
Урвалыг гурван ферментээс бүрдэх α-оксоглутаратдегидрогеназын цогцолбор катализатор болгодог.
 |
Сукцинил нь эрчим хүчээр баялаг холбоог агуулдаг.
Сукцинил-КоА-ийн тиоэфирийн холбоо тасрах нь гуанозин дифосфатын (ДНБ) фосфоржилттой холбоотой:
Сукцинил-КоА + ~ F + ДНБ Сукцинат + GTP + КоА
GTP-ийн фосфорын бүлэг нь ADP-д амархан шилжиж, ATP үүсгэдэг.
GTP + ADP ATP + ДНБ
Энэ бол субстратын фосфоржих урвал болох мөчлөгийн цорын ганц урвал юм.
Энэ бол гурав дахь исэлдэлтийн урвал юм:
Кребсийн мөчлөг нь нүүрстөрөгчийн давхар исэл, протон, электроныг үүсгэдэг.
Циклийн дөрвөн урвал нь редокс бөгөөд ферментүүд - NAD ба FAD коэнзим агуулсан дегидрогеназаар катализ болдог. Коэнзимүүд үүссэн H+ ба ē-г барьж амьсгалын замын гинжин хэлхээнд (биологийн исэлдэлтийн гинж) шилжүүлдэг.
Амьсгалын гинжин хэлхээний элементүүд нь митохондрийн дотоод мембран дээр байрладаг.
Амьсгалын гинж нь исэлдэлтийн урвалын систем бөгөөд энэ үед амьсгалын үр дүнд биед нэвтэрч буй H+ ба ē нь O2 руу аажмаар шилждэг. ATP нь амьсгалын замын гинжин хэлхээнд үүсдэг.
Гинжин дэх гол тээвэрлэгч ē нь төмөр, зэс агуулсан уураг (цитохром), коэнзим Q (ubiquinone) юм. Гинжинд 5 цитохром байдаг (b1, c1, c, a, a3).
b1, c1, c цитохромуудын протезийн бүлэг нь төмөр агуулсан гем юм.
Эдгээр цитохромын үйл ажиллагааны механизм нь ē ба H+ шилжүүлгийн үр дүнд исэлдсэн болон бууруулсан төлөвт аль алинд нь байж болох хувьсах валент бүхий төмрийн атом агуулдаг.
Цитохром оксидаза дээр үүсэх эцсийн урвал нь хэлбэртэй байна
Кребсийн мөчлөг ба амьсгалын замын гинжин хэлхээний энергийн тэнцвэр нь 24 ATP молекул юм.
Кребсийн мөчлөгийн диаграм

Органик бодисын задралын явцад ялгарсан энергийг эс тэр дор нь ашигладаггүй, харин өндөр энергитэй нэгдлүүд хэлбэрээр, ихэвчлэн хэлбэрээр хадгалагддаг. аденозин трифосфорын хүчил (ATP).
ATP нь мононуклеотид гэж ангилдаг. Энэ нь өндөр энергийн бондоор холбогдсон аденин, рибоз, фосфорын хүчлийн гурван үлдэгдэлээс бүрдэнэ.
Эдгээр холбоо нь тасарсан үед ялгардаг энергийг хадгалдаг.
ATP + H2O → ADP + H3PO4 + Q1,
ADP + H2O → AMP + H3PO4 + Q2,
AMP + H2O → аденин + рибоз + H3PO4 + Q3,
энд ATP нь аденозин трифосфорын хүчил; ADP - аценозин дифосфорын хүчил; AMP - аденозин монофосфорын хүчил; Q1 = Q2 = 30.6 кЖ; Q3 = 13.8 кЖ.
Эс дэх ATP-ийн нийлүүлэлт хязгаарлагдмал бөгөөд фосфоржилтын үйл явц - ADP (ADP + P → ATP) -д фосфорын хүчлийн үлдэгдэл нэмсэний улмаас нөхөгддөг.
Энэ нь амьсгалах, исгэх, фотосинтезийн үед янз бүрийн хурдаар явагддаг. ATP нь маш хурдан шинэчлэгддэг (хүний хувьд нэг ATP молекулын амьдрах хугацаа 1 минутаас бага байдаг).
ATP молекулуудад хуримтлагдсан энергийг бие махбодид анаболик урвалд (биосинтезийн урвал) ашигладаг.
ATP молекул нь бүх амьд биетүүдийн энергийн бүх нийтийн агуулах, тээвэрлэгч болдог.
Төв мэдрэлийн системийн анатоми ба физиологи
4. Өөх тосны солилцоо, тэдгээрийн биологийн үүрэг, дулааны багтаамж, бодисын солилцоонд оролцох. Өөх тосны энергийн үнэ цэнэ. Өөх тосны ордууд
Өөх тос нь амьтан, ургамлын эд эсийн нэг хэсэг болох органик нэгдлүүд бөгөөд голчлон триглицерид (глицерол ба янз бүрийн тосны хүчлүүдийн эфир) -ээс бүрддэг. Өөх тос нь триглицеридээс гадна бодис агуулдаг...
Органик бордооны хөрсний бичил биетэнд үзүүлэх нөлөө
2.
Байгаль дахь бодисын эргэлтэд бичил биетний үүрэг
Бичил биетний химийн идэвхжил нь азот, фосфор, хүхэр, нүүрстөрөгч болон бусад бодисын тасралтгүй эргэлтэнд илэрдэг. Байгаль дахь бичил биетний хамгийн идэвхтэй, өргөн оролцоотойгоор хөрс, усан мандалд...
Гормон окситоцин
1.
Окситоциний химийн бүтэц ба нийлэгжилт
Окситоцин нь мэдрэлийн гипофизийн өөрийн даавар биш бөгөөд зөвхөн түүний дотор хуримтлагдаж, гипоталамус-гипофизийн багцын аксонуудын дагуу урд гипоталамус - супраоптик ба паравентрикулярын цөмүүдээс хөдөлдөг.
3.
Бодисын урвал, шинжилгээ, синтез
Молекулын түвшинд байгалийн шинжлэх ухаан
3. Бодисын урвал, анализ, синтез
Бамбай булчирхайн өдөөгч ба бамбай булчирхайн дааврын түвшингийн бамбай булчирхайн өвчнөөс хамаарах байдал
2.5 Бамбай булчирхайн дааврын нийлэгжилтэнд үзүүлэх бодисын нөлөө
Одоогийн байдлаар янз бүрийн бодисын нийлэгжилтэнд үзүүлэх нөлөө нь холимог гэж үздэг.
Энэхүү диссертацийг R.V-ийн нийтлэлд нотолсон болно.
Кубасова, Е.Д...
Байгаль дахь бодисын эргэлтэнд бичил биетэн
Байгаль дахь бодисын эргэлтэд бичил биетний үүрэг
Бичил биетний тусламжтайгаар ургамал, амьтны гаралтай органик нэгдлүүдийг нүүрстөрөгч, азот, хүхэр, фосфор, төмөр гэх мэт эрдэсжүүлдэг.
Нүүрстөрөгчийн эргэлт. Ургамал нүүрстөрөгчийн эргэлтэнд идэвхтэй оролцдог...
Төрөл бүрийн байгалийн өөх тосоос тусгаарлагдсан бичил биетүүд
1.1 Тослог бодисын бүтэц
Өөх тос нь дэгддэггүй бодис бөгөөд 250-300°С хүртэл халаахад уур, хий, утаа хэлбэрээр ялгардаг дэгдэмхий бодисууд үүсч задардаг.
Өөх тос нь дулаан дамжуулагч муу...
Бүлэг 4. Элэг, түүний бодисын солилцоонд гүйцэтгэх үүрэг
Уургийн солилцоо. Өөх тосны солилцоо. Нүүрс усны солилцоо. Элэг, түүний бодисын солилцоонд гүйцэтгэх үүрэг
4.3 Бодисын солилцоонд элэгний үүрэг
Уураг, өөх тос, нүүрс усны солилцоог авч үзэхэд бид элэгний талаар олон удаа хөндөж байсан.
Элэг бол уургийн нийлэгжилтэнд хамгийн чухал эрхтэн юм. Цусан дахь бүх альбумин, коагуляцийн хүчин зүйлийн дийлэнх хэсгийг...
Хоол тэжээлийн үндсэн зарчим
7. Хүний хоол тэжээл дэх эрдэс бодисын үүрэг
Хүний биед агуулагдах эрдэс бодис болон хүнсний бүтээгдэхүүнд агуулагдах эрдэс бодисын хэмжээнээс хамааран макро болон микроэлементүүдэд хуваагддаг.
Эхнийх нь кальци, кали, магни, натри, фосфор, хлор, хүхэр...
Байгаль дахь химийн элементүүдийн эргэлтэд бичил биетний үүрэг
4. Байгаль дахь хүхрийн эргэлтэд бичил биетний гүйцэтгэх үүрэг, тэдгээрийн бодисыг хувиргах ач холбогдол, практик хэрэглээ.
Хүхрийн эргэлт нь түүнийг исэлдүүлдэг эсвэл бууруулдаг бактерийн үйл ажиллагааны үр дүнд үүсдэг.
Хүхрийг бууруулах үйл явц хэд хэдэн аргаар явагддаг. Ялзах нянгийн нөлөөгөөр - клостриди...
4.2 Каротиноидууд. Тэдний бүтэц, үүрэг, физиологийн үүрэг
Каротиноидууд - өөхөнд уусдаг шар, улбар шар, улаан пигментүүд нь бүх ургамлын хлоропластуудад байдаг. Тэд мөн ургамлын ногоон бус хэсэгт, жишээлбэл луувангийн үндэст хромопластын нэг хэсэг юм.
Фотосинтез нь биосфер дахь энергийн үндэс юм
4.3 Фикобилин. Тэдний бүтэц, үүрэг, физиологийн үүрэг
Цэнхэр-ногоон замаг (цианобактери), улаан замаг, далайн зарим криптомонадууд нь хлорофилл а, каротиноидоос гадна фикобилин пигмент агуулдаг...
Бичил биетний энергийн солилцоо
1.
Бодисын солилцоо, энергийн тухай ерөнхий ойлголт
Бүх амьд организм зөвхөн химийн холбоотой энергийг ашиглах боломжтой. Бодис бүр тодорхой хэмжээний боломжит энергитэй байдаг. Түүний химийн бондын үндсэн материал зөөгч...
ATP синтаза нь хоёр механизмаас бүрдэнэ. Эхнийх нь F0 нь эсийн мембранд байрлах цахилгаан мотор бөгөөд эсийн мембраны эсрэг талын потенциалын зөрүүгээр хуримтлагдсан энергийг хувиргадаг. Липидийн мембран нь энэхүү цахилгаан химийн "батерей" -д тусгаарлагчийн үүрэг гүйцэтгэдэг: ионууд түүгээр дамждаггүй. Боломжит ялгаа нь бусад нарийн төвөгтэй механизмаар эцэст нь хүчилтөрөгч дэх сахарыг "шатаах" замаар үүсдэг. Устөрөгчийн ион H+ нь "хэрэглэх олон талт" руу татагдаж, роторын уургийн дэлбээнд наалддаг. Ротор нь цахилгаан статик хүчний нөлөөгөөр эргэлдэж, моторын "яндангийн олон талт" хэсэгт хүрч буй дэлбэн нь катализаторын уургаар ионоос чөлөөлөгдөж, энэ ион нь цахилгаан статик хүчний потенциалыг тэнцүүлэх хандлагатай байгаа тул үүрэнд унадаг. мембраны хоёр тал. Тиймээс цахилгаан энерги нь эхлээд роторт бэхлэгдсэн молекулын босоо амны эргэлтийн механик энерги болж, эсийн гүнд орж, синтезийн механизм болох F1 руу шилждэг.
Механик-химийн реактор F1 нь гурван уургийн дэлбээнээс бүрдэх ба тэдгээр нь тус бүр нь хоёр уургийн молекулаас бүрддэг (тэдгээрийг α-F1 ба β-F1 гэж нэрлэдэг ба гол нь нэг молекулаас бүтсэн, γ-F1 гэж тэмдэглэгдсэн). Дэлбээн бүр нь атом хоорондын харилцан таталцлын улмаас орон зайн хоёр тогтвортой тохиргоог авч чаддаг - энгийн ханын унтраалга нь хоёр тогтвортой байрлалд байдаг шиг завсрын байрлал нь тогтворгүй байдаг. Гэхдээ эдгээр байрлалын нэг нь илүү өндөр энергитэй байдаг. Эргэдэг γ босоо амны тэгш бус байдлаас болж молекулууд нь "кам" байгаа мэт илүү өндөр энергийн тохиргоонд шилждэг.
ADP ба фосфатын ион αβ цогцолборт нэгдэх үед тэнцвэр алдагдаж, хуримтлагдсан энергитэй пүрш шиг молекул бага энергитэй төлөв рүү үсрэх ба хуримтлагдсан энерги нь ADP болон фосфатын ионыг ойртуулахад зарцуулагдана. , үүний үр дүнд тэд ATP молекул болж нэгдэж, эцэст нь энэ эрчим хүчний хангамжийг зайлуулдаг.
Хэрэв тусгайлан хийсэн урт гэрэлтдэг (флюресцент) бариул молекулыг F0 дээр роторт бэхэлсэн бол механизмын эргэлтийг микроскопоор харж болно. Киноны төгсгөлд та энэхүү гайхалтай туршилтыг Масасуке Ёшидагийн сэргээн засварлаж, роторын эргэлтийг харуулсан мэдээллийн хавсралтыг харж болно.
Сонирхолтой нь, роторын доод төгсгөлд өөр нэг уураг болох δ-F1 байдаг бөгөөд энэ нь урвалын анхны урвалж болох ADP-ийн оролцоотойгоор тохиргоог өөрчилж чаддаг. Реакторын эргэн тойронд хангалттай ADP байхгүй үед энэ уураг нь цахилгаан химийн энергийг үрэхгүйн тулд хэлбэрээ өөрчилж, роторыг саатуулдаг, учир нь зогссон ротороор H + ионуудын хөдөлгөөн хийх боломжгүй байдаг.
2.2. Бууруулах эквивалентуудын урсгалын зохицуулалт
Хэрэв исэлдэлтийн хоёр зам: чөлөөт ба энергийн нэгдэл нь нэг эсэд зэрэгцэн оршдог бол термодинамикийн хувьд илүү таатай байгаа бүх бууруулагч эквивалентыг ашиглахаас хэрхэн сэргийлэх вэ гэсэн асуудал гарч ирнэ. Энэ асуудлыг шийдвэрлэхэд бодисын солилцооны үйл явцын орон зайн ялгаа (тасалгаа) нь тэргүүлэх үүрэг гүйцэтгэдэг нь эргэлзээгүй. Жишээлбэл, үндсэн субстратын дегидрогеназууд нь матрицад байршдаг тул амьсгалын гинжийг тэжээдэг редукцийн эквивалентууд нь митохондри дотор шууд үүсдэг тул гадны чөлөөт исэлдэлтийн системд нэвтрэх боломжгүй байдаг. Үүнээс гадна дотоод митохондрийн мембран нь дегидрогеназууд нь зөвхөн митохондрид төдийгүй цитозолд байдаг субстратын матрицад хуримтлагдах үүрэгтэй AcH-аас хамааралтай хэд хэдэн тээвэрлэгчийг агуулдаг. Хэрэв өгөгдсөн субстратын дегидрогеназа нь зөвхөн цитозолд байрладаг бол цитозолоос матриц руу багасгах эквивалентыг шилжүүлэхийн тулд тусгай шаттл механизмыг ашигладаг.
малат-аспартат-глутамат шаттл.Энэ системийн үйл ажиллагаа нь NAD+ матрицаар дамжин экстрамитохондрийн NADH-ийн исэлдэлтэд хүргэдэг. Уг процесст дотоод митохондрийн мембраны хоёр талд байрлах хоёр фермент, тухайлбал малатдегидрогеназа ба аспартат: глутамат аминотрансфераза оролцдог. Үүнээс гадна хоёр тээвэрлэгч шаардлагатай: дикарбоксилын хүчил ба глутамат/аспартат антипортер. Сүүлийнх нь аспартат 2 -/ (глутамат 2_ + H +) солилцоог хурдасгадаг тул AjiH-ийн энергийг ашигладаг. Үүний үр дүнд гидридийн ионыг NADH+nar-аас NAD+in руу шилжүүлэх нь цитозолоос матриц руу нэг H+ ионы шилжилт хөдөлгөөнтэй нийлдэг.
Өөр нэг механизм нь хоёр глицерофосфатын дегидрогеназыг ашигладаг: цитозолик, NAD-аас хамааралтай ба митохондрийн, KoQ NAD-ийн оролцоогүйгээр. Шатл систем нь эд эсийн өвөрмөц шинж чанартай байдаг. Жишээлбэл, малат шаттл нь элгэнд маш идэвхтэй байдаг боловч митохондрид дикарбоксилат антипортер дутагдсан зүрхэнд байдаггүй. Глицерофосфатын хөлөг онгоцбамбай булчирхайн дааврын нөлөөгөөр огцом идэвхждэг.
Исэлдэлтийн бодисын солилцоог орон зайн тусгаарлах өөр нэг жишээ байж болно пероксисомууд.Эдгээр органеллууд нь нэвчилт нь гаднах митохондрийн мембрантай төстэй мембранаар хүрээлэгдсэн байдаг. Энэ нь уураг нэвчдэггүй боловч бага молекул жинтэй бодисыг амархан нэвтрүүлдэг. Пероксисомын хүчилтөрөгчийг шингээх нь урат оксидаза, D-амин хүчлийн оксидаза, а-гидрокси хүчлийн оксидазын үйл ажиллагаатай холбоотой юм. Пероксисомын оксидазууд нь митохондрийн хосолсон амьсгалын ферментүүдтэй өрсөлддөггүй, учир нь эдгээр оксидазын субстратууд нь NAD(P) болон амьсгалын замын гинжин хэлхээний оролцоогүйгээр исэлддэг. Урвалын хортой бүтээгдэхүүн болох устөрөгчийн хэт исэл нь эдгээр органеллуудын хамгийн элбэг уураг болох каталазын нөлөөгөөр пероксисомын дотор шууд задардаг.
3.1. H + - Пирофосфатын синтаза
1966 онд М.Бальчевски болон хамтран ажиллагсад хроматофороор органик бус пирофосфат үүсэхийг тодорхойлсон. Rhodospirillum rubrumгэрлийн нөлөөн дор. Хожим нь харанхуйд пирофосфат нь ATP шиг хроматофорын мембраныг эрчимжүүлдэг болохыг олж мэдсэн. Зохиогчийн бүлгийн туршилтууд нь пирофосфатын гидролиз нь хроматофорын мембран дээр Agr, түүнчлэн цэвэршүүлсэн пирофосфатаза агуулсан протеолипосом үүсгэдэг болохыг харуулсан. Rh. rubrum.Дараа нь Р.Нирен, М.Бальчевски нар пирофосфатаз ба H+-ATP синтаза агуулсан протеолипосомуудаар пирофосфатын гидролизийн энергийн улмаас АТФ нийлэгжсэн тухай мэдээлсэн. Rh. rubrum.Протонофорууд процессыг хаасан. Хроматофоруудад пирофосфатазын идэвхжилийн протоны хяналтыг харуулсан бөгөөд LpH тархах үед 8 дахин нэмэгджээ.
Дээр дурдсан тоо баримтууд үүнийг дүгнэхэд хангалттай юм шиг санагдаж байна Rh хроматофорын мембран пирофосфатаза. rubrtim H+ насосны үйл ажиллагаатай,Тогтмол гүйдэл ба пирофосфатын хоорондох энергийн урвуу харилцан хувиргалтыг катализатор. Тиймээс энэ ферментийг дараах байдлаар тодорхойлж болно H+-пирофосфатын синтаза.
Ферментийн үйл ажиллагааны механизм ба молекулын шинж чанар нь тодорхойгүй хэвээр байна. Мембран болон ферментийн уусдаг хэлбэрийн аль алиных нь пирофосфатазын идэвхийг дарангуйлдаг дарангуйлагчдын зөвхөн багцыг мэддэг. Эдгээр нь фтор, имодидифосфат, N-этилмалеймид, антибиотик Dio-9 юм. Олигомицин нь ферментэд нөлөөлдөггүй. DCCD нь хроматофор дахь пирофосфатазын идэвхийг бууруулдаг боловч уусмал эсвэл протеолипосомд биш юм. Протеолипосомоор A-f үүсэх нь DCCD-д мэдрэмтгий байдаг.
Энэ нь эсэд H+-пирофосфатын синтазын үүрэг гүйцэтгэдэг бололтой Rh. rubrumгэрлийн энергийн улмаас пирофосфатын нийлэгжилт байх ёстой (эсвэл
амьсгалах) эсвэл пирофосфатын гидролизийн улмаас AcH үүсэх. Гэсэн хэдий ч эхний тохиолдолд энгийн эсэд уусдаг пирофосфатазаар хуваагддаг үүссэн пирофосфатын цаашдын хувь заяа тодорхойгүй байна. Сүүлийнх нь пирофосфатын концентрацийг бага түвшинд байлгахад шаардлагатай бөгөөд ингэснээр ATP-аас хамааралтай биосинтезийг идэвхжүүлж, пирофосфат үүсэхтэй холбоотой юм. Гэсэн хэдий ч пирофосфатыг уусдаг пирофосфатазаар шууд задалдаг дүрэмд үл хамаарах зүйлүүд байдаг. Пирофосфатын энергийг ашигладаг хэд хэдэн синтетик процессыг зарим бактериудад тайлбарласан байдаг. байж магадгүй, Rh. rubrumЭнэ нь бичил биетний энэ ангилалд багтдаг. Ямар ч тохиолдолд H+-pyrophosphate synthase Rh. rubrumчухал биологийн үүрэгтэй байх ёстой. Хроматофор дахь түүний идэвхжил нь маш өндөр бөгөөд H + -ATP синтазынхтай харьцуулах боломжтой.
Ургамлын эсээс пирофосфатын санаанд оромгүй өндөр агууламж илэрсэн. Ургамлын хувьд H+-пирофосфатаза нь Голги аппаратын тонопласт ба мембранд байдаг.
3.2. Бактерийн бактери дахь протоны потенциалыг хянах
Өмнө дурьдсанчлан, олон бактери параллель электрон тээвэрлэх замтай байдаг бөгөөд тэдгээрийн зарим нь энерги хуримтлуулдаг бол зарим нь тийм биш юм. Нэмж дурдахад чөлөөт ба коньюгат исэлдэлтийг амьсгалын замын нэг гинжин хэлхээнд дараалан оруулж болно. "Ашигтай салгах" асуудлыг нянтай холбоотой судалж үзээгүй.
Өөрийгөө зохицуулах зарчимд суурилсан DCN-ийг өндөр байлгах механизмын сонирхолтой жишээг хөдөлгөөнт нянгаар хийсэн туршилтаар илрүүлсэн. DCN-ийн зохиомлоор өдөөгдсөн өөрчлөлтийг нян түүний хөдөлгөөнийг зохицуулдаг дохио гэж хүлээн зөвшөөрдөг болохыг харуулсан. Тиймээс задлагч нэмэх эсвэл хүчилтөрөгчийн дутагдал нь зэвүүн дохио болж, нянгийн хөдөлгөөний чиглэлийг өөрчилдөг. Үүний дагуу O2 нэмэх нь шугаман хөдөлгөөнд таатай татахуйц өдөөгч болж хувирдаг. Бактерийн үйл ажиллагаанд хүчилтөрөгчийн нөлөө (аэротаксис) нь зөвхөн орчин дахь O2-ийн концентраци Dn-д нөлөөлдөг тохиолдолд л илэрдэг болохыг тэмдэглэв.
Эдгээр мэдээллийн хамгийн энгийн тайлбар бол ийм юм бактери хэмжилт хийдэг төхөөрөмжтэй
протоны потенциал мөн туг мотор руу харгалзах дохиог илгээдэг;ингэж зохицуулж байнаТугны эргэлтийн чиглэл: Dp,H буурвал чиглэл нь эсрэгээрээ өөрчлөгдөнө, ихэсвэл өөрчлөгдөхгүй. Үүний үр дүнд эс нь Dp,N-ийг өндөр байлгах боломжтой газар руу шилждэг. Зохиогчийн нэрлэсэн ийм төрлийн таамаглалын механизм протометр,мембраны энергийн төлөв байдалд нөлөөлдөг олон ашигтай ба тааламжгүй үр нөлөөг нэгтгэх боломжийг танд олгоно.
Хлоропласт дахь хоёр фотосистемийн ажлыг зохицуулж, улмаар Dr,H, NADPH-ийн үйлдвэрлэлийг оновчтой болгодог механизмыг тодорхойлсон. Хэрэв фотосистем II хэт хурдан ажилладаг бол энэ нь исэлдүүлэгч тээвэрлэгчийг багасгахад хүргэдэг (магадгүй PQ),хоёр фотосистемийн хооронд холбогдсон. Энэ нөлөө нь ямар нэгэн байдлаар антенны хлорофилл агуулсан уургийг фосфоржуулдаг уургийн киназыг идэвхжүүлдэг. Нэрлэсэн уураг нь фосфоржуулаагүй төлөвт голчлон гранад савласан тилакоидуудад байрладаг. Фосфоржилт нь антенны уургуудын сөрөг цэнэгийг ихэсгэдэг бөгөөд тэдгээр нь тилакоидуудаас стромын мембранд тархдаг ба тэнд I фотосистем ихэвчлэн нутагшдаг.Үүний үр дүнд I фотосистем нь II-ээс илүү антенны хлорофилл, улмаар илүү их фотоныг хүлээн авдаг. Фотосистем I идэвхжсэнээр PQH2 исэлдэж, улмаар уураг киназыг дарангуйлдаг. Үргэлжилсэн уургийн фосфатаза нь антенны уургийг фосфоргүйжүүлж, стромын ламелла руу thylakoids-аас цааш урсахыг зогсооно.
5.1. Осмосын ажил
(Na+, метаболит)-симпортлогч. Архинд тэсвэртэй V. algino-lyticus,хуримтлалыг хариуцдаг Na+-NADH-хинон редуктаза, (Na+, метаболит)-симпортлогчтой 19 амин хүчил ба сахароз.
Мөн эсэд К+ хуримтлагддаг нь тогтоогдсон V. alginolyticusшүлтлэг рН үед энэ нь Na + -NADH-хинон редуктазын үүсгэсэн Aif> энергиээр хадгалагддаг. Шүлтлэг нян дахь Na+-аас хамааралтай метаболитуудын хуримтлалыг хэд хэдэн тайланд дурдсан байдаг. Гэсэн хэдий ч эдгээр шүлтлэгүүд Ajj,Na-г хэрхэн үүсгэдэг нь тодорхойгүй хэвээр байна.
NaCl-ийн бага ба дунд зэргийн концентрацид амьдардаг нейтрофил бактери нь импортын ион болгон Na+ биш харин H+ хэрэглэдэг. Гэсэн хэдий ч энэ дүрэмд үл хамаарах зүйлүүд бас мэдэгдэж байна. Тэгэхээр, пролин Na+-тай хамт эс рүү зөөвөрлөнө Mycobacterium phlei, Salmonella typhimuriumТэгээд E. coli.
Метаболит импортлох сонирхолтой "хос" механизмыг тайлбарлав E. coli.Энэ нян нь хуримтлуулах явцад H+ эсвэл Na+-ийг коньюгат катион болгон ашигладаг болох нь тогтоогдсон. мелибиоз.Бактерийн цитратыг шингээх Klebsiella pneumoniae-ийг хийдэгцитрат 3-, 2Na + ба 2H+-ийн шинж тэмдгийг хангадаг тээвэрлэгч. Энэ нь процессын хөдөлгөгч хүч нь Ar|e, pNa, DrN байх ёстой гэсэн үг юм.
А.Броуди болон хамтран ажиллагчид нь (Na+, proline) сим-портерийг салгаж чадсан. М.Флей,Энэ нь 20 кДа уураг болж хувирсан. Цэвэршүүлсэн симпортерийг фосфолипидээр сэргээсэн. Үүссэн протеолипосомууд нь K + ионуудын тархалтаас үүссэн Agr-ийн улмаас пролиныг зөөвөрлөсөн. Пролины хуримтлалыг протонофорууд дарангуйлдаг бөгөөд энэ нь Dg-ийг бууруулдаг, түүнчлэн сульфгидрил урвалжууд.
(Na+, акпартат) симпортерийг галофилийн бодисоос хэсэгчлэн цэвэрлэж, сэргээнэ. Halobacterium halobium.Бүх Далайн болон галофиль бичил биетүүд шүлтлэг бичил биетүүд шиг ихэвчлэн H + биш харин Na + -ийг импортын ион болгон ашигладаг.Энэ нь NaCl-ийн өндөр концентрацитай уусмалаар угаасан дээд амьтдын эсийн гаднах мембраны хувьд ч мөн адил юм. Энэ нөхцөл байдал нь цус бол "хүний бие дэх далайн нэг хэсэг" гэсэн үзэл баримтлалын бас нэг нотолгоо юм. Na+/K+-ATOa3a (зарим тохиолдолд Na+-ATPase) нь амьтны эсийн плазмалемма дээр AjiNa генераторын үүрэг гүйцэтгэдэг. Үүссэн AjiNa нь амин хүчил, элсэн чихэр, өөхний хүчил болон бусад нэгдлүүдийг эсэд зөөвөрлөх янз бүрийн тээвэрлэгчдэд ашиглагддаг. Хэд хэдэн (Na+, метаболит) симпортеруудыг тусгаарлаж, протеолипосомд нэгтгэдэг.
Зарим амьтны эсүүд гаднах мембранд H+-ATPase агуулдаг. Эдгээр эсүүдээс (H+, метаболит)-симпортерууд мөн илэрсэн.
ATP (аденозин трифосфат): амьд эсийг эрчим хүчээр хангадаг молекул
Цагаан будаа. 10.1. Аденозин трифосфатын бүтэц (ATP)
Электрон алдагдах нь реактив хүчилтөрөгчийн төрөл зүйл үүсэхэд хүргэдэг
Электронуудын ойролцоогоор 2% нь амьсгалын замын гинжин хэлхээнээс ялгарч хүчилтөрөгчтэй шууд холбогдож реактив хүчилтөрөгчийн төрлийг (ROS) үүсгэдэг. Амьсгалын гинжин хэлхээ эвдэрсэн тохиолдолд илүү их ROS үүсдэг. Эдгээр бодисууд нь митохондрийг гэмтээж, амьсгалын замын гинжин хэлхээг тасалдуулахад хүргэдэг. Харгис тойрог үүсч, үр дүнд нь ROS-ийн нөлөөн дор янз бүрийн гэмтэл хуримтлагдаж, эсийн хөгшрөлт үүсдэг.
Амьсгалын замын хордлого
ATP үүсэхийг саатуулдаг бодисууд нь биед хортой нөлөө үзүүлдэг.
АмиталТэгээд ротенонцогцолбор дахь электрон тээвэрлэлтийг блоклох I. Ротенон нь деррис (Derris scandens) ургамлын үндэснээс тусгаарлагдсан бөгөөд ихэвчлэн байгалийн пестицид болгон ашигладаг. Ходоод гэдэсний замд муу шингэдэг тул хүний биед бага хоруу чанартай. Гэсэн хэдий ч ротенон нь заламгайгаар хурдан шингэдэг тул загасанд хортой байдаг. Нэмж дурдахад, ротенон нь удаан хугацаагаар өртөхөд хүний хувьд аюултай бөгөөд энэ нь хөгжлийг үүсгэдэг.
Антимицин III цогцолбор дахь электрон тээвэрлэлтийг блоклодог.
Цианид(CN-), нүүрстөрөгчийн дутуу исэл (CO)Тэгээд Азидууд (N3-) IV цогцолборыг дарангуйлдаг. Тиймээс цианидын хордлогын үед цус нь хүчилтөрөгчөөр хангалттай ханасан хэдий ч аэробикийн бодисын солилцооны процессыг хаадаг. Аэробик бодисын солилцоо зогссоны улмаас венийн цус нь артерийн цусны өнгийг авдаг. Үүнээс гадна сүүн хүчлийн хуримтлалаас болж амьсгалын төвийг өдөөдөг тул гипервентиляци үүсдэг.
Олигомицинпротоны сувгийг хааж (V цогцолбор дахь F0) ба протонуудыг матриц руу буцахаас сэргийлдэг. Тиймээс ATP синтаза (F1) нь ATP-ийг нэгтгэх чадвараа алддаг.
Исэлдэлтийн фосфоржилтоор ATP-ийн биосинтез (II хэсэг)

Зураг дээр. Зураг 13.1-д амьсгалын гинжин хэлхээнд электрон ба протоны урсгалыг харуулав. -аас электрон ба протонууд NADH +дамжуулан цогцолбор Iба -аас FADN2дамжуулан цогцолбор IIдамжуулагддаг цогцолбор III. Дараа нь электронууд руу зөөгдөнө цогцолбор IV, тэдгээр нь хүчилтөрөгчтэй нэгддэг. Энэ үед протоныг матрицаас мембран хоорондын зай руу протоны шахуургаар шахаж, ATP синтазын F0 дэд нэгжийн протоны сувгаар дамжуулан матриц руу буцаж ирдэг. цогцолбор V). Протоны урсгал (протоны гүйдэл) молекулын хөдөлгүүрийг асаана - ATP синтазын цогцолборын F1 дэд хэсэг, мөн тэрээр молекулуудыг зохион байгуулдаг ADFТэгээд Fnтэдгээр нь молекул болж нийлдэг байдлаар ATP.
Амьсгалын замын ферментийн ажил гэж нэрлэгддэг нөлөөгөөр зохицуулагддаг амьсгалын замын хяналт.
- энэ нь амьсгалын замын гинжин хэлхээний дагуух электрон хөдөлгөөний хурд (өөрөөр хэлбэл амьсгалын хэмжээ) дээр цахилгаан химийн градиент шууд нөлөөлөл юм. Хариуд нь градиентийн хэмжээ нь шууд хамаардаг ATP/ADP харьцаа, эс дэх тоон нийлбэр нь бараг тогтмол байдаг ([ATP] + [ADP] = const). Катаболик урвал нь ATP-ийн өндөр түвшин, бага ADP-ийг тогтмол байлгахад чиглэгддэг.
Протоны градиент нэмэгдэх нь ADP-ийн хэмжээ буурч, ATP хуримтлагдах үед үүсдэг ( амрах байдал), i.e. Хэзээ ATP синтаза нь субстратаасаа салж, H + ионууд митохондрийн матриц руу нэвтэрдэггүй.. Энэ тохиолдолд градиентийн дарангуйлах нөлөө нэмэгддэг ба хэлхээгээр электронуудын хөдөлгөөн удааширдаг. Ферментийн цогцолборууд буурсан төлөвт үлддэг. Үүний үр дагавар нь I ба II цогцолборууд дээр NADH ба FADH 2-ийн исэлдэлт буурч, NADH болон NADH-ийн оролцоотойгоор TCA циклийн ферментийг дарангуйлах явдал юм. катаболизмыг удаашруулдагторонд.
Электрон хөдөлгөөний хурдаас цахилгаан химийн градиентийн хамаарал
Протоны градиент буурах нь ATP-ийн нөөц шавхагдаж, ADP илүүдэлтэй үед тохиолддог, өөрөөр хэлбэл. эсийн үйл ажиллагааны явцад. Энэ тохиолдолд ATP синтаза идэвхтэй ажиллаж, H + ионууд F o сувгаар матриц руу ордог. Энэ тохиолдолд протоны градиент аяндаа буурч, гинжин хэлхээний дагуух электронуудын урсгал нэмэгдэж, үр дүнд нь H + ионуудын мембран хоорондын зайд шахагдах нь нэмэгдэж, ATP синтазаар дахин хурдан "унадаг" митохондри руу ордог. ATP-ийн синтез. I ба II ферментийн цогцолборууд нь NADH ба FADH 2 (электронуудын эх үүсвэр) исэлдэлтийг сайжруулдаг. NADH-ийн дарангуйлах нөлөө арилдагнимбэгийн хүчлийн мөчлөг ба пируватдегидрогеназын цогцолбор дээр. Үр дүнд нь - катаболик урвал идэвхждэгнүүрс ус, өөх тос.
ATP синтаза- фермент (EC 3.6.3.14) нь ихэвчлэн протоны трансмембран цахилгаан химийн потенциалын энерги (өөрөөр хэлбэл протоны градиент ба цахилгаан хүчдэлийн хослол) -аас ADP ба фосфатын анионоос ATP нийлэгжилтийн урвалыг гүйцэтгэдэг. Зарим организмд натрийн ионуудын цахилгаан химийн чадавхийн улмаас түүнийг хувиргаснаар химийн бондын энерги болж хувирдаг бөгөөд үүнийг эсүүд биохимийн урвалд ашиглаж болно. Фермент нь урвуу процессыг явуулдаг тохиолдолд ATP гидролизийн улмаас трансмембран протоны градиент үүсгэдэг бол үүнийг нэрлэж болно. АТФаза.Антибиотик олигомицин нь ферментийн үйл ажиллагааг дарангуйлдаг.
Нэршил
ATP синтаза F 1 F 0 нь хоёр дэд нэгжээс бүрдэнэ.
- F 0 цогцолборын мембран хэсэг
- Митохондрийн матриц эсвэл бактерийн цитоплазм дахь цогцолборын F 1 хэсэг.
ATP синтазын дэд хэсгүүдийн нэршил нь нэлээд төвөгтэй бөгөөд урт түүхтэй. F 1 -бутархай нэр томъёоноос нэрээ авсан бутархай 1 1"), болон F0 (одоо илүү түгээмэл байдаг шиг "тэг" гэхээсээ илүү "O" гэсэн дэд үсгээр бичигдсэн) нь олигомициныг холбодог фракц гэж нэрлэгдсэн.
Бусад ферментүүдийн жишээн дээр ихэнх дэд нэгжийг Грек (α-аас ε) болон Латин (a-аас h) үсгээр нэрлэсэн байдаг. Үлдсэн дэд нэгжүүд нь нарийн төвөгтэй нэрийг авсан:
- F 6 (аас бутархай 6)
- OSCP (олигомицины мэдрэмтгий байдлыг хангах уураг- "олигомицинд мэдрэмтгий байдлын туслах уураг")
- A6L (энэ дэд нэгжийг кодлодог митохондрийн геномын генийн нэрээр нэрлэгдсэн)
- IF1 (дарангуйлах хүчин зүйл 1 -"дарангуйлах хүчин зүйл 1")
Дизайн ба үйл ажиллагааны зарчим
ATP синтаза нь эсийн мембрануудын аль нэг дээр байрладаг бөгөөд түүнд дүрэгдсэн F 0 домэйн ба γ дэд нэгжээр холбогдсон матриц эсвэл цитоплазм руу цухуйсан F 1 мужаас бүрдэнэ. Фермент нь мөөгний жимсний биетэй тодорхойгүй төстэй байдаг (тийм ч учраас эсийн биологийн уран зохиолд, ялангуяа хуучин хүмүүсийн ATP синтазыг заримдаа "мөөгний бие" гэж нэрлэдэг байсан).
F 1 цогцолбор нь ойролцоогоор 9-10 нм диаметртэй бөгөөд γ "хөл" устах үед мембранаас салж, F 1 -ATPase үүсгэдэг. F 1 нь гурван α ба гурван β дэд нэгжээс бүрдэх ба тэдгээр нь хос хосоороо нийлж гурван идэвхтэй төвтэй гексамеруудыг үүсгэдэг. γ дэд нэгж F 0 цогцолбортой хамт эргэлдэх үед конформаци өөрчлөгддөг.Энэ процессын хөдөлгөгч хүч нь F 0 домэйнээр катализлагдсан протоны дамжуулалт юм.Иймд протон нь ADP ба конденсацийн урвалд шууд оролцдоггүй. фосфатын анион. α 3 β 3 гексамерууд нь "статор" a-тай харьцуулахад эргэдэггүй гэдгийг тэмдэглэх нь зүйтэй, учир нь энэ нь δ дэд нэгжид агуулагддаг бөгөөд энэ нь эргээд F-ийн a дэд нэгж b ("иш") -тэй холбоотой байдаг. 1 цогцолбор (хэдийгээр F 1 нь ихэвчлэн хөдөлгөөнгүй гэж тооцогддог боловч үнэндээ хоёр цогцолбор нь бие биенээсээ эсрэг чиглэлд эргэлддэг).
F 1 цогцолборын үйл ажиллагааны зарчим нь эхлээд ADP ба фосфатыг идэвхтэй төв рүү сул холбож, дараа нь конформацийг өөрчилж, нягт холбодог бөгөөд үүний үр дүнд ATP синтез аяндаа явагддаг. Гурав дахь конформацид ATP идэвхтэй газраас гадагшилдаг.
F0 цогцолборын (ихэвчлэн "дэлхийн хамгийн жижиг эргэдэг цахилгаан мотор" гэж нэрлэдэг) ажиллах зарчим нь протоныг "ротор" (c-цагираг) руу холбохоос өмнө "stator" (дэд хэсэг a) дахь сувгаар дамжин өнгөрөх явдал юм. Мембраны нөгөө талд протоныг гаргахын тулд тодорхой зайд шилжсэн статор дахь өөр сувгаар гарах шаардлагатай, өөрөөр хэлбэл ротор гарахын тулд статортой харьцуулахад эргэлдэх шаардлагатай. . Тиймээс роторт хэвтээ потенциалын зөрүү үүсч, түүнийг статортой харьцуулахад эргүүлнэ.
Физиологийн үүрэг
ATPase-ийн үүргийг гүйцэтгэхэд ферментийг агааргүй бактери ашигладаг бөгөөд ATP-ийн энергийг ашиглан протоны мембраны цахилгаан химийн потенциалыг бий болгодог. Энэ градиент нь эргээд тугуудыг эргүүлж, ионуудыг эс рүү зөөвөрлөхөд ашиглагддаг.
Аэробик бактериудад ферментийг голчлон ATP синтез хийхэд ашигладаг бөгөөд үүний цахилгаан химийн потенциал нь амьсгалын замын электрон тээвэрлэлтийн гинжин хэлхээний үйл ажиллагаанаас үүсдэг. Ерөнхийдөө энэ процессыг исэлдэлтийн фосфоржилт гэж нэрлэдэг. Энэ нь эукариотуудын митохондрид үүсдэг ба дотоод мембран дээр ATP синтазын молекулууд байрладаг ба F 1 дэд хэсэг нь ADP ба фосфатаас ATP синтезийн процесс явагддаг матрицад байрладаг.
ATP синтез нь фотосинтезийн үйл явцад оролцдог; Энэ нь хлоропластын тилакоид мембран дээр байрладаг бөгөөд F 1 дэд нэгжийг стром руу чиглүүлдэг. Энэ тохиолдолд ферментийн бүтэц, үйл ажиллагааны механизм нь митохондрийн ATP синтазынхтай бараг ижил боловч протоны цахилгаан химийн потенциал нь үндсэндээ өөр электрон тээврийн гинжин хэлхээнд үүсдэг.