1. Өгүүлбэрт ямар үг дутуу, (а-г) үсгээр солигдсон бэ?
"АТФ молекул нь азотын суурь (a), таван нүүрстөрөгчийн моносахарид (b) ба (в) хүчлийн үлдэгдэл (d) зэргээс бүрдэнэ."
Дараах үгсийг үсгээр сольсон: а – аденин, б – рибоз, в – гурав, d – фосфор.
2. АТФ-ийн бүтэц ба нуклеотидын бүтцийг харьцуул. Ижил төстэй болон ялгаатай талуудыг тодорхойлох.
Үнэн хэрэгтээ ATP нь РНХ-ийн аденил нуклеотидын (аденозин монофосфат эсвэл AMP) дериватив юм. Хоёр бодисын молекулуудад азотын суурь аденин ба таван нүүрстөрөгчийн сахарын рибоз орно. Ялгаа нь РНХ-ийн аденил нуклеотид (бусад нуклеотидын адил) нь зөвхөн нэг фосфорын хүчлийн үлдэгдэл агуулдаг бөгөөд өндөр энергитэй (өндөр энергитэй) холбоо байхгүйтэй холбоотой юм. ATP молекул нь гурван фосфорын хүчлийн үлдэгдэл агуулдаг бөгөөд тэдгээрийн хооронд хоёр өндөр энергийн холбоо байдаг тул ATP нь батерей болон энерги зөөгч үүрэг гүйцэтгэдэг.
3. АТФ гидролизийн процесс юу вэ? ATP синтез? Гэж юу вэ биологийн үүрэг ATP?
Гидролизийн явцад нэг фосфорын хүчлийн үлдэгдлийг ATP молекулаас (дефосфоризаци) зайлуулдаг. Энэ тохиолдолд өндөр энергитэй холбоо тасарч, 40 кЖ/моль энерги ялгарч, ATP нь ADP (аденозин дифосфорын хүчил) болж хувирдаг.
ATP + H 2 O → ADP + H 3 PO 4 + 40 кЖ
ADP нь өөр фосфатын бүлгийг устгаж, энергийн хоёр дахь "хэсэг" ялгарснаар цаашдын гидролиз (энэ нь ховор тохиолддог) болно. Энэ тохиолдолд ADP нь AMP (аденозин монофосфорын хүчил) болж хувирдаг.
ADP + H 2 O → AMP + H 3 PO 4 + 40 кЖ
ATP нийлэгжилт нь ADP молекулд фосфорын хүчлийн үлдэгдэл нэмсэний үр дүнд үүсдэг (фосфоржилт). Энэ үйл явц нь гол төлөв митохондри ба хлоропласт, хэсэгчлэн эсийн гиалоплазмд тохиолддог. ADP-ээс 1 моль ATP үүсгэхийн тулд дор хаяж 40 кЖ энерги зарцуулах шаардлагатай.
ADP + H 3 PO 4 + 40 кЖ → ATP + H 2 O
ATP нь бүх нийтийн агуулах (батарей) бөгөөд амьд организмын эсэд энергийн тээвэрлэгч юм. Эрчим хүч шаарддаг эсэд тохиолддог бараг бүх биохимийн процессуудад ATP-ийг эрчим хүчний нийлүүлэгч болгон ашигладаг. ATP-ийн энергийн ачаар уураг, нүүрс ус, липидийн шинэ молекулууд нийлэгжиж, бодисын идэвхтэй тээвэрлэлт явагдаж, туг ба цилий хөдөлгөөн явагдаж, эсийн хуваагдал, булчингууд ажиллаж, биеийн тогтмол температурыг дулаанаар хангадаг. цуст амьтад гэх мэт.
4. Ямар холболтыг макроэрги гэж нэрлэдэг вэ? Өндөр энергийн холбоо агуулсан бодисууд ямар үүрэг гүйцэтгэдэг вэ?
Макроэргик холбоо нь тасрахад их хэмжээний энерги ялгаруулдаг (жишээлбэл, макроэргик ATP холбоо тус бүрийн тасрах үед 40 кЖ/моль энерги ялгардаг) холбоог хэлнэ. Өндөр энерги агуулсан бодисууд нь янз бүрийн амьдралын үйл явцад батерей, тээвэрлэгч, эрчим хүчний нийлүүлэгч болж чаддаг.
5. Ерөнхий томъёо ATP - C 10 H 16 N 5 O 13 P 3. 1 моль АТФ гидролиз болж ADP болоход 40 кЖ энерги ялгардаг. 1 кг ATP-ийн гидролизийн үед хичнээн хэмжээний энерги ялгарах вэ?
● ATP-ийн молийн массыг тооцоол.
M (C 10 H 16 N 5 O 13 P 3) = 12 × 10 + 1 × 16 + 14 × 5 + 16 × 13 + 31 × 3 = 507 г / моль.
● 507 г ATP (1 моль) гидролизд ороход 40 кЖ энерги ялгарна.
Энэ нь 1000 г ATP-ийн гидролизийн үед дараахь зүйл ялгарна гэсэн үг юм: 1000 г × 40 кЖ: 507 г ≈ 78.9 кЖ.
Хариулт: 1 кг АТФ-ыг АДФ болж гидролиздэхэд ойролцоогоор 78.9 кЖ энерги ялгарна.
6. Сүүлийн (гурав дахь) фосфорын хүчлийн үлдэгдэлд цацраг идэвхт фосфор 32 R гэсэн шошготой ATP молекулуудыг нэг эсэд, эхний (рибозтой хамгийн ойр) үлдэгдэлд 32 R гэж тэмдэглэсэн ATP молекулуудыг нөгөө эсэд оруулсан. 5 минутын дараа 32 R гэсэн шошготой органик бус фосфатын ионы агууламжийг хоёр эсэд хэмжсэн.Энэ нь хаана өндөр байсан, яагаад?
Сүүлчийн (гурав дахь) фосфорын хүчлийн үлдэгдэл нь ATP-ийн гидролизийн явцад амархан салдаг бөгөөд эхний (рибозтой хамгийн ойрхон) нь ATP-аас AMP-ийн хоёр үе шаттай гидролизийн үед ч салдаггүй. Тиймээс сүүлийн (гурав дахь) фосфорын хүчлийн үлдэгдэлд тэмдэглэгдсэн ATP-ийг нэвтрүүлсэн эсэд цацраг идэвхт органик бус фосфатын агууламж өндөр байх болно.
Эрчим хүч булчингийн үйл ажиллагаа
Өмнө дурьдсанчлан булчингийн үйл ажиллагааны хоёр үе шат - агшилт ба тайвшрал нь ATP-ийн гидролизийн явцад ялгардаг энергийг заавал хэрэглэх үед үүсдэг.
Гэсэн хэдий ч булчингийн эсүүд дэх ATP-ийн нөөц нь ач холбогдолгүй (амрах үед булчин дахь ATP-ийн концентраци 5 ммоль / л орчим байдаг) бөгөөд 1-2 секундын турш булчингийн ажилд хангалттай байдаг. Тиймээс булчингийн үйл ажиллагааг уртасгахын тулд булчинд ATP-ийн нөөцийг нөхөх шаардлагатай. үед шууд булчингийн эсэд ATP үүсэх биеийн ажил ATP-ийн дахин синтез гэж нэрлэгддэг ба эрчим хүчний хэрэглээтэй хамт ирдэг.
Тиймээс булчингууд ажиллах үед тэдгээрийн дотор хоёр процесс нэгэн зэрэг явагддаг: агшилт, тайвшрал, нөхөн төлжилтөд шаардлагатай энергийг өгдөг ATP гидролиз. ATP синтез, энэ бодисын алдагдлыг нөхөх. Хэрэв булчингийн агшилт, тайвшралыг хангахын тулд зөвхөн ATP-ийн химийн энергийг ашигладаг бол нүүрс ус, өөх тос, амин хүчил, креатин фосфат зэрэг олон төрлийн нэгдлүүдийн химийн энерги нь ATP-ийн дахин синтез хийхэд тохиромжтой.
ATP-ийн бүтэц, биологийн үүрэг
Аденозин трифосфат (ATP) нь нуклеотид юм. ATP (аденозин трифосфорын хүчил) молекул нь азотын суурь аденин, таван нүүрстөрөгчийн сахар рибоз ба өндөр энергийн холбоогоор холбогдсон фосфорын хүчлийн гурван үлдэгдэлээс бүрдэнэ. Гидролизийн үед их хэмжээний энерги ялгардаг. ATP нь эсийн гол макроэрг бөгөөд өндөр энергитэй химийн бондын энерги хэлбэрээр энерги хуримтлуулагч юм.
Физиологийн нөхцөлд, өөрөөр хэлбэл амьд эсэд байдаг ийм нөхцөлд ATP (506 г) моль задрахад 12 ккал буюу 50 кЖ энерги ялгардаг.
ATP үүсэх замууд
Аэробик исэлдэлт (эдийн амьсгал)
Ижил нэршил: исэлдэлтийн фосфоржилт, амьсгалын замын фосфоржилт, аэробик фосфоржилт.
Энэ зам нь митохондрид үүсдэг.
Цикл трикарбоксилын хүчилАнглийн биохимич Г.Кребс анх нээсэн (Зураг 4).
Эхний урвалыг цитрат синтаза ферментээр катализаж, ацетил-КоА-ийн ацетил бүлэг оксалоацетаттай конденсацлаж, нимбэгийн хүчил үүсгэдэг. Энэ урвалын үед ферменттэй холбогдсон цитрил-КоА нь завсрын бүтээгдэхүүн болж үүсдэг бололтой. Дараа нь сүүлийнх нь аяндаа, эргэлт буцалтгүй гидролиз болж цитрат ба HS-CoA үүсгэдэг.
Хоёр дахь урвалын үр дүнд үүссэн нимбэгийн хүчил нь усгүйжүүлж, цис-аконитын хүчил үүсгэдэг бөгөөд энэ нь усны молекулыг нэмснээр изоцитрат хүчил (изоцитрат) болдог. Эдгээр буцах боломжтой усжилт-шингэн алдалтын урвалыг аконитат гидратаза (аконитаза) ферментээр идэвхжүүлдэг. Үүний үр дүнд цитрат молекулд H ба OH-ийн харилцан хөдөлгөөн үүсдэг.
Цагаан будаа. 4. Трикарбоксилын хүчлийн мөчлөг (Кребсийн мөчлөг)
Гурав дахь урвал нь Кребсийн мөчлөгийн хурдыг хязгаарлаж байгаа бололтой. Изоцитритийн хүчил нь NAD-аас хамааралтай изоцитрат дегидрогеназын оролцоотойгоор усгүйжүүлдэг. Изоцитрат дегидрогеназын урвалын үед изоцитийн хүчил нэгэн зэрэг декарбоксил болдог. NAD-аас хамааралтай изоцитрат дегидрогеназа нь тусгай идэвхжүүлэгч болгон ADP-ийг шаарддаг аллостерик фермент юм. Нэмж дурдахад фермент нь үйл ажиллагаагаа харуулахын тулд ионууд эсвэл ионууд шаардлагатай байдаг.
Дөрөв дэх урвалын үед α-кетоглутарийн хүчлийн исэлдэлтийн декарбоксилжилт явагдаж, өндөр энергитэй сукцинил-КоА нэгдэл үүсдэг. Энэ урвалын механизм нь пируватыг ацетил-КоА-д исэлдүүлэх декарбоксилжих урвалтай төстэй; α-кетоглутаратдегидрогеназын цогцолбор нь бүтцийн хувьд пируватдегидрогеназын цогцолбортой төстэй. Аль ч тохиолдолд урвалд 5 коэнзим оролцдог: TPP, липоид хүчил амид, HS-CoA, FAD, NAD+.
Тав дахь урвалыг сукцинил-КоА синтетаза ферментээр хурдасгадаг. Энэ урвалын явцад GTP ба органик бус фосфатын оролцоотойгоор сукцинил-КоА нь сукциний хүчил (сукцинат) болж хувирдаг. Үүний зэрэгцээ GTP-ийн өндөр энергитэй фосфатын холбоо үүсэх нь сукцинил-КоА-ийн өндөр энергитэй тиоэфирийн холбооноос болж үүсдэг.
Зургаа дахь урвалын үр дүнд сукцинатыг фумарины хүчилд усгүйжүүлдэг. Сукцинатын исэлдэлт нь сукцинатдегидрогеназаар явагддаг.
коэнзим FAD нь уурагтай нягт (ковалентын) холбогддог молекулд. Хариуд нь сукцинатдегидрогеназа нь дотоод митохондрийн мембрантай нягт холбогддог.
Долоо дахь урвал нь фумарат гидратаза (фумараза) ферментийн нөлөөн дор явагддаг. Үүссэн фумарын хүчил нь усжуулж, урвалын бүтээгдэхүүн нь алимны хүчил (малат) юм.
Эцэст нь, трикарбоксилын хүчлийн мөчлөгийн найм дахь урвалын үед митохондрийн NAD-аас хамааралтай малатдегидрогеназын нөлөөн дор L-малат нь оксалоацетат болж исэлддэг.
Нэг мөчлөгийн эргэлтийн үед Кребсийн цикл дэх нэг ацетил-КоА молекулын исэлдэлт ба исэлдэлтийн фосфоржуулалтын систем нь 12 ATP молекулыг үүсгэж болно.
Агааргүй исэлдэлт
Синонимууд: субстратын фосфоржилт, агааргүй ATP синтез. Цитоплазмд орж, тусгаарлагдсан устөрөгч нь бусад бодисуудтай нэгддэг. Субстратаас хамааран ATP-ийн агааргүй синтезийн хоёр замыг ялгадаг: креатин фосфат (креатин киназ, алактик) ба гликолитик (гликолиз, лактат). Мэдрэлийн үед субстрат нь креатин фосфат, хоёрдугаарт - глюкоз юм.
Эдгээр замууд нь хүчилтөрөгчийн оролцоогүйгээр явагддаг.
Бидний биеийн аль ч эсэд сая сая биологийн бодис урсдаг химийн урвал. Тэдгээр нь ихэвчлэн эрчим хүч шаарддаг янз бүрийн ферментээр катализатор болдог. Үүнийг эс хаанаас авдаг вэ? Эрчим хүчний гол эх үүсвэрүүдийн нэг болох ATP молекулын бүтцийг авч үзвэл энэ асуултад хариулж болно.
ATP бол бүх нийтийн эрчим хүчний эх үүсвэр юм
ATP нь аденозин трифосфат буюу аденозин трифосфат гэсэн үг юм. Уг бодис нь аливаа эсийн энергийн хамгийн чухал хоёр эх үүсвэрийн нэг юм. ATP-ийн бүтэц, түүний биологийн үүрэг нь хоорондоо нягт холбоотой байдаг. Ихэнх биохимийн урвалууд нь зөвхөн бодисын молекулуудын оролцоотойгоор явагдах боломжтой бөгөөд энэ нь ялангуяа үнэн юм.Гэхдээ ATP нь урвалд шууд оролцдоггүй: аливаа процесс явагдахын тулд аденозин трифосфатад агуулагдах энерги шаардлагатай байдаг.
Бодисын молекулуудын бүтэц нь фосфатын бүлгүүдийн хооронд үүссэн холбоог агуулсан байдаг. их хэмжээнийэрчим хүч. Иймд ийм холбоог макроэргик буюу макроэнергетик (макро=олон, их хэмжээ) гэж бас нэрлэдэг. Энэ нэр томъёог эрдэмтэн Ф.Липман анх нэвтрүүлсэн бөгөөд тэрээр мөн тэдгээрийг тодорхойлохдоо ̴ тэмдгийг ашиглахыг санал болгосон.
Эсийн хувьд аденозин трифосфатын тогтмол түвшинг хадгалах нь маш чухал юм. Энэ нь ялангуяа булчингийн эдийн эсүүд болон мэдрэлийн утаснуудад үнэн байдаг, учир нь тэдгээр нь эрчим хүчнээс хамгийн их хамааралтай байдаг бөгөөд тэдгээрийн үйл ажиллагааг гүйцэтгэхийн тулд аденозин трифосфатын өндөр агууламж шаарддаг.
ATP молекулын бүтэц
Аденозин трифосфат нь рибоз, аденин, үлдэгдэл гэсэн гурван элементээс бүрдэнэ.

Рибоз- пентозын бүлэгт хамаарах нүүрс ус. Энэ нь рибоз нь 5 нүүрстөрөгчийн атом агуулдаг гэсэн үг бөгөөд тэдгээр нь нэг мөчлөгт багтдаг. Рибоз нь 1-р нүүрстөрөгчийн атомын β-N-гликозидын холбоогоор дамжуулан аденинтай холбогддог. 5-р нүүрстөрөгчийн атом дахь фосфорын хүчлийн үлдэгдэл мөн пентозд нэмэгддэг.
Аденин бол азотын суурь юм.Рибозд ямар азотын суурь наалдсанаас хамааран GTP (гуанозин трифосфат), TTP (тимидин трифосфат), CTP (цитидин трифосфат) ба UTP (уридин трифосфат) нь ялгагдана. Эдгээр бүх бодисууд нь аденозин трифосфаттай төстэй бүтэцтэй бөгөөд ойролцоогоор ижил үүрэг гүйцэтгэдэг боловч тэдгээр нь эсэд хамаагүй бага байдаг.
Фосфорын хүчлийн үлдэгдэл. Рибозд дээд тал нь гурван фосфорын хүчлийн үлдэгдэл хавсарч болно. Хэрэв хоёр эсвэл ганцхан байвал бодисыг ADP (дифосфат) эсвэл AMP (монофосфат) гэж нэрлэдэг. Фосфорын үлдэгдлүүдийн хооронд макроэнергийн холбоо үүсч, тасарсаны дараа 40-60 кЖ энерги ялгардаг. Хэрэв хоёр холбоо тасарсан бол 80, бага давтамжтай - 120 кЖ энерги ялгардаг. Рибоз болон фосфорын үлдэгдэл хоорондын холбоо тасрахад ердөө 13,8 кДж ялгардаг тул трифосфатын молекулд зөвхөн хоёр өндөр энергитэй холбоо (P ̴ P ̴ P), ADP молекулд нэг (P ̴) байна. P).
Эдгээр нь ATP-ийн бүтцийн онцлог юм. Фосфорын хүчлийн үлдэгдлүүдийн хооронд макроэнергетик холбоо үүсдэг тул ATP-ийн бүтэц, үйл ажиллагаа хоорондоо холбоотой байдаг.
ATP-ийн бүтэц, молекулын биологийн үүрэг. Аденозин трифосфатын нэмэлт үүрэг
Эрчим хүчээс гадна ATP нь эсэд бусад олон үүргийг гүйцэтгэдэг. Бусад нуклеотид трифосфатуудтай хамт трифосфат нь нуклейн хүчлийг бүтээхэд оролцдог. Энэ тохиолдолд ATP, GTP, TTP, CTP, UTP нь азотын суурь нийлүүлэгчид юм. Энэ шинж чанарыг процесс болон транскрипцид ашигладаг.
ATP нь ионы сувгуудын үйл ажиллагаанд шаардлагатай байдаг. Жишээлбэл, Na-K суваг нь эсээс 3 натрийн молекулыг шахаж, 2 калийн молекулыг эс рүү шахдаг. Энэхүү ионы гүйдэл нь мембраны гаднах гадаргуу дээр эерэг цэнэгийг хадгалахад шаардлагатай бөгөөд зөвхөн аденозин трифосфатын тусламжтайгаар суваг ажиллах боломжтой. Протон ба кальцийн сувагт мөн адил хамаарна.
ATP нь хоёр дахь элч cAMP (циклик аденозин монофосфат) -ын урьдал бодис юм - cAMP нь зөвхөн эсийн мембраны рецепторуудын хүлээн авсан дохиог дамжуулдаг төдийгүй аллостерийн эффектор юм. Аллостерийн эффекторууд нь ферментийн урвалыг хурдасгах эсвэл удаашруулдаг бодис юм. Тиймээс циклийн аденозин трифосфат нь бактерийн эсэд лактозын задралыг хурдасгадаг ферментийн нийлэгжилтийг саатуулдаг.
Аденозин трифосфатын молекул нь өөрөө аллостерийн эффектор байж болно. Түүнээс гадна, ийм процесст ADP нь ATP-ийн антагонист үүрэг гүйцэтгэдэг: хэрэв трифосфат нь урвалыг хурдасгадаг бол дифосфат нь үүнийг дарангуйлдаг ба эсрэгээр. Эдгээр нь ATP-ийн үүрэг, бүтэц юм.

Эсэд ATP хэрхэн үүсдэг вэ?
ATP-ийн үүрэг, бүтэц нь бодисын молекулуудыг хурдан хэрэглэж, устгадаг. Тиймээс трифосфатын синтез нь эсэд энерги үүсэх чухал үйл явц юм.
Аденозин трифосфатын синтезийн хамгийн чухал гурван арга байдаг.
1. Субстратын фосфоржилт.
2. Исэлдэлтийн фосфоржилт.
3. Фотофосфоризаци.
Субстратын фосфоржилт нь эсийн цитоплазмд тохиолддог олон урвал дээр суурилдаг. Эдгээр урвалыг гликолиз гэж нэрлэдэг - анэробын үе шат Гликолизийн 1 мөчлөгийн үр дүнд глюкозын 1 молекулаас хоёр молекул нийлэгжиж, дараа нь энерги үйлдвэрлэхэд зарцуулагддаг бөгөөд хоёр ATP нийлэгждэг.
- C 6 H 12 O 6 + 2ADP + 2Pn --> 2C 3 H 4 O 3 + 2ATP + 4H.
Эсийн амьсгал
Исэлдэлтийн фосфоржилт нь мембраны электрон тээвэрлэлтийн гинжин хэлхээний дагуу электронуудыг шилжүүлэх замаар аденозин трифосфат үүсэх явдал юм. Энэхүү дамжуулалтын үр дүнд мембраны нэг талд протоны градиент үүсч, ATP синтазын уургийн салшгүй багцын тусламжтайгаар молекулууд үүсдэг. Үйл явц нь митохондрийн мембран дээр явагддаг.

Митохондри дахь гликолиз ба исэлдэлтийн фосфоржилтын үе шатуудын дараалал нь амьсгал гэж нэрлэгддэг нийтлэг үйл явцыг бүрдүүлдэг. Дараа нь бүтэн мөчлөгНэг эс дэх глюкозын 1 молекулаас 36 ATP молекул үүсдэг.
Фотофосфоризаци
Фотофосфоржилтын үйл явц нь исэлдэлтийн фосфоржилттой адил бөгөөд зөвхөн нэг ялгаа нь: гэрлийн нөлөөн дор эсийн хлоропластуудад фотофосфоржилтын урвал явагддаг. ATP нь ногоон ургамал, замаг, зарим бактерийн эрчим хүчний үйлдвэрлэлийн гол үйл явц болох фотосинтезийн гэрлийн үе шатанд үүсдэг.
Фотосинтезийн явцад электронууд ижил электрон тээвэрлэх гинжээр дамждаг бөгөөд үүний үр дүнд протоны градиент үүсдэг. Мембраны нэг тал дахь протоны концентраци нь ATP синтезийн эх үүсвэр юм. Молекулуудын угсралтыг ATP синтаза ферментээр гүйцэтгэдэг.

Дундаж эс нь жингийн хувьд 0.04% аденозин трифосфат агуулдаг. Гэсэн хэдий ч хамгийн их их ач холбогдолбулчингийн эсүүдэд ажиглагддаг: 0.2-0.5%.
Нэг эсэд 1 тэрбум орчим ATP молекул байдаг.
Молекул бүр 1 минутаас илүүгүй амьдардаг.
Аденозин трифосфатын нэг молекул өдөрт 2000-3000 удаа шинэчлэгддэг.
Нийтдээ хүний бие өдөрт 40 кг аденозин трифосфатыг нийлэгжүүлдэг бөгөөд ямар ч үед ATP-ийн нөөц 250 гр байдаг.

Дүгнэлт
ATP-ийн бүтэц, түүний молекулуудын биологийн үүрэг нь хоорондоо нягт холбоотой байдаг. Фосфатын үлдэгдэл хоорондын өндөр энергийн холбоо нь асар их хэмжээний энерги агуулдаг тул энэ бодис нь амьдралын үйл явцад гол үүрэг гүйцэтгэдэг. Аденозин трифосфат нь эсэд олон үүрэг гүйцэтгэдэг тул үүнийг хадгалах нь чухал юм тогтмол төвлөрөлбодисууд. Бондын энерги нь биохимийн урвалд байнга ашиглагддаг тул задрал, синтез нь өндөр хурдтай явагддаг. Энэ нь биеийн аль ч эсэд зайлшгүй шаардлагатай бодис юм. Энэ нь ATP-ийн бүтцийн талаар хэлж болох бүх зүйл байж магадгүй юм.
Мэдлэгийн санд сайн ажлаа илгээх нь энгийн зүйл юм. Доорх маягтыг ашиглана уу
Мэдлэгийн баазыг суралцаж, ажилдаа ашигладаг оюутнууд, аспирантууд, залуу эрдэмтэд танд маш их талархах болно.
Нийтэлсэн http://www.allbest.ru/
- Оршил
- 1.1 ATP-ийн химийн шинж чанар
- 1.2 Физик шинж чанар ATP
- 2.1
- 3.1 Эс дэх үүрэг
- 3.2 Ферментийн үйл ажиллагаанд гүйцэтгэх үүрэг
- 3.4 ATP-ийн бусад функцууд
- Дүгнэлт
- Ном зүй
Тэмдгүүдийн жагсаалт
ATP - аденозин трифосфат
ADP - аденозин дифосфат
AMP - аденозин монофосфат
РНХ - рибонуклеины хүчил
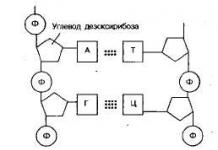
ДНХ - дезоксирибонуклеины хүчил
NAD - никотинамид аденин динуклеотид
PVC - пирувийн хүчил
G-6-P - фосфоглюкозын изомераза
F-6-F - фруктоз-6-фосфат
TPP - тиамин пирофосфат
FAD - фениладенин динуклеотид
Fn - хязгааргүй фосфат
G - энтропи
RNR - рибонуклеотидын редуктаза
Оршил
Манай гараг дээр оршин суудаг бүх амьд амьтны эрчим хүчний гол эх үүсвэр нь нарны гэрлийн энерги бөгөөд зөвхөн ногоон ургамал, замаг, ногоон, нил ягаан өнгийн бактерийн эсүүд шууд хэрэглэдэг. Эдгээр эсүүдээс нүүрстөрөгчийн давхар исэлфотосинтезийн явцад ус, органик бодис (нүүрс ус, өөх тос, уураг, нуклейн хүчил гэх мэт) үүсдэг. Ургамлыг идсэнээр амьтад органик бодисыг эцсийн хэлбэрээр олж авдаг. Эдгээр бодисуудад хуримтлагдсан энерги нь тэдэнтэй хамт гетеротроф организмын эсүүдэд дамждаг.
Амьтны организмын эсэд исэлдэх явцад органик нэгдлүүдийн энерги нь ATP энерги болж хувирдаг. (Энэ тохиолдолд ялгарсан нүүрстөрөгчийн давхар исэл ба усыг автотроф организмууд фотосинтезийн үйл явцад дахин ашигладаг.) Бүх амин чухал үйл явц нь ATP-ийн энергийг ашиглан явагддаг: органик нэгдлүүдийн биосинтез, хөдөлгөөн, өсөлт, эсийн хуваагдал гэх мэт.
Бие махбодид ATP үүсэх, ашиглах сэдэв нь удаан хугацааны туршид шинэ зүйл биш боловч та аль алиных нь бүрэн хэлэлцүүлгийг нэг эх сурвалжаас олох нь ховор бөгөөд эдгээр үйл явцын аль алиных нь дүн шинжилгээг нэг дор олж авах нь ховор байдаг. өөр өөр организмд.
Үүнтэй холбогдуулан бидний ажлын ач холбогдол нь амьд организмд ATP үүсэх, ашиглах талаар нарийвчлан судлах явдал болсон. Энэ сэдвийг шинжлэх ухааны алдартай уран зохиолд зохих түвшинд судлаагүй.
Бидний ажлын зорилго нь:
· амьтан, хүний биед АТФ үүсэх механизм, хэрэглэх арга замыг судлах.
Бидэнд дараах үүрэг даалгавар өгсөн.
· ATP-ийн химийн шинж чанар, шинж чанарыг судлах;
· Амьд организмд АТФ үүсэх замд дүн шинжилгээ хийх;
· Амьд организмд ATP ашиглах арга замыг авч үзэх;
· Харгалзах ATP утгахүн, амьтны биед зориулсан.
Бүлэг 1. ATP-ийн химийн шинж чанар, шинж чанар
1.1 ATP-ийн химийн шинж чанар
Аденозин трифосфат нь организм дахь энерги, бодисын солилцоонд онцгой чухал үүрэг гүйцэтгэдэг нуклеотид юм; Юуны өмнө нэгдэл нь хүн бүрийн эрчим хүчний бүх нийтийн эх үүсвэр гэдгээрээ алдартай биохимийн процессууд, амьд системд тохиолддог. ATP-ийг 1929 онд Карл Ломанн нээсэн бөгөөд 1941 онд Фриц Липман АТФ нь эсийн энергийн гол тээвэрлэгч гэдгийг харуулсан.
ATP-ийн системчилсэн нэр:
9-д-D-рибофураносиладенин-5"-трифосфат, эсвэл
9-д-D-рибофуранозил-6-амино-пурин-5"-трифосфат.
Химийн хувьд ATP нь аденозины трифосфатын эфир бөгөөд аденин ба рибозын дериватив юм.
Пурин азотын суурь - аденин нь рибозын 1" нүүрстөрөгчтэй β-N-гликозидын холбоогоор холбогддог. Фосфорын хүчлийн гурван молекул нь рибозын 5" нүүрстөрөгчтэй дараалан холбогддог бөгөөд үүнийг b, c үсгээр тэмдэглэв. болон г.
ATP-ийн бүтэц нь РНХ-ийн нэг хэсэг болох аденины нуклеотидтэй төстэй бөгөөд зөвхөн нэг фосфорын хүчлийн оронд ATP нь гурван фосфорын хүчлийн үлдэгдэл агуулдаг. Эсүүд нь мэдэгдэхүйц хэмжээгээр хүчил агуулдаггүй, харин зөвхөн давсыг агуулдаг. Тиймээс фосфорын хүчил нь ATP-д үлдэгдэл хэлбэрээр ордог (хүчлийн OH бүлгийн оронд сөрөг цэнэгтэй хүчилтөрөгчийн атом байдаг).
Ферментийн нөлөөн дор ATP молекул амархан гидролизд ордог, өөрөөр хэлбэл усны молекулыг холбож, аденозин дифосфорын хүчил (ADP) үүсгэхийн тулд задалдаг.
ATP + H2O ADP + H3PO4.
Өөр нэг фосфорын хүчлийн үлдэгдлийг арилгах нь ADP-ийг аденозин монофосфорын хүчил AMP болгон хувиргадаг.
ADP + H2O AMP + H3PO4.
Эдгээр урвалууд нь буцах боломжтой, өөрөөр хэлбэл AMP нь ADP болж хувирч, дараа нь ATP болж энерги хуримтлуулдаг. Ердийн пептидийн холбоог таслахад ердөө 12 кЖ/моль энерги ялгардаг. Фосфорын хүчлийн үлдэгдлийг холбодог холбоосууд нь өндөр энергитэй (тэдгээрийг өндөр энерги гэж нэрлэдэг): тус бүрийг устгахад 40 кЖ/моль энерги ялгардаг. Тиймээс ATP нь бүх нийтийн биологийн энерги хуримтлуулагч болох эсэд гол үүрэг гүйцэтгэдэг. ATP молекулууд нь митохондри болон хлоропластуудад нийлэгждэг (цитоплазмд зөвхөн бага хэмжээгээр нийлэгждэг), дараа нь эсийн янз бүрийн органеллд орж, бүх амин чухал үйл явцыг эрчим хүчээр хангадаг.
ATP-ийн энергийн улмаас эсийн хуваагдал, эсийн мембранаар бодисыг идэвхтэй дамжуулж, дамжуулах процессын явцад мембраны цахилгаан потенциалыг хадгалж байдаг. мэдрэлийн импульс, түүнчлэн өндөр молекулын нэгдлүүдийн биосинтез, физик ажил.
Ачаалал ихсэх үед (жишээлбэл, богино зайн гүйлтийн үед) булчингууд нь зөвхөн ATP-ийн нийлүүлэлтийн улмаас ажилладаг. Булчингийн эсүүдэд энэ нөөц нь хэдэн арван агшилтанд хангалттай бөгөөд дараа нь ATP-ийн хэмжээг нөхөх шаардлагатай. ADP ба AMP-аас ATP-ийн нийлэгжилт нь нүүрс ус, липид болон бусад бодисыг задлах явцад ялгардаг энергийн улмаас үүсдэг. Сэтгэцийн ажил гүйцэтгэхэд мөн их хэмжээний ATP шаардагдана. Энэ шалтгааны улмаас сэтгэцийн ажил эрхэлдэг хүмүүс глюкозын хэмжээг ихэсгэдэг бөгөөд задаргаа нь ATP-ийн нийлэгжилтийг баталгаажуулдаг.
1.2 ATP-ийн физик шинж чанар
ATP нь аденозин, рибоз ба гурван фосфатын бүлгээс бүрдэнэ. ATP нь усанд маш сайн уусдаг бөгөөд рН 6.8-7.4-ийн уусмалд нэлээд тогтвортой байдаг боловч хэт рН-д хурдан гидролиз болдог. Тиймээс ATP нь усгүй давсанд хамгийн сайн хадгалагддаг.
ATP нь тогтворгүй молекул юм. Буфергүй усанд энэ нь ADP болон фосфат болж гидролиз болдог. Учир нь ATP дахь фосфатын бүлгүүдийн хоорондох холбоо нь түүний бүтээгдэхүүн (ADP + фосфат) ба усны хоорондох устөрөгчийн холбоо (гидратын холбоо) -ын бат бөх чанараас бага байдаг. Тиймээс, хэрэв ATP ба ADP нь усан дахь химийн тэнцвэрт байдалд байвал бараг бүх ATP нь эцэстээ ADP болж хувирна. Тэнцвэрээс хол байгаа систем нь Гиббсийн чөлөөт энергийг агуулдаг бөгөөд ажил хийх чадвартай. Амьд эсүүд ATP ба ADP-ийн харьцааг тэнцвэрт байдлаас арав дахин өндөр түвшинд байлгадаг бөгөөд ATP-ийн концентраци нь ADP-ийн концентрациас мянга дахин их байдаг. Тэнцвэрийн байрлалаас ийнхүү шилжинэ гэдэг нь эс дэх ATP-ийн гидролиз нь их хэмжээний чөлөөт энерги ялгаруулдаг гэсэн үг юм.
ATP молекул дахь хоёр өндөр энергитэй фосфатын холбоо (зэргэлдээх фосфатуудыг холбодог) нь тухайн молекулын энергийн өндөр агууламжийг хариуцдаг. ATP-д хуримтлагдсан энергийг гидролизээр ялгаруулж болно. Рибозын сахараас хол зайд байрлах g-фосфатын бүлэг нь b- эсвэл b-фосфатаас илүү их гидролизийн энергитэй байдаг. ATP үлдэгдлийг гидролиз эсвэл фосфоржуулсны дараа үүссэн бонд нь бусад ATP бондоос бага энергитэй байдаг. Ферментийн катализаторын ATP гидролиз эсвэл ATP фосфоржилтын үед байгаа чөлөөт энергийг амьд системүүд ажил хийхэд ашиглаж болно.
Аливаа реактив молекулуудын тогтворгүй систем нь эсүүд урвалын тэнцвэрийн цэгээс хол зайд концентрацитай байсан бол чөлөөт энергийг хадгалах арга болж чадна. Гэсэн хэдий ч ихэнх полимер биомолекулуудын нэгэн адил РНХ, ДНХ, АТФ-ыг энгийн мономер болгон задлах нь энерги, энтропи ялгаруулж, стандарт концентраци болон эсэд агуулагдах концентрацийн аль алинд нь анхаарал хандуулдаг.
ATP гидролизийн үр дүнд гарсан энергийн стандарт хэмжээг байгалийн (стандарт) нөхцөлтэй холбоогүй энергийн өөрчлөлтөөс тооцоолж, дараа нь биологийн концентрацийг засч залруулж болно. АТФ-ыг ADP болон органик бус фосфат болгон задлахад дулааны энергийн (энтальпийн) цэвэр өөрчлөлт нь стандарт температур ба даралтын үед 20.5 кЖ/моль, чөлөөт энергийн өөрчлөлт нь 3.4 кЖ/моль байна. АТФ-аас фосфат эсвэл пирофосфатын задралаас ялгарах энерги нь улсын стандарт 1 М байна.
ATP + H 2 O > ADP + P i DG ? = - 30.5 кЖ/моль (-7.3 ккал/моль)
ATP + H 2 O > AMP + PP i DG ? = - 45.6 кЖ/моль (-10.9 ккал/моль)
Эдгээр утгыг физиологийн нөхцөлд болон эсийн ATP/ADP-ийн энергийн өөрчлөлтийг тооцоолоход ашиглаж болно. Гэсэн хэдий ч эрчим хүчний цэнэг гэж нэрлэгддэг илүү төлөөлөх ач холбогдол нь илүү олон удаа ажилладаг. Гиббсийн чөлөөт энергийн утгыг өгсөн. Эдгээр урвалууд нь нийт ионы хүч чадал, Mg 2+, Ca 2+ ион зэрэг шүлтлэг шороон металууд байгаа эсэх зэрэг олон хүчин зүйлээс хамаардаг. Хэвийн нөхцөлд DG нь ойролцоогоор -57 кЖ/моль (-14 ккал/моль) байна.
уургийн биологийн зайны энерги
Бүлэг 2. ATP үүсэх замууд
Бие махбодид ATP нь ADP-ийн фосфоржилтоор нийлэгждэг.
ADP + H 3 PO 4 + эрчим хүч> ATP + H 2 O.
ADP-ийн фосфоржилт нь субстратын фосфоржилт ба исэлдэлтийн фосфоржилт (исэлдүүлэгч бодисын энергийг ашиглах) гэсэн хоёр аргаар явагддаг. ATP-ийн ихэнх хэсэг нь H-аас хамааралтай ATP синтазын исэлдэлтийн фосфоржилтын үед митохондрийн мембран дээр үүсдэг. ATP-ийн субстратын фосфоржилт нь мембраны ферментийн оролцоог шаарддаггүй бөгөөд энэ нь гликолизийн үед эсвэл бусад өндөр энергитэй нэгдлүүдээс фосфатын бүлгийг шилжүүлэх замаар явагддаг.
ADP-ийн фосфоржилтын урвал, дараа нь ATP-ийг эрчим хүчний эх үүсвэр болгон ашиглах нь энергийн солилцооны мөн чанар болох мөчлөгийн процессыг бүрдүүлдэг.
Бие махбодид ATP нь байнга шинэчлэгддэг бодисуудын нэг юм. Тиймээс хүний хувьд нэг ATP молекулын амьдрах хугацаа 1 минутаас бага байдаг. Өдрийн туршид нэг ATP молекул дунджаар 2000-3000 мөчлөгийн дахин синтезийг туулдаг. Хүний биеӨдөрт 40 кг ATP нийлэгжүүлдэг), өөрөөр хэлбэл биед ATP-ийн нөөц бараг үүсдэггүй бөгөөд хэвийн амьдралын хувьд шинэ ATP молекулуудыг байнга синтезлэх шаардлагатай байдаг.
Исэлдэлтийн фосфоржилт -
Гэсэн хэдий ч нүүрс усыг ихэвчлэн субстрат болгон ашигладаг. Тиймээс тархины эсүүд нүүрс уснаас өөр хоол тэжээлийн субстратыг ашиглах боломжгүй байдаг.
Урьдчилан нийлмэл нүүрс ус нь энгийн нүүрсустөрөгчид задарч, глюкоз үүсэхэд хүргэдэг. Глюкоз нь эсийн амьсгалын үйл явц дахь бүх нийтийн субстрат юм. Глюкозын исэлдэлтийг 3 үе шатанд хуваадаг.
1. гликолиз;
2. исэлдэлтийн декарбоксилжилт ба Кребсийн мөчлөг;
3. исэлдэлтийн фосфоржилт.
Энэ тохиолдолд гликолиз нь аэробикийн нийтлэг үе шат юм агааргүй амьсгал.
2 .1.1 ГлicoЛиз- ATP-ийн синтез дагалддаг эс дэх глюкозыг дараалан задлах ферментийн процесс. Аэробик нөхцөлд гликолиз нь пирувийн хүчил (пируват), агааргүй нөхцөлд гликолиз нь сүүн хүчил (лактат) үүсэхэд хүргэдэг. Гликолиз нь амьтдын глюкозын катаболизмын гол зам юм.
Гликолизийн зам нь 10 дараалсан урвалаас бүрдэх бөгөөд тус бүр нь тусдаа ферментээр катализ болдог.
Гликолизийн үйл явцыг хоёр үе шатанд хувааж болно. 2 ATP молекулын эрчим хүчний хэрэглээтэй холбоотой эхний үе шат нь глюкозын молекулыг глицеральдегид-3-фосфатын 2 молекул болгон хуваахаас бүрдэнэ. Хоёрдахь шатанд глицеральдегид-3-фосфатын NAD-аас хамааралтай исэлдэлт явагдаж, ATP-ийн нийлэгжилт дагалддаг. Гликолиз нь өөрөө бүрэн агааргүй процесс бөгөөд өөрөөр хэлбэл урвал үүсэхийн тулд хүчилтөрөгч байх шаардлагагүй.
Гликолиз нь бараг бүх амьд организмд мэдэгддэг хамгийн эртний бодисын солилцооны процессуудын нэг юм. Гликолиз нь анхдагч прокариотуудад 3.5 тэрбум жилийн өмнө үүссэн гэж таамаглаж байна.
Гликолизийн үр дүн нь глюкозын нэг молекулыг пирувийн хүчлийн хоёр молекул (PVA) болгон хувиргаж, NADH коэнзим хэлбэрээр хоёр бууруулагч эквивалент үүсэх явдал юм.
Гликолизийн бүрэн тэгшитгэл нь:
C 6 H 12 O 6 + 2NAD + + 2ADP + 2P n = 2NAD H + 2PVK + 2ATP + 2H 2 O + 2H +.
Эсэд хүчилтөрөгч байхгүй эсвэл дутагдалтай тохиолдолд пирувийн хүчил нь сүүн хүчил болж буурдаг бөгөөд гликолизийн ерөнхий тэгшитгэл дараах байдалтай байна.
C 6 H 12 O 6 + 2ADP + 2P n = 2 лактат + 2ATP + 2H 2 O.
Тиймээс нэг глюкозын молекулын агааргүй задралын үед ATP-ийн нийт цэвэр гарц нь ADP-ийн субстратын фосфоржилтын урвалаар олж авсан хоёр молекул юм.
Аэробик организмд гликолизийн эцсийн бүтээгдэхүүн нь эсийн амьсгалтай холбоотой биохимийн мөчлөгт цаашдын өөрчлөлтөд ордог. Үүний үр дүнд нэг глюкозын молекулын бүх метаболитыг бүрэн исэлдүүлсний дараа эсийн амьсгалын сүүлчийн үе шатанд - митохондрийн исэлдэлтийн фосфоржилт үүсдэг. амьсгалын замын гинжхүчилтөрөгч байгаа тохиолдолд глюкозын молекул бүрт нэмэлт 34 эсвэл 36 ATP молекул нийлэгждэг.
Гликолизийн эхний урвал нь глюкозын молекулын фосфоржилт бөгөөд энэ нь 1 молекул ATP-ийн эрчим хүчний зарцуулалтаар эд эсийн өвөрмөц фермент гексокиназын оролцоотойгоор явагддаг; глюкозын идэвхтэй хэлбэр үүсдэг - глюкоз-6-фосфат (G-6-F):
Урвал үүсэхийн тулд ATP молекул нарийн холбогддог орчинд Mg 2+ ион байх шаардлагатай. Энэ урвал нь эргэлт буцалтгүй бөгөөд анхных юм түлхүүр урвал гликолиз.
Глюкозын фосфоржилт нь хоёр зорилготой: нэгдүгээрт, глюкозын төвийг сахисан молекулыг нэвчүүлдэг плазмын мембран нь сөрөг цэнэгтэй G-6-P молекулуудыг нэвтрүүлэхгүй байгаа тул фосфоржуулсан глюкоз нь эсийн дотор түгжигддэг. Хоёрдугаарт, фосфоржилтын үед глюкоз болж хувирдаг идэвхтэй хэлбэр, биохимийн урвалд оролцож, бодисын солилцооны мөчлөгт хамрагдах чадвартай.
Гексокиназын элэгний изоэнзим глюкокиназа нь цусан дахь глюкозын хэмжээг зохицуулахад чухал үүрэгтэй.
Дараагийн урвалд ( 2 ) ферментийн нөлөөгөөр G-6-P фосфоглюкоизомераза болж хувирдаг фруктоз 6-фосфат (F-6-F):
Энэ урвалд эрчим хүч шаардагдахгүй бөгөөд урвал нь бүрэн буцаагдах боломжтой. Асаалттай энэ үе шатандФруктоз нь фосфоржих замаар гликолизийн үйл явцад оролцдог.
Дараа нь хоёр урвал бараг тэр даруй дараалан явагдана: фруктоз-6-фосфатын эргэлт буцалтгүй фосфоржилт ( 3 ) болон үүссэн альдолын урвуу хуваагдал фруктоз 1,6-бифосфат (F-1.6-bF) хоёр гурвалсан ( 4 ).
P-6-P-ийн фосфоржилт нь өөр ATP молекулын энерги зарцуулалтаар фосфофруктокиназаар явагддаг; энэ бол хоёр дахь нь түлхүүр урвалгликолиз, түүний зохицуулалт нь бүхэлдээ гликолизийн эрчмийг тодорхойлдог.
Алдолын хуваагдал F-1.6-bFфруктоз-1,6-бисфосфат альдолазын нөлөөн дор үүсдэг.
Дөрөв дэх урвалын үр дүнд дигидроксиацетон фосфатТэгээд глицеральдегид-3-фосфат, эхнийх нь бараг шууд нөлөөнд автдаг фосфотриоз изомеразахоёрдугаарт очдог ( 5 ), цаашдын өөрчлөлтөд оролцдог:
Глицеральдегидийн фосфатын молекул бүр нь NAD+-аар исэлддэг. дегидрогеназууд глицеральдегид фосфатөмнө 1,3- гба фосфогликоз- харьцаа (6 ):
Дараа нь 1,3-дифосфоглицерат 1-р байрлалд өндөр энергитэй холбоо агуулсан фосфоглицератын киназа фермент нь фосфорын хүчлийн үлдэгдлийг ADP молекул руу шилжүүлдэг (урвал 7 ) - ATP молекул үүсдэг:
Энэ бол субстратын фосфоржилтын анхны урвал юм. Энэ мөчөөс эхлэн глюкозын задралын үйл явц нь эрчим хүчний хувьд ашиггүй байхаа больсон, учир нь эхний шатны эрчим хүчний зардлыг нөхдөг: 2 ATP молекул нийлэгждэг (1,3-дифосфоглицерат тус бүрд нэг) нийлэгждэг. урвалууд 1 Тэгээд 3 . Энэ урвал явагдахын тулд цитозолд ADP байх шаардлагатай, өөрөөр хэлбэл эсэд ATP илүүдэл (мөн ADP дутагдалтай) үед түүний хурд буурдаг. Метаболизмд ордоггүй ATP нь эсэд хуримтлагддаггүй, харин зүгээр л устгадаг тул энэ урвал нь гликолизийн чухал зохицуулагч юм.
Дараа нь дараалан: фосфоглицерин мутаза үүсдэг 2-фосфо- глицерат (8 ):
Энолазын хэлбэрүүд фосфоенолпируват (9 ):
Эцэст нь ADP-ийн субстратын фосфоржилтын хоёр дахь урвал нь пируват ба ATP-ийн энол хэлбэр үүсэх замаар явагддаг. 10 ):
Пируват киназын үйл ажиллагааны дор урвал явагдана. Энэ бол гликолизийн сүүлчийн гол урвал юм. Пируватын энол хэлбэрийг пируват болгон изомержих нь ферментийн бус аргаар явагддаг.
Үүссэн цагаасаа хойш F-1.6-bFЗөвхөн энерги ялгаруулдаг урвал явагддаг 7 Тэгээд 10 , үүнд субстрат үүсдэг ADP фосфоржилт.
Зохицуулалт гликолиз
Орон нутгийн болон ерөнхий зохицуулалт байдаг.
Орон нутгийн зохицуулалтыг эсийн доторх янз бүрийн метаболитуудын нөлөөн дор ферментийн үйл ажиллагааг өөрчлөх замаар гүйцэтгэдэг.
Гликолизийн зохицуулалт нь бүхэлдээ, бүхэл бүтэн организмын хувьд гормоны нөлөөн дор явагддаг бөгөөд энэ нь хоёрдогч элчийн молекулуудаар дамжин эсийн доторх бодисын солилцоог өөрчилдөг.
Инсулин нь гликолизийг өдөөхөд чухал үүрэг гүйцэтгэдэг. Глюкагон ба адреналин нь гликолизийн хамгийн чухал дааврын дарангуйлагч юм.
Инсулин нь дараахь байдлаар гликолизийг өдөөдөг.
· гексокиназын урвалыг идэвхжүүлэх;
· фосфофруктокиназыг өдөөх;
· пируват киназын өдөөлт.
Бусад гормонууд нь гликолизэд нөлөөлдөг. Жишээлбэл, соматотропин нь гликолитик ферментийг дарангуйлдаг ба бамбай булчирхайн даавар нь өдөөгч юм.
Гликолизийг хэд хэдэн үндсэн үе шаттайгаар зохицуулдаг. Гексокиназын катализаторын урвалууд ( 1 ), фосфофруктокиназа ( 3 ) ба пируват киназа ( 10 ) нь чөлөөт энергийн мэдэгдэхүйц бууралтаар тодорхойлогддог бөгөөд бараг эргэлт буцалтгүй байдаг нь гликолизийн зохицуулалтын үр дүнтэй цэгүүд болох боломжийг олгодог.
Гликолиз бол онцгой ач холбогдолтой катаболик зам юм. Энэ нь эсийн урвал, түүний дотор уургийн нийлэгжилтийг эрчим хүчээр хангадаг. Гликолизийн завсрын бүтээгдэхүүнийг өөхний нийлэгжилтэнд ашигладаг. Пируватыг мөн аланин, аспартат болон бусад нэгдлүүдийг нэгтгэхэд ашиглаж болно. Гликолизийн ачаар митохондрийн гүйцэтгэл, хүчилтөрөгчийн хүртээмж нь богино хугацааны хэт ачааллын үед булчингийн хүчийг хязгаарладаггүй.
2.1.2 Исэлдэлтийн декарбоксилжилт - пируватыг ацетил-КоА болтол исэлдүүлэх нь пируватдегидрогеназын цогцолбор гэж нэрлэгддэг олон ферментийн системд бүтцийн хувьд нэгдсэн олон тооны фермент, коэнзимийн оролцоотойгоор явагддаг.
Энэ үйл явцын I үе шатанд пируват дегидрогеназа (E 1) ферментийн идэвхтэй төвд тиамин пирофосфат (TPP) -тэй харилцан үйлчлэлийн үр дүнд пируват нь карбоксил бүлгээ алддаг. II үе шатанд E 1 -TPP-CHOH-CH 3 цогцолборын оксиэтил бүлэг исэлдэж ацетил бүлэг үүсгэх ба энэ нь нэгэн зэрэг дигидролипойлацетилтрансфераза (E 2) ферменттэй холбоотой липойн хүчлийн амид (коэнзим) руу шилждэг. Энэ фермент нь 3-р үе шатыг катализ болгодог - ацетил бүлгийг коэнзим КоА (HS-KoA) руу шилжүүлэх замаар эцсийн бүтээгдэхүүн ацетил-КоА үүсэх ба энэ нь өндөр энергитэй (макроэргик) нэгдэл юм.
IV үе шатанд липомиидын исэлдсэн хэлбэр нь буурсан дигидролипоамид-Е 2 цогцолбороос сэргээгддэг. Дихидролипоил дегидрогеназа (E 3) ферментийн оролцоотойгоор устөрөгч нь дигидролипомиидын бууруулсан сульфгидрил бүлгээс FAD руу шилждэг бөгөөд энэ нь энэ ферментийн протезийн бүлэг болж, түүнтэй нягт холбоотой байдаг. V үе шатанд буурсан FADH 2 дигидро-липойлдегидрогеназа нь устөрөгчийг коэнзим NAD руу шилжүүлж, NADH + H + үүсгэдэг.
Пируватыг исэлдэлтийн декарбоксилжих процесс нь митохондрийн матрицад явагддаг. Үүнд 3 фермент (пируват дегидрогеназа, дигидролипоил ацетилтрансфераза, дигидролипоил дегидрогеназа) ба 5 коэнзим (TPF, липоид хүчлийн амид, коэнзим А, FAD ба NAD) багтдаг (нийтлэг олон ферментийн цогцолборын нэг хэсэг), тэдгээрийн гурав нь ферменттэй харьцангуй нягт холбоотой байдаг. (TPF-E 1, lipoamide-E 2 ба FAD-E 3), хоёр нь амархан салдаг (HS-KoA ба NAD).
Цагаан будаа. 1 Пируватдегидрогеназын цогцолборын үйл ажиллагааны механизм
E 1 - пируватдегидрогеназа; E 2 - ди-гидролипойлацетилтрансфераза; E 3 - дигидролипойлдегидрогеназа; Тойрог доторх тоо нь үйл явцын үе шатуудыг заана.
Дэд бүтэцтэй эдгээр бүх ферментүүд, коэнзимүүд нь нэг цогцолбор болж зохион байгуулагдсан байдаг. Тиймээс завсрын бүтээгдэхүүнүүд хоорондоо хурдан харьцах чадвартай байдаг. Цогцолборыг бүрдүүлдэг дигидролипойл ацетилтрансферазын дэд хэсгүүдийн полипептидийн гинж нь цогцолборын цөмийг бүрдүүлдэг бөгөөд тэдгээрийн эргэн тойронд пируватдегидрогеназа ба дигидролипойлдегидрогеназа байрладаг нь батлагдсан. Төрөлхийн ферментийн цогцолборыг өөрөө угсрах замаар бүрдүүлдэг гэж ерөнхийд нь хүлээн зөвшөөрдөг.
Пируватдегидрогеназын цогцолборын катализаторын ерөнхий урвалыг дараах байдлаар илэрхийлж болно.
Пируват + NAD + + HS-CoA - > Ацетил-КоА + NADH + H + + CO 2.
Урвал нь стандарт чөлөөт энергийн мэдэгдэхүйц бууралт дагалддаг бөгөөд бараг эргэлт буцалтгүй байдаг.
Исэлдэлтийн декарбоксилжилтын үед үүссэн ацетил-КоА нь CO 2 ба H 2 O үүсэх замаар цааш исэлдэлтэнд ордог. Ацетил-КоА-ийн бүрэн исэлдэлт нь трикарбоксилын хүчлийн мөчлөгт (Кребсийн мөчлөг) явагддаг. Энэ процесс, түүнчлэн пируватын исэлдэлтийн декарбоксилжилт нь эсийн митохондрид явагддаг.
2 .1.3 ЦиклтрикарбонисгэлэнТ (мөчлөг Crebsa, ятгазузаан мөчлөг) - төв хэсэгкатаболизмын ерөнхий зам, нүүрс ус, өөх тос, уураг задрах явцад амьд организмд үүссэн хоёр ба гурван нүүрстөрөгчийн нэгдлүүдийг СО 2 болгон хувиргах циклик биохимийн аэробик процесс. Энэ тохиолдолд ялгарсан устөрөгчийг эд эсийн амьсгалын гинжин хэлхээнд илгээж, улмаар ус руу исэлдэж, бүх нийтийн эрчим хүчний эх үүсвэр болох ATP-ийн нийлэгжилтэнд шууд оролцдог.
Кребсын мөчлөг нь хүчилтөрөгч хэрэглэдэг бүх эсүүдийн амьсгалын гол үе шат бөгөөд бие махбод дахь бодисын солилцооны олон замуудын огтлолцол юм. Цикл нь эрчим хүчний чухал үүрэг гүйцэтгэхээс гадна чухал ач холбогдолтой хуванцар функцтэй, өөрөөр хэлбэл энэ нь бусад биохимийн өөрчлөлтүүдийн үед эсийн амьдралд чухал ач холбогдолтой нэгдлүүдийг нийлэгжүүлдэг урьдал молекулуудын чухал эх үүсвэр юм. амин хүчил, нүүрс ус, өөх тосны хүчил гэх мэт.
Өөрчлөлтийн мөчлөг Лимонхүчиламьд эсийг Германы биохимич Сэр Ханс Кребс нээж, судалсан бөгөөд энэ ажлынхаа төлөө тэрээр (Ф. Липмантай хамт) шагнагджээ. Нобелийн шагнал(1953).
Эукариотуудад Кребсийн мөчлөгийн бүх урвалууд митохондри дотор явагддаг бөгөөд нэгээс бусад нь тэдгээрийг катализатор болгодог ферментүүд нь митохондрийн дотоод мембран дээр байрладаг сукцинат дегидрогеназаас бусад нь митохондрийн матрицад чөлөөт төлөвт байдаг. липидийн давхар давхарга. Прокариотуудад мөчлөгийн урвалууд цитоплазмд явагддаг.
Кребсийн мөчлөгийн нэг эргэлтийн ерөнхий тэгшитгэл нь:
Ацетил-КоА > 2CO 2 + CoA + 8e ?
Зохицуулалт мөчлөгА:
Кребсийн мөчлөгийг "сөрөг хариу урвалын механизмаар" зохицуулдаг; их хэмжээний субстрат (ацетил-КоА, оксалоацетат) байгаа тохиолдолд цикл идэвхтэй ажилладаг ба урвалын бүтээгдэхүүн (NAD, ATP) илүүдэлтэй үед. энэ нь саатуулдаг. Зохицуулалт нь гормоны тусламжтайгаар хийгддэг; ацетил-КоА-ийн гол эх үүсвэр нь глюкоз тул глюкозын аэробик задралыг дэмждэг дааварууд нь Кребсийн мөчлөгийн үйл ажиллагаанд хувь нэмэр оруулдаг. Эдгээр гормонууд нь:
· инсулин;
· адреналин.
Глюкагон нь глюкозын нийлэгжилтийг идэвхжүүлж, Кребсийн мөчлөгийн урвалыг саатуулдаг.
Дүрмээр бол циклийг субстратаар дүүргэдэг анаплеротик урвалын улмаас Кребсийн мөчлөгийн ажил тасалддаггүй.
Пируват + CO 2 + ATP = Оксалоацетат (Кребс циклийн субстрат) + ADP + Fn.
Ажил ATP синтаза
Исэлдэлтийн фосфоржилтын процессыг 5 төрлийн 9 дэд нэгжээс бүрдэх митохондрийн амьсгалын замын гинжин хэлхээний тав дахь цогцолбор - Протон ATP синтаза гүйцэтгэдэг.
3 дэд нэгж (d, e, f) нь ATP синтазын бүрэн бүтэн байдалд хувь нэмэр оруулдаг
· Дэд нэгж нь үндсэн функциональ нэгж юм. Энэ нь 3 тохироотой:
· L-конформаци - ADP ба фосфатыг хавсаргана (тусгай тээвэрлэгчийг ашиглан цитоплазмаас митохондрид орох)
Т-конформаци - фосфат нь ADP-тэй нэгдэж, ATP үүсдэг
· О-конформаци - ATP нь b дэд нэгжээс салж, b дэд нэгж рүү шилждэг.
· Дэд нэгж нь конформацаа өөрчлөхийн тулд устөрөгчийн протон шаардлагатай, учир нь конформаци 3 удаа өөрчлөгддөг тул 3 устөрөгчийн протон шаардлагатай. Протонууд нь цахилгаан химийн потенциалын нөлөөн дор митохондрийн мембран хоорондын зайнаас шахагддаг.
· b-дэд нэгж нь ATP-ийг мембран зөөвөрлөгч рүү зөөвөрлөх ба энэ нь цитоплазм руу ATP-ийг “шиддэг”. Үүний хариуд ижил тээвэрлэгч нь цитоплазмаас ADP-ийг тээвэрлэдэг. Митохондрийн дотоод мембран нь цитоплазмаас митохондри руу чиглэсэн фосфатын тээвэрлэгчийг агуулдаг боловч түүний үйл ажиллагаанд устөрөгчийн протон шаардлагатай байдаг. Ийм тээвэрлэгчийг транслоказ гэж нэрлэдэг.
Нийт гарах
1 ATP молекулыг нэгтгэхийн тулд 3 протон шаардлагатай.
Дарангуйлагчид исэлдүүлэх фосфоржилт
Дарангуйлагчид V цогцолборыг блоклодог:
· Олигомицин - ATP синтазын протоны сувгийг блоклодог.
· Атратилозид, циклофиллин - транслоказыг блоклодог.
Салгагч исэлдүүлэх фосфоржилт
Салгагч- протоныг хүлээн авч, митохондрийн дотоод мембранаар дамжуулж, V цогцолборыг (түүний протоны суваг) дамжих чадвартай липофиль бодисууд. Салгагч:
· Байгалийн- липидийн хэт исэлдлийн бүтээгдэхүүн; өөх тосны хүчилурт гинжтэй; бамбай булчирхайн дааврын их тунгаар.
· Хиймэл- динитрофенол, эфир, витамин К дериватив, мэдээ алдуулагч.
2.2 Субстратын фосфоржилт
СубстратА нарийнфосфорилТэгээд сэлүүрт (биохимийн), гликолизийн исэлдэлтийн урвалын энерги (фосфоглицеральдегиддегидрогеназа ба энолазагаар катализлагдсан) болон трикарбоксилын хүчлийн мөчлөгт а-кетоглутарийн хүчлийг исэлдүүлэх явцад (а-кетоглутаратын нөлөөн дор) эрчим хүчээр баялаг фосфорын нэгдлүүдийн нийлэгжилт. ба сукцинат тиокиназа). Бактерийн хувьд S. f.-ийн тохиолдлуудыг тодорхойлсон. пирувийн хүчлийн исэлдэлтийн үед.C. е., электрон тээвэрлэх гинжин хэлхээнд фосфоржилтоос ялгаатай нь, Энэ нь хордлогын нөлөөгөөр (жишээлбэл, динитрофенол) дарангуйлагддаггүй бөгөөд митохондрийн мембран дахь ферментийг бэхлэхтэй холбоогүй байдаг. S. f-ийн оруулсан хувь нэмэр. аэробикийн нөхцөлд эсийн ATP санд оруулах хувь нэмэр нь электрон тээвэрлэлтийн гинжин хэлхээнд фосфоржилтын хувь нэмэрээс хамаагүй бага юм.
Бүлэг 3. ATP ашиглах арга замууд
3.1 Эс дэх үүрэг
Бие дэх ATP-ийн гол үүрэг нь олон тооны биохимийн урвалыг эрчим хүчээр хангахтай холбоотой юм. Хоёр өндөр энергийн холбоог зөөвөрлөгчийн хувьд ATP нь эрчим хүч зарцуулдаг олон биохими, физиологийн процессуудад шууд эрчим хүчний эх үүсвэр болдог. Энэ бүхэн нь бие махбод дахь нарийн төвөгтэй бодисуудын нийлэгжилтийн урвал юм: молекулуудыг идэвхтэй дамжуулах үйл явц юм. биологийн мембранууд, үүнд трансмембран цахилгаан потенциалыг бий болгох; булчингийн агшилтын хэрэгжилт.
Амьд организмын био энергид мэдэгдэж байгаачлан хоёр гол зүйл чухал байдаг.
a) химийн энерги нь органик субстратын исэлдэлтийн экзергон катаболик урвалын хамт ATP үүсэх замаар хадгалагддаг;
б) химийн энергийг АТФ задрах, анаболизмын эндергоник урвалууд болон бусад эрчим хүч шаарддаг үйл явцын хамт ашигладаг.
Яагаад ATP молекул биоэнергетикийн гол үүргээ гүйцэтгэдэг вэ гэсэн асуулт гарч ирнэ. Үүнийг шийдэхийн тулд ATP-ийн бүтцийг авч үзье Бүтэц ATP - (цагт рН 7,0 тетра цэнэг анион) .
ATP нь термодинамик тогтворгүй нэгдэл юм. ATP-ийн тогтворгүй байдал нь нэгдүгээрт, ижил нэртэй сөрөг цэнэгийн бөөгнөрөл дэх электростатик түлхэлтээр тодорхойлогддог бөгөөд энэ нь бүх молекулын хурцадмал байдалд хүргэдэг боловч холбоо нь хамгийн хүчтэй байдаг - P - O - P, хоёрдугаарт, тодорхой резонансаар. Сүүлчийн хүчин зүйлийн дагуу фосфорын атомуудын хооронд байрладаг хүчилтөрөгчийн атомын хуваагдаагүй хөдөлгөөнт электронуудын төлөөх өрсөлдөөн байдаг, учир нь фосфорын атом бүр хэсэгчилсэн байдаг. эерэг цэнэг P=O ба P - O- бүлгийн электрон рецепторын мэдэгдэхүйц нөлөөллөөс шалтгаална. Тиймээс ATP оршин тогтнох боломжийг молекул дахь эдгээр физик-химийн стрессийг нөхөх хангалттай хэмжээний химийн энерги байгаагаар тодорхойлдог. ATP молекул нь хоёр фосфоангидрид (пирофосфат) холбоог агуулдаг бөгөөд тэдгээрийн гидролиз нь чөлөөт энергийн мэдэгдэхүйц бууралт (рН 7.0 ба 37 ° C) дагалддаг.
ATP + H 2 O = ADP + H 3 PO 4 G0I = - 31.0 КЖ/моль.
ADP + H 2 O = AMP + H 3 PO 4 G0I = - 31.9 КЖ/моль.
Био энергийн гол асуудлын нэг бол амьд байгальд ADP-ийн фосфоржилтоор явагддаг ATP-ийн биосинтез юм.
ADP-ийн фосфоржилт нь эндергоник процесс бөгөөд эрчим хүчний эх үүсвэр шаарддаг. Өмнө дурьдсанчлан байгальд ийм хоёр эрчим хүчний эх үүсвэр давамгайлдаг - эдгээр нь нарны эрчим хүчболон багассан органик нэгдлүүдийн химийн энерги. Ногоон ургамал болон зарим бичил биетүүд шингэсэн гэрлийн квантуудын энергийг химийн энерги болгон хувиргах чадвартай бөгөөд энэ нь фотосинтезийн гэрлийн үе шатанд ADP-ийн фосфоржилтод зарцуулагддаг. ATP нөхөн төлжих энэ үйл явцыг фотосинтезийн фосфоржилт гэж нэрлэдэг. Органик нэгдлүүдийн исэлдэлтийн энергийг аэробикийн нөхцөлд ATP-ийн макроэнергетик холбоо болгон хувиргах нь үндсэндээ исэлдэлтийн фосфоржилтоор дамждаг. ATP үүсэхэд шаардагдах чөлөөт энерги нь митохондри дахь амьсгалын исэлдэлтийн гинжин хэлхээнд үүсдэг.
ATP синтезийн өөр нэг хэлбэрийг субстратын фосфоржилт гэж нэрлэдэг. Электрон дамжуулалттай холбоотой исэлдэлтийн фосфоржилтоос ялгаатай нь ATP-ийг нөхөн сэргээхэд шаардлагатай идэвхжүүлсэн фосфорын бүлгийн донор (- PO3 H2) нь гликолиз ба трикарбоксилын хүчлийн мөчлөгийн завсрын хэсэг юм. Эдгээр бүх тохиолдолд исэлдэлтийн процессууд нь өндөр энергитэй нэгдлүүд үүсэхэд хүргэдэг: 1,3-дифосфоглицерат (гликолиз), сукцинил-КоА (трикарбоксилын хүчлийн мөчлөг), эдгээр нь зохих ферментийн оролцоотойгоор ADP болон фолиляци хийх чадвартай. ATP үүсгэдэг. Субстратын түвшинд энерги хувирах нь агааргүй организмд ATP синтезийн цорын ганц арга зам юм. ATP синтезийн энэхүү үйл явц нь эрчимтэй ажлыг дэмжих боломжийг олгодог араг ясны булчингуудхүчилтөрөгчийн өлсгөлөнгийн үед. Энэ нь митохондригүй боловсорч гүйцсэн улаан эсийн ATP синтезийн цорын ганц зам гэдгийг санах нь зүйтэй.
Фосфорын хүчлийн хоёр үлдэгдэл нэгддэг аденил нуклеотид нь эсийн биоэнергетикт онцгой чухал үүрэг гүйцэтгэдэг. Энэ бодисыг аденозин трифосфорын хүчил (ATP) гэж нэрлэдэг. Органик фосфоритыг салгахад ялгардаг ATP молекулын фосфорын хүчлийн үлдэгдэл хоорондын химийн холбоонд энерги хуримтлагддаг.
ATP = ADP+P+E,
Энд F нь фермент, E нь ялгаруулах энерги юм. Энэ урвалын үед аденозин фосфорын хүчил (ADP) үүсдэг - ATP молекулын үлдэгдэл ба органик фосфат. Бүх эсүүд ATP энергийг биосинтезийн үйл явц, хөдөлгөөн, дулаан үйлдвэрлэх, мэдрэлийн импульс, гэрэлтэх (жишээлбэл, гэрэлтдэг бактери), өөрөөр хэлбэл бүх амин чухал үйл явцад ашигладаг.
ATP бол бүх нийтийн биологийн энергийн хуримтлуулагч юм. Хэрэглэсэн хоолонд агуулагдах гэрлийн энерги нь ATP молекулуудад хадгалагддаг.
Эс дэх ATP-ийн нийлүүлэлт бага байдаг. Тиймээс булчин дахь ATP нөөц нь 20-30 агшилтанд хангалттай байдаг. Хүчтэй, гэхдээ богино хугацааны ажил хийх үед булчингууд нь зөвхөн тэдгээрт агуулагдах ATP задралын улмаас ажилладаг. Ажил дууссаны дараа хүн маш их амьсгалдаг - энэ хугацаанд нүүрс ус болон бусад бодисууд задарч (эрчим хүч хуримтлагдаж), эсийн ATP-ийн хангамж сэргээгддэг.
ATP нь синапс дахь дамжуулагчийн үүргийг бас мэддэг.
3.2 Ферментийн үйл ажиллагаанд гүйцэтгэх үүрэг
Амьд эс тэнцвэрт байдлаас хол байдаг химийн систем: Эцсийн эцэст, амьд систем тэнцвэрт байдалд ойртох нь түүний задрал, үхэл гэсэн үг юм. Фермент бүрийн бүтээгдэхүүн нь бодисын солилцооны замд өөр ферментээр субстрат болгон ашигладаг тул ихэвчлэн хурдан зарцуулагддаг. Хамгийн чухал нь олон тооны ферментийн урвалууд нь ATP-ийг ADP болон органик бус фосфат болгон задалдаг. Үүнийг хэрэгжүүлэхийн тулд ATP-ийн санг тэнцвэрт байдлаас хол түвшинд байлгах шаардлагатай бөгөөд ингэснээр ATP-ийн концентраци болон түүний гидролизийн бүтээгдэхүүний концентрацийн харьцаа өндөр байна. Тиймээс ATP усан сан нь ферментийн оролцоотойгоор тодорхойлогддог бодисын солилцооны замын дагуу энерги, атомыг эсэд тогтмол шилжүүлдэг "батерей" үүрэг гүйцэтгэдэг.
Тиймээс, ATP гидролизийн үйл явц, түүний ферментийн үйл ажиллагаанд үзүүлэх нөлөөг авч үзье. Хоёр мономер болох А ба В нь бие биентэйгээ усгүйжүүлэлтийн урвалаар (конденсаци гэж нэрлэдэг) нэгдэж ус ялгарах ердийн биосинтетик процессыг төсөөлөөд үз дээ.
A - N + B - OH - AB + H2O
Усны молекул нь ковалент холболттой A - B нэгдлийг задалдаг гидролиз гэж нэрлэгддэг урвуу урвал нь бараг үргэлж энергийн хувьд таатай байх болно. Энэ нь жишээлбэл, уургийн гидролизийн задралын үед тохиолддог. нуклейн хүчилболон полисахаридууд нь дэд хэсгүүдэд хуваагдана.
A - B эсүүд A - H ба B - OH-тэй үүсэх ерөнхий стратеги нь олон үе шаттай урвалын дарааллыг агуулдаг бөгөөд үүний үр дүнд n Шаардлагатай нэгдлүүдийн энергийн тааламжгүй синтезийг тэнцвэртэй ашигтай урвалтай холбодог.
ATP гидролиз нь их хэмжээний сөрөг утгатай тохирч байна уу? Тиймээс ATP гидролиз нь ихэвчлэн энергийн таатай урвалын үүрэг гүйцэтгэдэг бөгөөд үүний улмаас эсийн доторх биосинтезийн урвал явагддаг.
ATP гидролизтэй холбоотой A - H ба B - OH - A - B замд гидролизийн энерги нь эхлээд B - OH-ийг өндөр энергитэй завсрын бүтээгдэхүүн болгон хувиргаж, дараа нь A - H -тэй шууд урвалд орж A - B үүсгэдэг. Энэ үйл явцын энгийн механизм нь B - OPO 3 эсвэл B - O - P үүсэх замаар фосфатыг ATP-ээс B - OH руу шилжүүлэх явдал бөгөөд энэ тохиолдолд нийт урвал зөвхөн хоёр үе шаттайгаар явагдана.
1) B - OH + ATP - B - B - P + ADP
2) A - N + B - O - R - A - B + R
Урвалын явцад үүссэн B - O - P завсрын нэгдэл дахин устдаг тул ерөнхий урвалыг дараах тэгшитгэлээр тодорхойлж болно.
3) A-N + B - OH - A - B ба ATP - ADP + P
Эхний, энергийн хувьд тааламжгүй урвал нь хоёр дахь, энергийн хувьд таатай урвал (ATP гидролиз) -тэй холбоотой тул боломжтой болж хувирдаг. Энэ төрлийн хосолсон биосинтетик урвалын жишээ бол амин хүчлийн глютамины нийлэгжилт юм.
ADP ба органик бус фосфат хүртэлх ATP-ийн гидролизийн G утга нь бүх урвалд орж буй бодисын концентрацаас хамаардаг бөгөөд ихэвчлэн эсийн нөхцөлд - 11-13 ккал / моль хооронд хэлбэлздэг. ATP гидролизийн урвалыг эцэст нь G-ийн утга нь ойролцоогоор +10 ккал/моль байх термодинамикийн хувьд тааламжгүй урвал явуулахад ашиглаж болно, мэдээжийн хэрэг зохих урвалын дараалал байгаа тохиолдолд. Гэсэн хэдий ч олон биосинтезийн урвалын хувьд энэ нь хангалтгүй юм уу? G = - 13 ккал/моль. Эдгээр болон бусад тохиолдолд ATP-ийн гидролизийн замыг өөрчилснөөр эхлээд AMP ба РР (пирофосфат) үүсдэг. Дараагийн шатанд пирофосфат нь мөн гидролизд ордог; бүх процессын нийт чөлөөт энергийн өөрчлөлт нь ойролцоогоор - 26 ккал/моль.
Пирофосфатын гидролизийн энергийг биосинтетик урвалд хэрхэн ашигладаг вэ? Аргын аль нэгийг A - H ба B - OH-тэй A - B нэгдлүүдийн нийлэгжилтийн жишээгээр харуулж болно. Зохих ферментийн тусламжтайгаар B - OH нь ATP-тэй урвалд орж, B - O - P - P өндөр энергитэй нэгдэл болж хувирдаг. Одоо урвал нь гурван үе шатаас бүрдэнэ.
1) B - OH + ATP - B - B - P - P + AMP
2) A - N + B - O - R - R - A - B + RR
3) PP + H2O - 2P
Нийт урвалыг дараах байдлаар илэрхийлж болно.
A - H + B - OH - A - B ба ATP + H2O - AMP + 2P
Фермент нь катализаторын урвалыг урагш болон урвуу чиглэлд үргэлж хурдасгадаг тул A - B нэгдэл нь пирофосфаттай урвалд орж задарч болно (урвал, 2-р алхамын урвуу). Гэсэн хэдий ч пирофосфатын гидролизийн эрч хүчтэй эерэг урвал (3-р шат) нь тогтвортой байдлыг хадгалахад тусалдаг. A-B холболтуудпирофосфатын концентраци маш бага хэвээр байгаа тул (энэ нь 2-р алхамаас урвуу урвал үүсэхээс сэргийлдэг). Тиймээс пирофосфатын гидролизийн энерги нь урвал урагшлах чиглэлд явагддаг. Энэ төрлийн биосинтезийн чухал урвалын жишээ бол полинуклеотидын нийлэгжилт юм.
3.3 ДНХ, РНХ, уургийн нийлэгжилтэнд гүйцэтгэх үүрэг
Мэдэгдэж байгаа бүх организмд ДНХ-ийг бүрдүүлдэг дезоксирибонуклеотидууд нь холбогдох рибонуклеотидууд дээр рибонуклеотид редуктаза (RNR) ферментийн үйлчлэлээр нийлэгждэг. Эдгээр ферментүүд нь 2" гидроксил бүлэг, рибонуклеозидын дифосфатын субстрат, дезоксирибонуклеозидын дифосфатын бүтээгдэхүүнээс хүчилтөрөгчийг зайлуулж, элсэн чихрийн үлдэгдлийг отирибозыг дезоксирибоз болгон бууруулдаг. Бүх редуктаза ферментүүд нь реактив исэлдүүлсэн цистеин болон задралын урвалд ордог сульфгидрил радикал механизмыг ашигладаг. урвалын үед.РНР ферментийг тиоредоксин эсвэл глутаредоксинтэй урвалд оруулан боловсруулдаг.
RHP болон холбогдох ферментүүдийн зохицуулалт нь бие биентэйгээ тэнцвэрийг хадгалж байдаг. Маш бага концентраци нь ДНХ-ийн нийлэгжилт, ДНХ-ийн засварыг саатуулж, эсийг үхэлд хүргэдэг бол хэвийн бус харьцаа нь ДНХ-ийн нийлэгжилтийн явцад ДНХ полимеразыг оруулах магадлал ихэсдэг тул мутаген шинж чанартай байдаг.
РНХ-ийн нуклейн хүчлүүдийн нийлэгжилтийн явцад АТФ-аас гаргаж авсан аденозин нь РНХ полимеразагаар шууд РНХ молекулд нэгддэг дөрвөн нуклеотидын нэг юм. Эрчим хүч, энэ полимержилт нь пирофосфатыг (хоёр фосфатын бүлэг) арилгахад тохиолддог. Энэ үйл явц нь ДНХ-ийн биосинтезтэй төстэй бөгөөд зөвхөн ATP нь ДНХ-д нэгдэхээсээ өмнө дезоксирибонуклеотид dATP болж буурдаг.
IN синтез хэрэм. Аминоацил-тРНХ-ийн синтетазууд нь трибосом руу шилжихэд бэлэн аминоацил-тРНХ-ийг үүсгэн, тРНХ молекулыг тодорхой амин хүчилд холбохын тулд ATP ферментийг энергийн эх үүсвэр болгон ашигладаг. Хоёр фосфатын бүлгийг зайлуулдаг аденозин монофосфат (AMP) -ээр ATP-ийн гидролизийн үр дүнд эрчим хүч гарч ирдэг.
ATP нь эсийн мембранаар дамжин хөдөлж буй бодисыг зөөвөрлөх зэрэг эсийн олон үйл ажиллагаанд ашиглагддаг. Мөн булчингийн агшилтанд шаардлагатай энергийг хангах механик ажилд ашигладаг. Энэ нь зөвхөн зүрхний булчин (цусны эргэлтэнд) болон араг ясны булчингуудад (жишээлбэл, биеийн нийт хөдөлгөөнд) төдийгүй хромосом, тугуудыг эрчим хүчээр хангадаг бөгөөд ингэснээр тэдгээр нь олон үүргээ гүйцэтгэх боломжтой болдог. ATP-ийн гол үүрэг нь химийн ажилд оршдог бөгөөд эсэд байх ёстой хэдэн мянган төрлийн макромолекулуудыг нийлэгжүүлэхэд шаардлагатай энергийг өгдөг.
ATP нь химийн урвалыг хянах, мэдээлэл дамжуулах зэрэгт асаах унтраалга болгон ашигладаг. Амьдралд хэрэглэгддэг барилгын материал болон бусад бүтцийг бий болгодог уургийн гинжний хэлбэр нь ихэвчлэн амархан арилдаг, өөрчлөгддөг сул химийн холбоогоор тодорхойлогддог. Эдгээр хэлхээ нь эрчим хүчний оролт, гаралтын хариуд богиносгож, уртасч, хэлбэрээ өөрчилж болно. Гинжин хэлхээний өөрчлөлт нь уургийн хэлбэрийг өөрчлөхөөс гадна түүний үйл ажиллагааг өөрчлөх эсвэл идэвхтэй эсвэл идэвхгүй болгоход хүргэдэг.
ATP молекулууд нь уургийн молекулын нэг хэсэгтэй холбогдож, ижил молекулын өөр нэг хэсэг нь бага зэрэг гулсаж, хөдөлж, улмаар молекулыг идэвхгүй болгож, конформацийг нь өөрчилдөг. Устгасны дараа ATP нь уураг анхны хэлбэрт нь буцаахад хүргэдэг бөгөөд ингэснээр дахин үйл ажиллагаагаа явуулдаг.
Молекул буцаж ирэх хүртэл циклийг давтаж болох бөгөөд энэ нь асаах/унтраах товчлуурын үүрэг гүйцэтгэдэг. Фосфор нэмэх (фосфоризаци) болон уурагаас фосфорыг зайлуулах (дефосфоризаци) хоёулаа асаах, унтраах үүрэг гүйцэтгэдэг.
3.4 ATP-ийн бусад функцууд
Үүрэг В бодисын солилцоо, синтез Тэгээд идэвхтэй тээвэрлэлт
Тиймээс ATP нь орон зайн тусгаарлагдсан бодисын солилцооны урвалуудын хооронд энергийг шилжүүлдэг. ATP нь ихэнх эсийн үйл ажиллагааны эрчим хүчний гол эх үүсвэр юм. Үүнд макромолекулууд, түүний дотор ДНХ, РНХ, уургийн нийлэгжилт орно. ATP нь мөн макромолекулуудыг экзоцитоз ба эндоцитоз гэх мэт эсийн мембранаар тээвэрлэхэд чухал үүрэг гүйцэтгэдэг.
Үүрэг В бүтэц эсүүд Тэгээд хөдөлгөөн
ATP нь эсийн бүтцийг хадгалахад оролцдог бөгөөд эсийн араг ясны элементүүдийг угсрах, задлахад тусалдаг. Энэ процессын улмаас актин утаснуудын агшилтанд ATP, булчингийн агшилтанд миозин шаардлагатай байдаг. Энэ сүүлчийн үйл явц нь амьтдын эрчим хүчний үндсэн шаардлагын нэг бөгөөд хөдөлгөөн, амьсгалахад зайлшгүй шаардлагатай.
Үүрэг В дохио системүүд
ондэсийн гаднахдохиосистемүүд
ATP нь мөн дохионы молекул юм. ATP, ADP эсвэл аденозиныг пуринергик рецептор гэж хүлээн зөвшөөрдөг. Пуринорецепторууд нь хөхтөн амьтдын эдэд хамгийн элбэг байдаг рецепторууд байж болно.
Хүний хувьд энэ дохионы үүрэг нь төв болон захын мэдрэлийн системд чухал үүрэг гүйцэтгэдэг. Үйл ажиллагаа нь мембран рецепторыг пуринергик идэвхжүүлснээр синапс, аксон, глиагаас ATP ялгарахаас хамаарна.
ондэсийн доторхдохиосистемүүд
ATP нь дохио дамжуулах процесст чухал үүрэг гүйцэтгэдэг. Үүнийг киназууд фосфат шилжүүлэх урвалд фосфатын бүлгийн эх үүсвэр болгон ашигладаг. Мембран уураг эсвэл липид зэрэг тулгуур дээрх киназууд нь дохионы нийтлэг хэлбэр юм. Уургийн киназын фосфоржилт нь митогенээр идэвхжсэн уургийн киназын каскад гэх мэт энэ каскадыг идэвхжүүлдэг.
ATP нь мөн аденилат циклазад ашиглагддаг бөгөөд AMP хэмээх хоёр дахь элч молекул болж хувирдаг бөгөөд энэ нь эсийн доторх агуулахаас кальцийг ялгаруулах кальцийн дохиог өдөөхөд оролцдог. [38] Энэ дохионы хэлбэр нь тархины үйл ажиллагаанд онцгой ач холбогдолтой боловч бусад олон эсийн үйл явцыг зохицуулахад оролцдог.
Дүгнэлт
1. Аденозин трифосфат - нуклеотид, организм дахь энерги, бодисын солилцоонд онцгой чухал үүрэг гүйцэтгэдэг; Юуны өмнө, нэгдэл нь амьд системд тохиолддог бүх биохимийн үйл явцын эрчим хүчний бүх нийтийн эх үүсвэр гэж нэрлэгддэг. Химийн хувьд ATP нь аденозины трифосфатын эфир бөгөөд аденин ба рибозын дериватив юм. ATP-ийн бүтэц нь РНХ-ийн нэг хэсэг болох аденины нуклеотидтэй төстэй бөгөөд зөвхөн нэг фосфорын хүчлийн оронд ATP нь гурван фосфорын хүчлийн үлдэгдэл агуулдаг. Эсүүд нь мэдэгдэхүйц хэмжээгээр хүчил агуулдаггүй, харин зөвхөн давсыг агуулдаг. Тиймээс фосфорын хүчил нь ATP-д үлдэгдэл хэлбэрээр ордог (хүчлийн OH бүлгийн оронд сөрөг цэнэгтэй хүчилтөрөгчийн атом байдаг).
2. Бие махбодид ADP-ийн фосфоржилтоор АТФ нийлэгдэнэ.
ADP + H 3 PO 4 + эрчим хүч> ATP + H 2 O.
ADP-ийн фосфоржилт нь субстратын фосфоржилт ба исэлдэлтийн фосфоржилт (исэлдүүлэгч бодисын энергийг ашиглах) гэсэн хоёр аргаар явагддаг.
Исэлдэлтийн фосфоржилт - эсийн амьсгалын хамгийн чухал бүрэлдэхүүн хэсгүүдийн нэг нь ATP хэлбэрээр энерги үйлдвэрлэхэд хүргэдэг. Исэлдэлтийн фосфоржилтын субстрат нь уураг, өөх тос, нүүрс усны органик нэгдлүүдийн задралын бүтээгдэхүүн юм. Исэлдэлтийн фосфоржих үйл явц нь митохондрийн кристалууд дээр явагддаг.
СубстратА нарийнфосфорилТэгээд сэлүүрт (биохимийн), гликолизийн исэлдэлтийн урвалын энерги болон трикарбоксилын хүчлийн цикл дэх a-ketoglutaric хүчил исэлдэх явцад эрчим хүчээр баялаг фосфорын нэгдлүүдийн нийлэгжилт.
3. Бие дэх ATP-ийн гол үүрэг нь олон тооны биохимийн урвалыг эрчим хүчээр хангахтай холбоотой юм. Хоёр өндөр энергийн холбоог зөөвөрлөгчийн хувьд ATP нь эрчим хүч зарцуулдаг олон биохими, физиологийн процессуудад шууд эрчим хүчний эх үүсвэр болдог. Амьд организмын биоэнергетикт дараахь зүйлс чухал ач холбогдолтой: химийн энерги нь органик субстратын исэлдэлтийн эксергон катаболик урвалтай хослуулан ATP үүсэх замаар хадгалагддаг; Химийн энергийг АТФ задрах, анаболизмын эндергоник урвал болон бусад эрчим хүч шаарддаг үйл явцын хамт ашигладаг.
4. Ачаалал ихсэх үед (жишээлбэл, ойрын зайн гүйлтийн үед) булчингууд нь зөвхөн ATP-ийн нийлүүлэлтийн улмаас ажилладаг. Булчингийн эсүүдэд энэ нөөц нь хэдэн арван агшилтанд хангалттай бөгөөд дараа нь ATP-ийн хэмжээг нөхөх шаардлагатай. ADP ба AMP-аас ATP-ийн нийлэгжилт нь нүүрс ус, липид болон бусад бодисыг задлах явцад ялгардаг энергийн улмаас үүсдэг. Сэтгэцийн ажил гүйцэтгэхэд мөн их хэмжээний ATP шаардагдана. Энэ шалтгааны улмаас сэтгэцийн ажил эрхэлдэг хүмүүс глюкозын хэмжээг ихэсгэдэг бөгөөд задаргаа нь ATP-ийн нийлэгжилтийг баталгаажуулдаг.
Эрчим хүчээс гадна ATP нь бие махбодид адил чухал ач холбогдолтой хэд хэдэн үүргийг гүйцэтгэдэг.
· Бусад нуклеозид трифосфатуудтай хамт ATP нь нуклейн хүчлүүдийн нийлэгжилтийн эхлэлийн бүтээгдэхүүн юм.
· Үүнээс гадна ATP нь биохимийн олон процессыг зохицуулахад чухал үүрэг гүйцэтгэдэг. Олон тооны ферментийн аллостерийн эффектор болох ATP нь тэдгээрийн зохицуулалтын төвүүдэд нэгдэж, үйл ажиллагааг нь сайжруулж эсвэл дарангуйлдаг.
· ATP нь мөн эсийн дотор дааврын дохио дамжуулах хоёрдогч элч болох цикл аденозин монофосфатын нийлэгжилтийн шууд урьдал бодис юм.
ATP нь синапс дахь дамжуулагчийн үүргийг бас мэддэг.
Ном зүй
1. Лемеза, Н.А. Их дээд сургуульд элсэгчдэд зориулсан биологийн гарын авлага / L.V. Камлюк Н.Д. Лисов. - Mn.: Unipress, 2011 - 624 х.
2. Lodish, H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J. Molecular Cell Biology, 5-р хэвлэл. - Нью Йорк: В.Х.Фриман, 2004 он.
3. Романовский, Ю.М. Амьд эсийн молекулын энерги хувиргагчид. Протон ATP синтаза - эргэдэг молекул мотор / Ю.М. Романовский A.N. Тихонов // UFN. - 2010. - Т.180. - P.931 - 956.
4. Воет Д, Воет Ж.Г. Биохими 1-р боть 3-р хэвлэл. - Вилли: Хобокен, НЖ. - N-Y: W. H. Freeman and Company, 2002. - 487 урэх.
5. ерөнхий хими. Биофизикийн хими. Биоген элементүүдийн хими. М.: төгссөн сургууль, 1993
6. Вершубский, А.В. Биофизик. / A.V. Вершубский, V.I. Приклонский, A.N. Тихонов. - М: 471-481.
7. Alberts B. Эсийн молекул биологи 3 боть. / Alberts B., Bray D., Lewis J. et al. M.: Mir, 1994.1558 х.
8. Николаев А.Я. Биологийн хими - М.: Эмнэлгийн мэдээллийн агентлаг ХХК, 1998 он.
9. Берг, J. M. Биохими, олон улсын хэвлэл. / Берг, Ж.М, Тимоцко, Ж.Л, Страйер, Л. - Нью-Йорк: В.Х. Фриман, 2011; p287.
10. Knorre D.G. Биологийн хими: Сурах бичиг. химийн хувьд биол. Мөн зөгийн бал. мэргэжилтэн. их дээд сургуулиуд - 3-р хэвлэл, илч. / Knorre D.G., Mysina S.D. - М .: Илүү өндөр. сургууль, 2000. - 479 х.: өвчтэй.
11. Элиот, В.Биохими ба молекул биологи / В.Элиот, Д.Элиот. - М .: ОХУ-ын Анагаахын Шинжлэх Ухааны Академийн биоанагаах ухааны химийн судалгааны хүрээлэнгийн хэвлэлийн газар, "Материк-альфа" ХХК, 1999, - 372 х.
12. Shina CL, K., 7 Areieh, W. Уусмал дахь ATP гидролизийн энергийн тухай. Physical Chemistry B сэтгүүл, 113 (47), (2009).
13. Berg, J. M. Biochemistry / J. M. Berg: J. L. Tymoczko, L. Stryer. - N-Y: W. H. Freeman and Company, 2002. - 1514 х.
...Үүнтэй төстэй баримт бичиг
Хүний биед агуулагдах органик нэгдлүүд. Уургийн бүтэц, үүрэг, ангилал. Нуклейн хүчлүүд (полинуклеотидууд), РНХ ба ДНХ-ийн бүтцийн онцлог, шинж чанарууд. Байгаль, хүний бие дэх нүүрс ус. Липидүүд нь өөх тос, өөх тостой төстэй бодисууд юм.
хураангуй, 2009-09-06 нэмэгдсэн
Уургийн нийлэгжилтийн үйл явц ба тэдгээрийн амьд организмын амьдралд гүйцэтгэх үүрэг. Чиг үүрэг ба Химийн шинж чанарамин хүчлүүд. Хүний биед тэдний дутагдлын шалтгаанууд. Чухал хүчил агуулсан хүнсний төрлүүд. Элгэнд нийлэгжсэн амин хүчлүүд.
танилцуулга, 2014 оны 10-р сарын 23-нд нэмэгдсэн
Нүүрс усны эрчим хүч, хадгалах, дэмжих үйл ажиллагаа. Хүний биеийн энергийн гол эх үүсвэр болох моносахаридын шинж чанар; глюкоз. Дисахаридын гол төлөөлөгчид; сахароз. Полисахарид, цардуул үүсэх, нүүрс усны солилцоо.
тайлан, 2010/04/30 нэмэгдсэн
Бие дэхь бодисын солилцооны үйл ажиллагаа: шим тэжээлийг задлах явцад үүссэн эрчим хүчээр эрхтэн, системийг хангах; молекулуудын хувирал хүнсний бүтээгдэхүүнбарилгын блок руу; нуклейн хүчил, липид, нүүрс ус болон бусад бүрэлдэхүүн хэсгүүд үүсэх.
хураангуй, 2009 оны 01-р сарын 20-нд нэмэгдсэн
Бүх амин чухал үйл явцын хэвийн үйл явцад уураг, өөх тос, нүүрс усны үүрэг, ач холбогдол. Уураг, өөх тос, нүүрс усны найрлага, бүтэц, үндсэн шинж чанарууд, тэдгээрийн хамгийн чухал ажлуудболон бие махбод дахь үйл ажиллагаа. Эдгээр шим тэжээлийн гол эх үүсвэрүүд.
танилцуулга, 2013 оны 4-р сарын 11-нд нэмэгдсэн
Холестерины молекулуудын бүтцийн шинж чанар нь чухал бүрэлдэхүүн хэсэг юм эсийн мембран. Хүний биед холестерины солилцооны зохицуулалтын механизмыг судлах. Цусны урсгал дахь илүүдэл бага нягтралтай липопротеины илрэлийн шинж чанаруудын шинжилгээ.
хураангуй, 2012/06/17 нэмэгдсэн
Уураг, липид, нүүрс усны солилцоо. Хүний хоол тэжээлийн төрлүүд: бүх идэштэн, тусдаа, нүүрс ус багатай хоол тэжээл, цагаан хоолтон, түүхий хүнсний хоолны дэглэм. Бодисын солилцоонд уургийн үүрэг. Бие дэх өөх тосны дутагдал. Хоолны төрөл өөрчлөгдсөний үр дүнд бие махбодид гарсан өөрчлөлтүүд.
курсын ажил, 2014-02-02 нэмэгдсэн
Исэлдэлтийн процесс, коллагены нийлэгжилд төмрийн оролцоог авч үзэх. Цус үүсэх үйл явцад гемоглобины ач холбогдлыг таниулах. Хүний биед төмрийн дутагдлаас болж толгой эргэх, амьсгал давчдах, бодисын солилцооны эмгэг.
танилцуулга, 2012-08-02 нэмэгдсэн
Фтор ба төмрийн шинж чанарууд. Биеийн өдөр тутмын хэрэгцээ. Фторын биед үзүүлэх үүрэг, нөлөө, үхлийн тун, бусад бодисуудтай харилцан үйлчлэл. Хүний биед агуулагдах төмөр, түүний эх үүсвэр. Бие махбодид төмрийн дутагдлын үр дагавар, түүний илүүдэл.
танилцуулга, 2017 оны 02-р сарын 14-нд нэмэгдсэн
Уургууд нь хүнсний эх үүсвэр, тэдгээрийн үндсэн үүрэг. Уураг үүсгэхэд оролцдог амин хүчлүүд. Полипептидийн гинжин хэлхээний бүтэц. Бие дэх уургийн өөрчлөлтүүд. Бүрэн ба бүрэн бус уураг. Уургийн бүтэц, химийн шинж чанар, чанарын урвал.
Хүний биед орж буй хоол хүнс нь нарийн төвөгтэй химийн өөрчлөлтөд ордог, өөрөөр хэлбэл. хэсэгчлэн исэлдэлт эсвэл агааргүй задралд ордог. Анаэробик задрал нь хөдөлгөөнд шаардлагатай химийн энергийг ялгаруулж, бие махбодид шаардлагатай бодисын нийлэгжилтийг үүсгэдэг.
Амьд организм дахь бодисын солилцоо нь хоорондоо холбоотой хоёр процессоос бүрдэнэ.
- анаболизм
- катаболизм
Анаболизм эсвэл ассимиляци- бие махбодид орж буй бодисууд дээр үндэслэн илүү энгийн, илүү төвөгтэй нэгдлүүдийн нийлэгжилт гадаад орчинбодисууд.
Жишээлбэл, ногоон ургамлын органик бодис нь нүүрстөрөгчийн давхар исэл, уснаас фотосинтезийн үр дүнд үүсдэг.
Катаболизм эсвэл диссимиляци– анаболизмын эсрэг үйл явц. Катаболизмын явцад нарийн төвөгтэй нэгдлүүд нь энгийн нэгдлүүд болж задардаг бөгөөд тэдгээр нь эцсийн бүтээгдэхүүн болон хүрээлэн буй орчинд ялгардаг.
Катаболизмд нүүрс усны гол эх үүсвэр нь гидролизийн ферментээр задардаг нүүрс ус юм. Хэрэв ургамалд үрийн соёололтын үед цардуул нь амилаза ферментийн нөлөөгөөр гидролиз болж, мальтоза дисахарид үүсгэдэг бол амьтдад шүлс, нойр булчирхайн амилазын нөлөөн дор мальтоз үүсдэг. Дараа нь мальтаза ферментийн нөлөөн дор глюкоз болж хувирдаг бөгөөд энэ нь исгэх, гликолиз, амьсгалын үр дүнд эцэст нь нүүрстөрөгчийн давхар исэл, ус руу задардаг. Эдгээр үйл явцын явцад ялгарсан энерги нь биед хуримтлагддаг. Нэг грамм нүүрс ус шатахад 4.1 ккал (17.22 кЖ) ялгардаг нь тогтоогдсон.
Өөх тос, уургийн катаболизм нь тодорхой ферментийн нөлөөн дор гидролизийн задралаас эхэлдэг бөгөөд эхний тохиолдолд чөлөөт тосны хүчил ба глицерин, хоёрдугаарт бага молекул жинтэй пептид ба амин хүчлүүд үүсдэг.
Метаболизм буюу бодисын солилцоог гурван үе шатанд хувааж болно.
- Эхнийх нь хоол боловсруулах эрхтэн дэх хоол хүнсний механик болон химийн боловсруулалт, шим тэжээлийг шингээхээс бүрддэг хоол боловсруулах үйл явц юм.
- Хоёр дахь шат нь бодисын задрал, нийлэгжилтийн үйл явцыг багтаасан завсрын бодисын солилцоо юм. Энэ үйл явц нь завсрын болон эцсийн бодисын солилцооны бүтээгдэхүүн үүсэх дагалддаг. Жишээлбэл, глюкоз нь CO2 ба H2O-ийн солилцооны эцсийн бүтээгдэхүүн болж хувирахаас өмнө хэд хэдэн завсрын өөрчлөлтөд ордог.
- Гурав дахь шат бол амьсгалсан агаар, шээс гэх мэт бодисын солилцооны бүтээгдэхүүнийг биеэс гаргах явдал юм. Бодисын солилцооны үйл явцад нөлөөлдөг бодисыг метаболит гэж нэрлэдэг. Эдгээрт амин хүчил, тосны хүчил, сахар, азотын суурь болон бусад нэгдлүүд орно.
Метаболизм буюу бодисын солилцоо нь энергийн хувиралтай салшгүй холбоотой. Амьд организм гадаад орчноос эрчим хүчийг байнга шаарддаг. Энэ нь фотосинтезийн үед, i.e. нарны гэрлийн энергийг хувиргах замаар сүүлийнх нь органик бодисуудад химийн боломжит энерги хэлбэрээр хадгалагддаг. Нүүрс ус, өөх тос болон бусад өндөр молекулын нэгдлүүдийн задралын үр дүнд үүссэн химийн боломжит энерги нь өндөр энергитэй нэгдлүүдэд хуримтлагддаг эсвэл хуримтлагддаг.
Солилцооны процесст энерги дараах байдлаар ялгардаг. Нэгдүгээрт, өндөр молекултай бодисууд нь гидролитийн аргаар бага молекултай бодисууд руу задардаг; жишээлбэл, полисахаридууд - моносахаридуудад; уураг - амин хүчил хүртэл; өөх тос - өөх тосны хүчил ба глицерин хүртэл. Үүний зэрэгцээ эдгээр бодисуудын гидролизийн задралын үед ялгарах энерги нь маш бага байдаг. Дараа нь гликолиз, өөх тосны хүчил, амин хүчлийг исэлдүүлэх явцад их хэмжээний энерги ялгардаг. Гидролизийн бүтээгдэхүүнээс гурав нь эрчим хүчний чухал ач холбогдолтой: ацетил коэнзим А, В-кетоглутарийн хүчил, оксало цууны хүчил. Эдгээр бодисууд нь ди-трикарбоксилын хүчлийн мөчлөгөөр (Кребсийн мөчлөг) исэлдэлтэнд ордог. Эрчим хүчний 2/3 нь Кребсын мөчлөгт ялгардаг.
ATP нь биед өндөр молекул жинтэй органик нэгдлүүдийн задралын үед ялгарах энергийг барьж, хадгалдаг. Үүний зэрэгцээ ATP нь эсэд нийлэгжиж, фосфорын холбоонд энерги хуримтлагддаг. Уургийн нийлэгжилт, түүнчлэн эрхтэн, булчингийн үйл ажиллагааны явцад ATP-ийн задрал нь энерги ялгарах үед өндөр энергитэй бонд үүсдэг. Үүссэн энерги нь нийлэгжилт, түүнчлэн моторын процессын эх үүсвэр болдог.
Дээрхээс харахад ATP нь хоёр эсрэг үйл явцын хоорондох холбоос бөгөөд бодисыг задлах явцад энерги хуримтлуулж, шингээх явцад ялгаруулдаг.
Бодисын солилцооны энерги дэх ATP-ийн биологийн үүргийг зүрхний цохилтын жишээг ашиглан дүрсэлж болно. Булчингийн агшилтын уурагтай харьцах үед ATP нь зүрхний агшилт, цусыг цусны эргэлтийн системд түлхэхэд шаардлагатай энергийг өгдөг. Үүний зэрэгцээ зүрхний хэвийн үйл ажиллагааг хангахын тулд ATP-ийн хэмжээг тогтмол нөхөх шаардлагатай байдаг. Хэрэв зүрх нь шаардлагатай хэмжээний тэжээллэг бодис, "түлш" (нүүрс ус ба тэдгээрийн задралын бүтээгдэхүүн), түүнчлэн ATP үүсэхэд шаардлагатай хүчилтөрөгчийг хүлээн авахгүй бол зүрхний үйл ажиллагаа тасалддаг.
Төрөл бүрийн эрхтнүүдийн үйл ажиллагаанд шаардлагатай ATP-ийг эсийн организмууд - исэлдэлтийн фосфоржилтын явцад митохондрид үйлдвэрлэдэг.