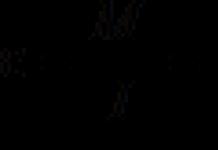Нүүрстөрөгчийн давхар исэл
Нүүрстөрөгчийн дутуу исэл (нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн ангидрид, нүүрстөрөгчийн давхар исэл
) — CO2, өнгөгүй хий, үнэргүй, бага зэрэг исгэлэн амттай.
Дэлхийн агаар мандалд нүүрсхүчлийн хийн агууламж дунджаар 0.038% байна.
Энэ нь амьдралыг дэмжихэд тохиромжгүй. Гэсэн хэдий ч энэ нь ургамал "тэжээж", түүнийг органик бодис болгон хувиргадаг. Нэмж дурдахад энэ нь дэлхийн нэгэн төрлийн "хөнжил" юм. Хэрэв энэ хий агаар мандлаас гэнэт алга болвол дэлхий илүү сэрүүн болж, бороо бараг алга болно.
"Дэлхийн хөнжил"
Нүүрстөрөгчийн давхар исэл
(нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн давхар исэл, CO 2
) нь нүүрстөрөгч ба хүчилтөрөгч гэсэн хоёр элементийг нэгтгэснээр үүсдэг. Энэ нь нүүрс эсвэл нүүрсустөрөгчийн нэгдлүүдийг шатаах, шингэнийг исгэх явцад, мөн хүн, амьтны амьсгалын бүтээгдэхүүн хэлбэрээр үүсдэг. Энэ нь мөн агаар мандалд бага хэмжээгээр агуулагддаг бөгөөд тэндээсээ ургамал шингээж, улмаар хүчилтөрөгч үүсгэдэг.
Нүүрстөрөгчийн давхар исэл нь өнгөгүй, агаараас хүнд байдаг. -78.5 хэмд хөлдөж, нүүрстөрөгчийн давхар ислээс тогтсон цас үүсгэдэг. Усан уусмалд энэ нь нүүрстөрөгчийн хүчил үүсгэдэг боловч амархан тусгаарлагдахад хангалттай тогтвортой биш юм.
Нүүрстөрөгчийн давхар исэл бол дэлхийн хөнжил юм. Энэ нь манай гарагийг халаадаг хэт ягаан туяаг хялбархан дамжуулж, түүний гадаргуугаас ялгарах хэт улаан туяаг сансар огторгуйд тусгадаг. Хэрэв нүүрстөрөгчийн давхар исэл агаар мандлаас гэнэт алга болвол энэ нь юуны түрүүнд уур амьсгалд нөлөөлнө. Дэлхий дээр илүү сэрүүн болж, бороо маш ховор орох болно. Эцсийн эцэст энэ нь хаашаа эргэхийг таахад хэцүү биш юм.
Ийм сүйрэл бидэнд хараахан заналхийлээгүй нь үнэн. Яг эсрэгээрээ. Шатаж байна органик бодис: газрын тос, нүүрс, Байгалийн хий, мод - агаар мандалд нүүрстөрөгчийн давхар ислийн агууламжийг аажмаар нэмэгдүүлдэг. Энэ нь цаг хугацааны явцад бид мэдэгдэхүйц дулаарч, чийгшүүлэхийг хүлээх ёстой гэсэн үг юм дэлхийн уур амьсгал. Дашрамд дурдахад, ахмадууд залуу насныхаасаа илт дулаахан болсон гэж үздэг...
Нүүрстөрөгчийн давхар исэл ялгардаг бага температурт шингэн, өндөр даралтын шингэн ба хийн. Энэ нь аммиак, спиртийн үйлдвэрлэлийн хаягдал хий, түүнчлэн тусгай түлшний шаталт болон бусад үйлдвэрүүдээс гаргаж авдаг. Нүүрстөрөгчийн давхар ислийн хий- 20°С-ийн температурт, 101.3 кПа (760 мм м.у.б) даралттай өнгөгүй, үнэргүй хий, нягт - 1.839 кг/м 3. Шингэн нүүрстөрөгчийн давхар исэл- зүгээр л өнгөгүй, үнэргүй шингэн.
Нүүрстөрөгчийн давхар исэлхоргүй, тэсэрч дэлбэрэх аюултай. 5% -иас дээш (92 г / м3) агууламжтай нүүрстөрөгчийн давхар исэл нь хүний эрүүл мэндэд хортой нөлөө үзүүлдэг - энэ нь агаараас хүнд бөгөөд шалны ойролцоо агааржуулалт муутай газарт хуримтлагддаг. Энэ нь агаар дахь хүчилтөрөгчийн эзлэхүүнийг багасгаж, хүчилтөрөгчийн дутагдал, амьсгал боогдох шалтгаан болдог.
Нүүрстөрөгчийн давхар исэл үйлдвэрлэх
Аж үйлдвэрт нүүрстөрөгчийн давхар ислийг зуухны хий, байгалийн карбонат (шохойн чулуу, доломит) задралын бүтээгдэхүүнээс гаргаж авдаг. Хийн хольцыг калийн карбонатын уусмалаар угааж, нүүрстөрөгчийн давхар ислийг шингээж, бикарбонат болгон хувиргадаг. Халах үед бикарбонатын уусмал задарч, нүүрстөрөгчийн давхар ислийг ялгаруулдаг. At аж үйлдвэрийн үйлдвэрлэлцилиндрт хий шахдаг.
Лабораторийн нөхцөлд биш их хэмжээгээркарбонат ба бикарбонатыг хүчилтэй, жишээлбэл, гантиг, давсны хүчилтэй урвалд оруулснаар олж авсан.
Өргөдөл
IN Хүнсний үйлдвэр
нүүрстөрөгчийн давхар ислийг хадгалах бодис болгон ашигладаг бөгөөд кодын дор савлагаа дээр заасан байдаг E290
Шингэн нүүрстөрөгчийн давхар исэл(шингэн хүнсний нүүрстөрөгчийн давхар исэл) - өндөр даралтын дор (~ 65-70 Атм) хадгалсан шингэрүүлсэн нүүрстөрөгчийн давхар исэл. Өнгөгүй шингэн. Шингэн нүүрстөрөгчийн давхар ислийг цилиндрээс агаар мандалд гаргахад нэг хэсэг нь ууршиж, нөгөө хэсэг нь хуурай мөсөн ширхэг үүсгэдэг.
Шингэн нүүрстөрөгчийн давхар исэл бүхий цилиндргал унтраагч болон хийжүүлсэн ус, нимбэгний ундаа үйлдвэрлэхэд өргөн хэрэглэгддэг.
Нүүрстөрөгчийн давхар исэлЭнэ нь утсаар гагнах үед хамгаалалтын орчин болгон ашигладаг боловч өндөр температурт хүчилтөрөгч ялгаруулж, ялгаруулдаг. Гарсан хүчилтөрөгч нь металыг исэлдүүлдэг. Үүнтэй холбогдуулан гагнуурын утсанд манган, цахиур зэрэг исэлдүүлэгч бодисыг нэвтрүүлэх шаардлагатай. Исэлдэлттэй холбоотой хүчилтөрөгчийн нөлөөллийн өөр нэг үр дагавар нь огцом бууралт юм гадаргуугийн хурцадмал байдал, энэ нь бусад зүйлсийн дотор аргон эсвэл гелийд гагнахаас илүү хүчтэй металл цацахад хүргэдэг.
Лаазанд агуулагдах нүүрстөрөгчийн давхар исэлАгаарын бууд болон нисэх онгоцны загварчлалын хөдөлгүүрийн тэжээлийн эх үүсвэр болгон ашигладаг.
Хатуу нүүрстөрөгчийн давхар исэл - хуурай мөс- мөсөн голд ашигладаг. Шингэн нүүрстөрөгчийн давхар ислийг дулааны цахилгаан станцуудад (хөргөгч, хөлдөөгч, нарны цахилгаан үүсгүүр гэх мэт) хөргөгч болон ажлын шингэн болгон ашигладаг.
"Хуурай мөс" болон нүүрстөрөгчийн давхар ислийн бусад ашигтай шинж чанарууд
Нүүрстөрөгчийн давхар ислийг өдөр тутмын практикт нэлээд өргөн ашигладаг. Жишээлбэл, анхилуун үнэрт эссэнс нэмсэн оргилуун ус бол гайхалтай сэргээгч ундаа юм. Хүнсний үйлдвэрт нүүрстөрөгчийн давхар ислийг мөн хадгалах бодис болгон ашигладаг - үүнийг кодын дор савлагаа дээр заасан болно. E290
, мөн зуурсан гурил исгэх бодис болгон.
Галын үед нүүрстөрөгчийн давхар ислийн гал унтраагчийг ашигладаг. Биохимичид ... агаарыг нүүрстөрөгчийн давхар ислээр бордох нь төрөл бүрийн үр тарианы ургацыг нэмэгдүүлэх маш үр дүнтэй хэрэгсэл болохыг олж тогтоосон. Магадгүй энэ бордоо нь ганц, гэхдээ мэдэгдэхүйц сул талтай: үүнийг зөвхөн хүлэмжинд ашиглаж болно. Нүүрстөрөгчийн давхар исэл үйлдвэрлэдэг үйлдвэрүүдэд шингэрүүлсэн хийг ган цилиндрт савлаж хэрэглэгчдэд хүргэдэг. Хэрэв та хавхлагыг нээвэл цас исгэрсээр гарч ирдэг. Ямар гайхамшиг вэ?
Бүх зүйлийг энгийнээр тайлбарлав. Хийг шахахад зарцуулсан ажил нь түүнийг өргөтгөхөд шаардагдахаас хамаагүй бага юм. Үүний үр дүнд үүссэн алдагдлыг ямар нэгэн байдлаар нөхөхийн тулд нүүрстөрөгчийн давхар ислийг огцом хөргөж, "хуурай мөс" болж хувирдаг. Энэ нь хадгалахад өргөн хэрэглэгддэг хүнсний бүтээгдэхүүнба өмнө нь ердийн мөсмэдэгдэхүйц давуу талтай: нэгдүгээрт, түүний "хөргөх хүчин чадал" нь жингийн нэгжээс хоёр дахин их; хоёрдугаарт, ул мөргүй ууршдаг.
Нүүрстөрөгчийн давхар ислийг утас гагнуурын идэвхтэй орчин болгон ашигладаг, учир нь нумын температурт нүүрстөрөгчийн давхар исэл задарч нүүрстөрөгчийн дутуу исэл CO ба хүчилтөрөгч нь эргээд шингэн металлтай харилцан үйлчилж, исэлдүүлдэг.
Лаазанд агуулагдах нүүрстөрөгчийн давхар ислийг агаарын буу, онгоцны загварчлалын хөдөлгүүрт эрчим хүчний эх үүсвэр болгон ашигладаг.
Нүүрстөрөгчийн давхар ислийн чанарын үзүүлэлтүүд ГОСТ 8050-85
|
Үзүүлэлтийн нэр |
Өнгөгүй, үнэргүй. Цусны эргэлт, амьсгалын хамгийн чухал зохицуулагч. Хоргүй. Үүнгүйгээр баян талх, амттай карбонатлаг ундаа байхгүй болно. Энэ өгүүллээс та нүүрстөрөгчийн давхар исэл гэж юу болох, хүний биед хэрхэн нөлөөлдөг талаар мэдэх болно. Бидний ихэнх нь сайн санахгүй байна сургуулийн курсфизикч, химич, гэхдээ тэд мэддэг: хий нь үл үзэгдэх, дүрмээр бол биет бус, тиймээс далд байдаг. Тиймээс нүүрстөрөгчийн давхар исэл нь биед хортой эсэх асуултад хариулахаасаа өмнө энэ нь юу болохыг санацгаая. Дэлхий хөнжил- нүүрстөрөгчийн давхар исэл. Энэ нь мөн нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн дутуу исэл (IV) эсвэл нүүрстөрөгчийн ангидрид юм. Хэвийн нөхцөлд энэ нь исгэлэн амттай өнгөгүй, үнэргүй хий юм. Агаар мандлын даралтын дор нүүрстөрөгчийн давхар исэл нь хоёр байдаг нэгтгэх байдал: хий (нүүрстөрөгчийн давхар исэл агаараас хүнд, усанд муу уусдаг) ба хатуу (-78 ºС-т хуурай мөс болж хувирдаг). Нүүрстөрөгчийн давхар исэл нь үндсэн бүрэлдэхүүн хэсгүүдийн нэг юм орчин. Агаар, гүний рашаан усанд агуулагдаж, хүн, амьтны амьсгалах явцад ялгарч, ургамлын фотосинтезд оролцдог. Нүүрстөрөгчийн давхар исэл нь уур амьсгалд идэвхтэй нөлөөлдөг. Энэ нь гаригийн дулаан солилцоог зохицуулдаг: хэт ягаан туяаг дамжуулж, хэт улаан туяаны цацрагийг хаадаг. Үүнтэй холбоотойгоор нүүрстөрөгчийн давхар ислийг заримдаа дэлхийн хөнжил гэж нэрлэдэг. O2 нь энерги юм. CO2 - очНүүрстөрөгчийн давхар исэл нь хүнийг амьдралынхаа туршид дагалддаг. Амьсгал, цусны эргэлтийн байгалийн зохицуулагч болох нүүрстөрөгчийн давхар исэл нь бодисын солилцооны салшгүй бүрэлдэхүүн хэсэг юм.
Амьсгалах замаар хүн уушгийг хүчилтөрөгчөөр дүүргэдэг. Үүний зэрэгцээ цулцангийн хэсэгт (уушигны тусгай "бөмбөлөг") хоёр талын солилцоо явагддаг: хүчилтөрөгч цус руу орж, нүүрстөрөгчийн давхар исэл ялгардаг. Эрэгтэй амьсгалаа гаргана. CO2 нь нэг юм эцсийн бүтээгдэхүүнбодисын солилцоо. Дүрслэлээр хэлбэл хүчилтөрөгч нь энерги, нүүрстөрөгчийн давхар исэл нь түүнийг асаадаг оч юм. Нэг цагт 30 литр хүчилтөрөгчөөр амьсгалсан хүн 20-25 литр нүүрстөрөгчийн давхар исэл ялгаруулдаг. Нүүрстөрөгчийн давхар исэл нь хүчилтөрөгчөөс дутахгүй биед чухал ач холбогдолтой юм. Энэ нь амьсгалын физиологийн өдөөгч юм: тархины бор гадаргад нөлөөлж, амьсгалын төвийг өдөөдөг. Дараагийн амьсгалын дохио нь хүчилтөрөгчийн дутагдал биш, харин нүүрстөрөгчийн давхар ислийн илүүдэл юм. Эцсийн эцэст, эс, эд эсийн бодисын солилцоо тасралтгүй явагддаг бөгөөд түүний эцсийн бүтээгдэхүүнийг байнга зайлуулж байх ёстой. Үүнээс гадна нүүрстөрөгчийн давхар исэл нь гормоны шүүрэл, ферментийн үйл ажиллагаа, биохимийн үйл явцын хурдад нөлөөлдөг. Хийн солилцооны тэнцвэрНүүрстөрөгчийн давхар исэл нь хоргүй, тэсрэлтгүй, хүмүүст туйлын хор хөнөөлгүй юм. Гэсэн хэдий ч нүүрстөрөгчийн давхар исэл ба хүчилтөрөгчийн тэнцвэр нь хэвийн амьдралд маш чухал юм. Бие дэх нүүрстөрөгчийн давхар ислийн дутагдал, илүүдэл нь гипокапни ба гиперкапни үүсгэдэг. Гипокапни- цусан дахь CO2 дутагдалтай. Энэ нь шаардлагатай хэмжээнээс илүү хүчилтөрөгч биед орох үед гүнзгий, хурдан амьсгалсны үр дүнд үүсдэг. Жишээлбэл, хэт эрчимтэй биеийн тамирын дасгал хийх үед. Үр дагавар нь янз бүр байж болно: бага зэргийн толгой эргэхээс эхлээд ухаан алдах хүртэл. Гиперкапни- цусан дахь CO2 илүүдэл. Хүн (хүчилтөрөгч, азот, усны уур, инертийн хийтэй хамт) 0.04% нүүрстөрөгчийн давхар исэл, 4.4% нь амьсгалдаг. Хэрэв та агааржуулалт муутай жижиг өрөөнд байгаа бол нүүрстөрөгчийн давхар ислийн концентраци нь нормоос давж болно. Үүний үр дүнд толгой өвдөх, дотор муухайрах, нойрмоглох шинж тэмдэг илэрч болно. Гэхдээ ихэнхдээ гиперкапни нь онцгой нөхцөл байдлыг дагалддаг: амьсгалын аппаратын эвдрэл, усан дор амьсгалаа барих гэх мэт. Тиймээс ихэнх хүмүүсийн бодлоос ялгаатай нь нүүрстөрөгчийн давхар исэл нь байгалиас заяасан хэмжээгээр хүний амь нас, эрүүл мэндэд зайлшгүй шаардлагатай байдаг. Нэмж дурдахад энэ нь үйлдвэрлэлийн өргөн хэрэглээг олж, хүмүүст олон практик ашиг тусыг авчирдаг. Тогооч нарын үйлчилгээнд гялалзсан бөмбөлөгүүдCO2 нь олон салбарт ашиглагддаг. Гэхдээ магадгүй нүүрстөрөгчийн давхар исэл нь хүнсний үйлдвэрлэл, хоол хийхэд хамгийн их эрэлт хэрэгцээтэй байдаг. Исгэлтийн нөлөөгөөр мөөгөнцрийн зуурмагт нүүрстөрөгчийн давхар исэл үүсдэг. Энэ нь түүний бөмбөлөгүүд нь зуурсан гурилыг сулруулж, агаартай болгож, эзэлхүүнийг нь нэмэгдүүлдэг.
Эдгээр ундаанууд нь дэлхийн өнцөг булан бүрт сая сая хэрэглэгчдийн дунд түгээмэл байдаг бөгөөд энэ нь гялалзсан бөмбөлөгүүд нь шилэнд маш хөгжилтэй хагарч, хамрыг нь маш тааламжтайгаар "хатгадаг"-тай холбоотой юм. Хийжүүлсэн ундаанд агуулагдах нүүрстөрөгчийн давхар исэл нь гиперкапни үүсэх эсвэл эрүүл биед ямар нэгэн хор хөнөөл учруулж болох уу? Мэдээж үгүй! Нэгдүгээрт, карбонатлаг ундаа бэлтгэхэд ашигладаг нүүрстөрөгчийн давхар ислийг хүнсний үйлдвэрт ашиглахаар тусгайлан бэлтгэсэн. Хийжүүлсэн ундаанд агуулагдах хэмжээ нь эрүүл хүмүүсийн биед огт хор хөнөөлгүй байдаг. Хоёрдугаарт, нүүрстөрөгчийн давхар ислийн ихэнх хэсэг нь савыг онгойлгосны дараа шууд ууршдаг. Үлдсэн бөмбөлгүүд нь уух явцад "ууршдаг" бөгөөд зөвхөн өвөрмөц исгэлэн мэдрэмжийг үлдээдэг. Үүний үр дүнд бага хэмжээний нүүрстөрөгчийн давхар исэл бие махбодид ордог. "Тэгвэл эмч нар яагаад заримдаа хийжүүлсэн ундаа уухыг хориглодог юм бэ?" - Та асуух. Анагаахын шинжлэх ухааны нэр дэвшигч, гастроэнтерологич Алена Александровна Тяжевагийн хэлснээр энэ нь олон тооны өвчин байдагтай холбоотой юм. ходоод гэдэсний зам, үүнд тусгай хатуу хоолны дэглэм тогтоодог. Эсрэг заалтуудын жагсаалтад зөвхөн хий агуулсан ундаа төдийгүй олон хүнсний бүтээгдэхүүн орно. Эрүүл хүн хоолны дэглэмдээ дунд зэргийн хийжүүлсэн ундааг хялбархан оруулж, хааяа нэг аяга кола ууж болно. ДүгнэлтНүүрстөрөгчийн давхар исэл нь гараг болон бие даасан организмын амьдралыг дэмжихэд зайлшгүй шаардлагатай. CO2 нь уур амьсгалд нөлөөлж, нэг төрлийн хөнжилийн үүрэг гүйцэтгэдэг. Үүнгүйгээр метаболизм боломжгүй: бодисын солилцооны бүтээгдэхүүн нь биеийг нүүрстөрөгчийн давхар ислээр орхидог. Энэ нь хүн бүрийн дуртай хийжүүлсэн ундааны зайлшгүй бүрэлдэхүүн хэсэг юм. Нүүрстөрөгчийн давхар исэл нь таны хамарыг гижигдэх хөгжилтэй бөмбөлөгүүдийг үүсгэдэг. Үүний зэрэгцээ энэ нь эрүүл хүний хувьд туйлын аюулгүй юм. ТОДОРХОЙЛОЛТ Нүүрстөрөгчийн давхар исэл (нүүрстөрөгчийн давхар исэл)хэвийн нөхцөлд энэ нь агаараас 1.5 дахин хүнд, өнгөгүй хий бөгөөд үүнээс болж нэг савнаас нөгөө сав руу шингэн шиг цутгаж болно. Хэвийн нөхцөлд 1 литр CO 2-ийн масс 1.98 г.Нүүрстөрөгчийн давхар ислийн усанд уусах чадвар бага: 20оС-т 1 эзэлхүүнтэй ус 0.88 эзэлхүүн CO 2, 0oС-т 1.7 эзэлхүүнийг уусгана. 0.6 МПа даралтын дор нүүрстөрөгчийн давхар исэл нь өрөөний температурт шингэн болж хувирдаг. Шингэн нүүрстөрөгчийн давхар ислийг ган цилиндрт хадгалдаг. Цилиндрээс хурдан асгахад ууршилтаас болж маш их дулаан шингэж, CO 2 нь цас шиг цул цагаан масс болж хувирдаг бөгөөд энэ нь хайлахгүйгээр -78.5 ° C-т сублимат болдог. Усан дахь CO 2-ийн уусмал нь исгэлэн амттай бөгөөд буцах урвалын үр дүнд үүссэн бага хэмжээний нүүрстөрөгчийн хүчил H 2 CO 3 уусмалд агуулагддаг тул бага зэрэг хүчиллэг урвалтай байдаг. CO 2 + H 2 O↔H 2 CO 3 . Нүүрстөрөгчийн давхар ислийн зарим шинж чанарыг дараах хүснэгтэд үзүүлэв. Нүүрстөрөгчийн давхар исэл үйлдвэрлэхНүүрстөрөгчийн давхар исэл нь карбонатууд дээр хүчлийн нөлөөгөөр бага хэмжээгээр үүсдэг. CaCO 3 + 2HCl = CaCl 2 + H 2 O + CO 2. Үйлдвэрлэлийн хэмжээнд CO 2 нь аммиакийн нийлэгжилтийн явцад голчлон дагалдах бүтээгдэхүүн болгон үйлдвэрлэгддэг. CH 4 + 2H 2 O = CO 2 + 4H 2; CO + H 2 O = CO 2 + H 2. Үүнээс гадна шохойн чулууг шатаах замаар их хэмжээний нүүрстөрөгчийн давхар исэл үүсдэг. CaCO 3 = CaO + CO 2. Нүүрстөрөгчийн давхар ислийн химийн шинж чанарНүүрстөрөгчийн давхар исэл нь хүчиллэг шинж чанартай байдаг: шүлт ба аммиакийн гидраттай урвалд ордог. Идэвхтэй металл, устөрөгч, нүүрстөрөгчөөр багасдаг. CO 2 + NaOH шингэрүүлсэн = NaHCO 3; CO 2 + 2NaOH conc = Na 2 CO 3 + H 2 O; CO 2 + Ba(OH) 2 = BaCO 3 + H 2 O; CO 2 + BaCO 3 + H 2 O = Ba(HCO 3) 2; CO 2 + NH 3 × H 2 O = NH 4 HCO 3; CO 2 + 4H 2 = CH 4 + 2H 2 O (t = 200 o C, cat. Cu 2 O); CO 2 + C = 2CO (t > 1000 o C); CO 2 + 2Mg = C + 2MgO; 2CO 2 + 5Ca = CaC 2 + 4CaO (t = 500 o C); 2CO 2 + 2Na 2 O 2 = 2Na 2 CO 3 + O 2. Нүүрстөрөгчийн давхар ислийн хэрэглээНүүрстөрөгчийн давхар ислийг аммиак хлоридын аргаар сод үйлдвэрлэх, мочевин нийлэгжүүлэх, нүүрстөрөгчийн хүчлийн давс үйлдвэрлэх, түүнчлэн жимс, рашаан, бусад ундааг карбонатжуулахад ашигладаг. "Хуурай мөс" хэмээх хатуу нүүрстөрөгчийн давхар ислийг хурдан мууддаг хүнсний бүтээгдэхүүнийг хөргөх, зайрмаг үйлдвэрлэх, хадгалах, бага температур шаардлагатай бусад олон тохиолдолд ашигладаг. Асуудлыг шийдвэрлэх жишээЖИШЭЭ 1 ЖИШЭЭ 2
Нүүрстөрөгчийн давхар исэл, нүүрстөрөгчийн дутуу исэл, нүүрстөрөгчийн давхар исэл - энэ бүхэн нь нүүрстөрөгчийн давхар исэл гэж бидний мэддэг нэг бодисын нэр юм. Тэгэхээр энэ хий ямар шинж чанартай, түүний хэрэглээний талбарууд юу вэ? Нүүрстөрөгчийн давхар исэл ба түүний физик шинж чанарНүүрстөрөгчийн давхар исэл нь нүүрстөрөгч ба хүчилтөрөгчөөс бүрдэнэ. Нүүрстөрөгчийн давхар ислийн томъёо нь иймэрхүү харагдаж байна - CO₂. Байгалийн хувьд энэ нь органик бодисыг шатаах эсвэл задлах явцад үүсдэг. Агаар, рашаан дахь хийн агууламж ч нэлээд өндөр байдаг. Үүнээс гадна хүн, амьтад амьсгалахдаа нүүрстөрөгчийн давхар исэл ялгаруулдаг.
Цагаан будаа. 1. Нүүрстөрөгчийн давхар ислийн молекул. Нүүрстөрөгчийн давхар исэл нь бүрэн өнгөгүй хий бөгөөд харагдахгүй. Энэ нь бас үнэргүй байдаг. Гэсэн хэдий ч өндөр концентрацитай үед хүн гиперкапни, өөрөөр хэлбэл амьсгал боогдох боломжтой. Нүүрстөрөгчийн давхар ислийн дутагдал нь эрүүл мэндийн асуудал үүсгэдэг. Энэ хий дутагдсаны улмаас амьсгал боогдохын эсрэг нөхцөл байдал үүсдэг - гипокапни. Хэрэв та нүүрстөрөгчийн давхар ислийг бага температурт байрлуулбал -72 хэмд талсжиж, цас шиг болно. Тиймээс хатуу төлөвт байгаа нүүрстөрөгчийн давхар ислийг "хуурай цас" гэж нэрлэдэг.
Цагаан будаа. 2. Хуурай цас – нүүрстөрөгчийн давхар исэл. Нүүрстөрөгчийн давхар исэл нь агаараас 1.5 дахин нягт байдаг. Түүний нягт нь 1.98 кг / м³ байна Химийн холбоонүүрстөрөгчийн давхар ислийн молекул дахь ковалент нь туйлтай байдаг. Хүчилтөрөгч нь илүү өндөр цахилгаан сөрөг утгатай байдаг тул туйлширсан байдаг. Бодисын судалгааны чухал ойлголт бол молекул ба молийн масс юм. Нүүрстөрөгчийн давхар ислийн молийн масс 44. Энэ тоо нь молекулыг бүрдүүлэгч атомуудын харьцангуй атомын массын нийлбэрээс үүсдэг. Харьцангуй атомын массын утгыг D.I-ийн хүснэгтээс авсан болно. Менделеев ба бүхэл тоо хүртэл дугуйрсан. Үүний дагуу CO₂-ийн молийн масс = 12+2*16. Нүүрстөрөгчийн давхар исэл дэх элементүүдийн массын хувийг тооцоолохын тулд та тооцооллын томъёог дагаж мөрдөх ёстой. массын фракцуудхүн бүр химийн элементматериалд. n- атом эсвэл молекулын тоо. Mr(CO₂) = 14 + 16 * 2 = 44 w(C) = 1 * 12 / 44 = 0.27 буюу 27% Нүүрстөрөгчийн давхар ислийн томъёонд хүчилтөрөгчийн хоёр атом орсон тул n = 2 w(O) = 2 * 16 болно. / 44 = 0.73 буюу 73% Хариулт: w(C) = 0.27 буюу 27%; w(O) = 0.73 буюу 73% Нүүрстөрөгчийн давхар ислийн химийн болон биологийн шинж чанарНүүрстөрөгчийн давхар исэл нь хүчиллэг исэл учраас хүчиллэг шинж чанартай бөгөөд усанд уусвал нүүрстөрөгчийн хүчил үүсгэдэг. CO₂+H₂O=H₂CO₃ Шүлттэй урвалд орж, карбонат ба бикарбонат үүсдэг. Энэ хий шатдаггүй. Зөвхөн зарим идэвхтэй металлууд, тухайлбал магни нь түүнд шатдаг. Халах үед нүүрстөрөгчийн давхар исэл нь нүүрстөрөгчийн дутуу исэл ба хүчилтөрөгч болж задардаг. 2CO₃=2CO+O₃. Бусад хүчиллэг ислийн нэгэн адил энэ хий нь бусад исэлтэй амархан урвалд ордог. СаO+Co₃=CaCO₃. Нүүрстөрөгчийн давхар исэл нь бүх органик бодисын нэг хэсэг юм. Байгальд энэ хийн эргэлтийг үйлдвэрлэгч, хэрэглэгчид, задлагчдын тусламжтайгаар гүйцэтгэдэг. Амьдралын явцад хүн өдөрт ойролцоогоор 1 кг нүүрстөрөгчийн давхар исэл ялгаруулдаг. Амьсгалах үед бид хүчилтөрөгч хүлээн авдаг боловч энэ мөчид нүүрстөрөгчийн давхар исэл цулцангийн хэсэгт үүсдэг. Энэ мөчид солилцоо үүсдэг: хүчилтөрөгч цус руу орж, нүүрстөрөгчийн давхар исэл гарч ирдэг. Архи үйлдвэрлэх явцад нүүрстөрөгчийн давхар исэл үүсдэг. Энэ хий нь мөн азот, хүчилтөрөгч, аргон үйлдвэрлэхэд дагалдах бүтээгдэхүүн юм. Нүүрстөрөгчийн давхар ислийг хэрэглэх нь хүнсний үйлдвэрт зайлшгүй шаардлагатай бөгөөд нүүрстөрөгчийн давхар исэл нь хадгалалтын үүрэг гүйцэтгэдэг бөгөөд шингэн хэлбэрээр нүүрстөрөгчийн давхар исэл нь гал унтраагуурт байдаг. Зорилго:
Ашигласан техникүүд:“үнэн ба худал мэдэгдэл”, “зигзаг-1”, кластерууд. Лабораторийн тоног төхөөрөмж:лабораторийн тавиур, хий авах төхөөрөмж, 50 мл-ийн аяга, гантиг чулуу, давсны хүчил (1:2), шохойн ус, Мохр хавчаар. I. Дуудлага хийх үе шат Сорилтын шатанд "үнэн ба худал мэдэгдэл" аргыг ашигладаг.
II. Жирэмсний үе шат 1. Оролцогчид “зигзаг”-ын таван үндсэн сэдвээр бичвэр хүлээн авдаг ажлын хэсгүүдийн үйл ажиллагааг зохион байгуулах:
Тексттэй анхны танилцах, анхны уншлага байдаг. 2. Шинжээчдийн бүлгүүдэд ажиллах. Шинжээчдийн бүлгүүд тодорхой асуудлаар "шинжээчдийг" нэгтгэдэг. Тэдний даалгавар бол текстийг анхааралтай унших, гол хэллэг, шинэ ойлголтыг тодруулах, эсвэл текстийн агуулгыг графикаар дүрслэхийн тулд кластер, янз бүрийн схемийг ашиглах явдал юм (ажил тус бүрээр хийгддэг). 3. Материалын сонголт, түүний бүтэц, нэмэлт (бүлгийн ажил) 4. Ажлын хэсгүүдэд текстийг дамжуулах бэлтгэл ажил
5. Илтгэлд бэлтгэх (зурагт хуудас) III. Тусгалын үе шат Ажлын хэсэг рүү буцах
Энэ нь иймэрхүү харагдаж магадгүй:
"Зигзаг" -ын таван үндсэн сэдвийн талаархи бичвэрүүд1. Нүүрстөрөгчийн давхар ислийг нээсэн түүх Нүүрстөрөгчийн давхар исэл нь 16-р зууны алхимич "зэрлэг хий" гэсэн нэрээр агаарыг эсэргүүцсэн бусад хийнүүдийн дотроос анхных юм. Вант Хелмонт. CO 2-ийн нээлт нь химийн шинэ салбар болох пневматохими (хийн хими) эхлэлийг тавьсан юм. Шотландын химич Жозеф Блэк (1728 - 1799) 1754 онд шохойтой эрдэс гантиг (кальцийн карбонат) халах үед задарч, хий ялгаруулж, шатаасан шохой (кальцийн исэл) үүсгэдэг болохыг тогтоожээ. CaCO 3 CaO + CO 2 Гарсан хийг кальцийн оксидтэй дахин нэгтгэж кальцийн карбонатыг дахин үүсгэж болно. CaO + CO 2 CaCO 3 Энэ хий нь Ван Хелмонтын нээсэн "зэрлэг хий"-тэй яг адилхан байсан боловч Блэк түүнд "холбогдсон агаар" гэсэн шинэ нэр өгсөн - энэ хий нь холбогдож, дахин хатуу бодис болж хувирдаг, мөн татагдах чадвартай байсан. шохойн ус (кальцийн гидроксид) руу орж, үүлэрхэг болгох:
Хэдэн жилийн дараа Кавендиш өөр хоёр шинж чанарыг олж мэдэв физик шинж чанарнүүрстөрөгчийн давхар исэл - түүний өндөр нягтрал, усанд уусах чадвар. 2. Байгаль дахь нүүрстөрөгчийн давхар исэл Агаар мандалд нүүрстөрөгчийн давхар ислийн агууламж харьцангуй бага, ердөө 0.04-0.03% (эзэлхүүнээр). Агаар мандалд хуримтлагдсан CO 2 нь 2200 тэрбум тонн жинтэй. 3. Нүүрстөрөгчийн давхар ислийг бий болгох Аж үйлдвэрт нүүрстөрөгчийн давхар ислийг голчлон шохойн чулуу шатаах, согтууруулах ундааны исгэх гэх мэт дайвар бүтээгдэхүүн хэлбэрээр авдаг. CaCO 3 + 2HCl CaCl 2 + CO 2 + H 2 O Давсны хүчлийн оронд хүхрийн хүчил хэрэглэх боломжгүй, учир нь усанд уусдаг кальцийн хлоридын оронд гипс - кальцийн сульфат (CaSO 4) - усанд бага зэрэг уусдаг давс авах болно. Гантиг чулуун дээр тогтох үед гипс нь хүчилд хүрэхэд маш хэцүү болгодог бөгөөд ингэснээр урвалыг удаашруулдаг.
4. Нүүрстөрөгчийн давхар ислийн шинж чанар CO 2 нь өнгөгүй, үнэргүй, агаараас 1.5 дахин хүнд, холиход хэцүү хий (Д.И.Менделеевийн хэлснээр агаарт “живдэг”) бөгөөд үүнийг дараах туршилтаар нотлох боломжтой: шилний дээгүүр, дотор шатаж буй лаа бэхэлсэн бол нүүрстөрөгчийн давхар ислээр дүүргэсэн шилийг хөмрүүл. Лаа тэр даруй унтарна. CO 2 + Ca(OH) 2 CaCO 3 + H 2 O Илүүдэл CO2 нэмэхэд уусдаггүй карбонатыг уусдаг кальцийн бикарбонат болгон хувиргаснаар үүлэрхэг уусмал дахин тунгалаг болно. CaCO 3 + H 2 O + CO 2 Ca(HCO 3) 2 5. Нүүрстөрөгчийн давхар ислийн практик хэрэглээ Дарагдсан хатуу нүүрстөрөгчийн давхар ислийг "хуурай мөс" гэж нэрлэдэг. Уран зохиол
|
|---|


 Нүүрстөрөгчийн давхар ислийн тусламжтайгаар янз бүрийн шинэ сэргэг ундаа хийдэг: квас, рашаан болон бусад хийжүүлсэн ундаанууд хүүхэд, насанд хүрэгчдэд хайртай.
Нүүрстөрөгчийн давхар ислийн тусламжтайгаар янз бүрийн шинэ сэргэг ундаа хийдэг: квас, рашаан болон бусад хийжүүлсэн ундаанууд хүүхэд, насанд хүрэгчдэд хайртай.