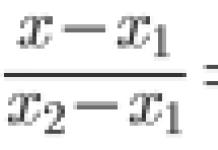Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов. Для аминов характерны ярко выраженные основные свойства. Водные растворы алифатических аминов проявляют щелочную реакцию. Алифатические амины – более сильные основания, чем аммиак. Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку не-поделенная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.
На основность аминов влияют различные факторы: электронные эффекты углеводородных радикалов, пространственное экранирование радикалами атома азота, а также способность образующихся ионов к стабилизации за счет сольватации в среде растворителя. В результате донорного эффекта алкильных групп основность алифатических аминов в газовой фазе (без растворителя) растет в ряду: первичные < вторичные < третичные. Основность ароматических аминов зависит также от характера заместителей в бензольном кольце. Электроноакцепторные заместители (-F, -Cl, -NO2 и т. п.) уменьшают основные свойства ариламина по сравнению с анилином, а электронодонорные (алкил R-, -OCH3, -N(CH3)2 и др.), напротив, увеличивают.
1. CH3-NH 2 + Н2O → OH (взаимодействие с водой)
2. (CH 3)2NH + HCl → [(CH3)2NH2]Cl хлорид диметиламмония (взаимодействие с кислотами)
[(CH 3)2NH 2]Cl + NaOH → (CH 3)2NH + NaCl + H2O (взаимодействие солей аминов со щелочами)

(ацителирование, с третичными аминами не идет)
4. R-NH2 + CH3I → I¯ →NH3 → CH3NHR + NH4I (алкилирование)
5. Взаимодействие с азотистой кислотой: строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различия первичных, вторичных и третичных аминов.
а) R-NH2 + HNO2 → R-OH + N2 + H2O (первичные жирные амины)
б) С6Н5-NH2 + NaNO2 + HCl → [С6Н5-N≡N]+Cl¯ – соль диазония (первичные ароматические амины)
в) R2NH + Н-О-N=O → R2N-N=O (N-нитрозамин) + Н2O (вторичные жирные и ароматические амины)
г) R3N + Н-О-N=O → при низкой температуре нет реакции (третичные жирные амины)

(третичные ароматические амины)
Свойства анилина. Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и аммиаком, но под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения по сравнению с бензолом.
C6H5-NH2 + HCl → Cl = C6H5NH2 HCl
C6H5NH2 HCl + NaOH → C6H5NH2 + NaCl + H2O
C6H5NH2 + CH3I →t → +I¯

Аминокислоты
Аминокислотами называются гетеро-функциональные соединения, молекулы которых содержат одновременно аминогруппу и карбоксильную группу. В зависимости от взаимного расположения амино– и карбоксильной групп аминокислоты подразделяют на α-, β-, γ– и т. д. По ИЮПАК, для наименования аминокислот группу NH2- называют приставкой амино-, указывая цифрой номер углеродного атома, с которым она связана, а затем следует название соответствующей кислоты.

2-аминопропановая кислота (α-аминопропановая, α-аланин)
Наиболее общие свойства всех органических соединений - способность их гореть. Сам аммиак горит и, в общем, легко, но поджечь его не всегда просто. В отличие от него амины загораются легко и горят чаще всего бесцветным или малоокрашенным пламенем. При этом азот аминов традиционно окисляется до молекулярного азота, поскольку оксиды азота малоустойчивы.
Амины загораются на воздухе легче, чем аммиак.
4NH 3 + 3O 2 = 2N 2 + 6H 2 O;
4С 2 H 5 NH 2 + 15O 2 = 8CO 2 + 14H 2 O + 2N 2 .
Основные свойства
Первичные, вторичные и третичные амины обязательно содержат неподеленную электронную пару, как и полагается трехвалентному азоту. То есть амины в растворе проявляют основные свойства, или их растворы являются основаниями. Именно поэтому амины в водном растворе окрашивают лакмус в синий цвет, а фенолфталеин в малиновый. Рис. 1, 2.
Рис. 1.
Рис. 2.

Благодаря этой электронной паре может образовываться донорно-акцепторная связь с ионом водорода:
С 2 Н 5 NH 2 + H + = C 2 H 5 NH 3 + .
Таким образом, подобно аммиаку, амины проявляют свойства оснований:
NH 3 + H 2 O NH 4 OH;
С 2 Н 5 NH 2 + H 2 O C 2 H 5 NH 3 OH.
С кислотами аммиак образует соли аммония, а амины - алкиламмония :
NH 3 + HBr = NH 4 Br (бромид аммония)
С 2 Н 5 NH 2 + HBr = C 2 H 5 NH 3 Br (бромид этиламмония)
Точно так же, как с кислотами аммиак образует соли аммония, амины образуют соответствующие соли. Эти соли могут быть образованы, как и в случае аммиака, не только при реакции водных растворов, но и в газовой фазе, если амины достаточно летучи.
То есть, если поставить рядом сосуды с концентрированной соляной кислотой или даже с органической летучей, например уксусной, и сосуд с летучим амином, то скоро между ними в пространстве появится нечто напоминающее дым без огня, т. е. будут образовываться кристаллики, соответствующие соли алкиламина. Рис. 3.

Рис. 3.
Щелочи вытесняют амины , являющиеся, как и аммиак, слабыми основаниями, из солей алкиламмония:
NH 4 Cl + KOH = NH 3 - + KCl + H 2 O;
CH 3 NH 3 Cl + KOH = CH 3 NH 2 - + KCl + H 2 O.
Основные свойства аминов выше, чем у аммиака. Почему? Образование донорно-акцепторной связи с ионом водорода происходит тем легче, чем выше электронная плотность на атоме азота. Углеводородные радикалы содержат много электронов и охотно «делятся» ими с атомом азота (рис. 4).

Рис. 4. Донорно-акцепторная связь с ионом водорода
Однако основные свойства третичных аминов меньше, чем вторичных (сравните константы основности). Почему? В третичном амине атом азота со всех сторон окружен углеводородными радикалами, и его способность вступать в реакции затруднена.
Амины, подобно аммиаку, способны реагировать с галогеналканами, замещая атом галогена:
СН 3 Br + NH 3 = CH 3 NH 2 + HBr;
СH 3 NH 2 + CH 3 Br = (CH 3) 2 NH + HBr;
(CH 3) 2 NH + CH 3 Br = (CH 3) 3 N + HBr.
Замещать галоген могут и третичные амины, так что реакция может пойти и дальше. Образуется четвертичная аммониевая соль - бромид тетраметиламмония (CH 3) 4 NBr:
(CH 3) 3 N + CH 3 Br = (CH 3) 4 N+ + Br-.
Подведение итога урока
На данном уроке была рассмотрена тема «Аминосоединения. Классификация, изомерия, названия и физические свойства». Вы повторили генезис кислородсодержащих органических соединений и вспомнили о некоторых общих свойствах аммиака и воды. Затем рассмотрели, как получить аминосоединения. Изучили их классификацию, изомерию, названия и присущие им физические свойства.
Список литературы
- Рудзитис Г.Е., Фельдман Ф.Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
- Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин, А.А. Дроздов, В.И. Теренин. - М.: Дрофа, 2008. - 463 с.
- Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин, А.А. Дроздов, В.И. Теренин. - М.: Дрофа, 2010. - 462 с.
- Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
- сайт ().
- Chemistry.ssu.samara.ru ().
- Химик.ру ().
- Promobud.ua ().
Домашнее задание
- №№ 3, 4 (с. 14) Рудзитис Г.Е., Фельдман Ф.Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
- Сравните свойства аминов предельного ряда и спиртов.
- Напишите уравнения реакций, подтверждающих основность аминов.
Амины
Классификация и номенклатура
Аминами являются органические производные аммиака, в молекуле которого один, два или три атома водорода заменены радикалами. По этому признаку различают первичные (RNH 2), вторичные (R 2 NH) и третичные (R 3 N) амины.
В зависимости от характера радикала амины могут быть предельными или ароматическими, а также предельно-ароматическими (метиламин, анилин и метиланилин, соответственно). С атомом азота может быть связан и разветвленный радикал (например, трет бутиламин), и поликонденсированный, что демонстрируется примером адамантиламина (аминоадамантана), обладающего биологическим действием и применяемого в медицине


По принципам рациональной номенклатуры название этого класса веществ складывается из названия радикалов при атоме азота, именуемого амином. В названии первичных аминов по международной номенклатуре аминному атому азота присваивается название ами- но, употребляемое с указанием его местоположения перед названием углеводородной цепи. Впрочем, многие амины сохранили.свои тривиальные названия, например, анилин".
Кроме аминогруппы в молекулах органических веществ могут находиться и иные заместители, как это, к примеру, имеет место в случае сульфаниловой кислоты. Аминный атом азота может быть включен и в насыщенный цикл. К числу насыщенных гетероциклических аминов относится построенный с напряжением трехчленный этиленимин, обладающий сильным мутагенным действием. Этилениминовый цикл входит в состав молекул некоторых лекарств. Без напряжения построены тетрагидропиррольный и пиперидиновый циклы, присутствующие в молекулах ряда алкалоидов (в том числе никотина и анабазина, см. разд. 20.4). С их участием, как и с помощью морфолинового кольца, построены молекулы многих лекарственных средств.




Гетероциклическими ароматическими аминами являются, к примеру, пиррол и пиридин. Наконец, аминогруппа может быть связана и с гетероциклом, что иллюстрируется примером аденина (6-аминопурина) - незаменимого фрагмента нуклеиновых кислот.


К числу производных аммиака относятся и органические вещества, которые можно построить из солей аммония или его гидроксида замещением всех четырех атомов водорода различными углеводородными радикалами, как это видно на примере тетраметиламмоний гидроксида:

Другим примером тетразамещенных аммонийных производных - четвертичных аммониевых оснований или их солей - служит нейрин, токсичное вещество, образующееся в процессе гниения тканей животного происхождения.
Четвертичный атом азота может входить в состав гетероциклов, например, соответствующей соли из ряда пиридина - N-алкилпиридиниевой соли. К таким четвертичным солям относятся некоторые алкалоиды. Кроме того, четвертичный атом азота входит в состав многих лекарственных веществ и некоторых биомолекул.
Выше приведенные примеры демонстрируют многообразие аминосоединений и их большое медико-биологическое значение. К этому необходимо добавить, что аминогруппа входит в состав таких классов биомолекул, как аминокислоты и белки, нуклеиновые кислоты, присутствует в ряде природных производных углеводов, именуемых аминосахарами. Аминогруппа является важнейшей функциональной группой алкалоидов и многочисленных лекарственных препаратов самого различного назначения. Отдельные примеры таких веществ будут приведены ниже.
24.3.2. Амины как органические основания

 Наличие
свободной электронной пары азота
сообщает аминам свойства оснований.
Поэтому
характерной особенностью аминов
является реакция с кислотами с
образованием соответствующих
аммониевых солей, что видно из реакции
для первичного предельного амина:
Наличие
свободной электронной пары азота
сообщает аминам свойства оснований.
Поэтому
характерной особенностью аминов
является реакция с кислотами с
образованием соответствующих
аммониевых солей, что видно из реакции
для первичного предельного амина:
Аналогично из анилина образуется анилиниевая соль, из пиридина - пиридиниевая и т.д. Подобно аммиаку, амины в водных растворах создают щелочную среду, согласно уравнению:
Количественно основность азотсодержащих оснований в водной среде отражается величиной константы равновесия (К ь ) (чаще используют величинурК ь ) илир/С а (ВН +), характеризующей кислотность сопряженной кислоты данного основания.

Наиболее сильными основаниями будут соединения, содержащие атом азота, у которого неподеленная пара азота находится на неподеленной 5р 3 -гибридной орбитали (алифатические амины, аммиак, аминокислоты), а наиболее слабыми - те, у которых эта пара участвует в р,п-сопряжении (амиды, пиррол, пиридин).
Электронодонорные заместители, к которым относятся алкильные группы, должны увеличивать основность аминов, поскольку увеличивают электронную плотность у атома азота. Так, метиламин (рК ь = 3,27) является более сильным основанием, чем аммиак (рК ь = 4,75), а диметиламин (рК ь = 3,02) - более сильное основание, чем метиламин. Однако при переходе к триметиламину, вопреки ожиданию, основность несколько падает (рК ь = 4,10). Причина этого состоит в том, что с увеличением числа заместителей у атома азота подход протона все более затрудняется. Таким образом, здесь речь идет не об электронном, а пространственном влиянии заместителей. Это воздействие заместителей называют стерическим фактором.
Ароматические амины - более слабые основания, чем предельные, из-за электроноак-цепторного эффекта ароматического кольца. Поэтому невысока основность и пиридина. Накопление фенильных заместителей заметно подавляет активность электронной пары атома азота. Так, рК, дифениламина составляет 13,12, а трифениламин совсем не проявляет свойств основания.
Чрезвычайно низкая основность пиррола вызвана тем, что в его молекуле электронная пара атома азота вовлечена в образование бл-электронной ароматической связи. На ее связывание с протоном требуется значительная дополнительная затрата энергии. В результате образования пирролиевых солей ароматическая связь, а, следовательно, и стабильность молекулы исчезают. Этим объясняется то, что пиррол в кислой среде быстро осмоляется.
Интересно отметить, что сильный электроноакцепторный эффект, оказываемый пир-рольным циклом на атом азота, приводит к ослаблению связи N-H, в силу чего пиррол способен проявлять свойства слабой кислоты (рК а = 17,5).
![]()
Под действием такого активного металла, как калий, может быть приготовлена его калиевая соль - пиррол-калий.
Кислотные свойства связи N-H пиррольного цикла объясняют, в частности, способность порфина и его природных производных к образованию солей с катионами металлов. Два пиррольных кольца молекулы порфирина координируются с катионом за счет электронных пар своих атомов азота, а два других - заменяя атомы водорода, как и молекула самого пиррола при образовании пиррол-калия. Именно такими солями и являются хлорофилл и гемоглобин

ТЕМА ЛЕКЦИИ: АМИНЫ И АМИНОСПИРТЫ
Вопросы:
Общая характеристика: строение, классификация, номенклатура.
Методы получения
Физические свойства
Химические свойства
Отдельные представители. Способы идентификации.
Общая характеристика: строение, классификация, номенклатура
Аминами называются производные аммиака, молекуле которого атомы водорода замещены на углеводородные радикалы.
Классификация
1– В зависимости от числа замещенных атомов водорода аммиака различают амины :
– первичные содержат аминогруппу аминогруппу (–NH 2), общая формула: R–NH 2 ,
– вторичные содержат иминогруппу (–NH),
общая формула: R 1 –NH–R 2
– третичные содержат атом азота, общая формула: R 3 –N
Известны также соединения с четвертичным атомом азота: четвертичный гидроксид аммония и его соли.
2– В зависимости от строения радикала амины различают:
– алифатические (предельные и непредельные)
– алициклические
– ароматические (содержащие в ядре аминогруппу или боковой цепи)
– гетероциклические.
Номенклатура, изомерия аминов
1. Названия аминов по рациональной номенклатуре обычно производят от названий входящих в них углеводородных радикалов с присоединением окончания –амин : метиламин СН 3 –NН 2 , диметиламин СН 3 –NН–СН 3 , триметиламин (СН 3) 3 N, пропиламин СН 3 СН 2 СН 2 –NН 2 , фениламин С 6 Н 5 – NН 2 и т. д.
2. По номенклатуре ИЮПАК аминогруппу рассматривают как функциональную группу и ее название амино- ставят перед названием основной цепи:
Изомерия аминов зависит от изомерии радикалов.
Способы получения аминов
Амины могут быть получены различными способами.
А) Действием на аммиак галогеналкилами
2NH 3 + CH 3 I ––® CH 3 – NH 2 + NH 4 I
Б) Каталитическое гидрирование нитробензола молекулярным водородом:
С 6 Н 5 NО 2 ––® С 6 Н 5 NН 2 + Н 2 О
нитробензол кат анилин
В) Получение низших аминов (С 1 –С 4) путем алкилирования спиртами:
350 0 C, Al 2 O 3
R–OH + NH 3 –––––––––––® R–NH 2 +H 2 O
350 0 C, Al 2 O 3
2R–OH + NH 3 –––––––––––® R 2 –NH +2H 2 O
350 0 C, Al 2 O 3
3R–OH + NH 3 –––––––––––® R 3 –N + 3H 2 O
Физические свойства аминов
Метиламин, диметиламин и триметиламин - газы, средние члены ряда аминов - жидкости, высшие - твердые тела. С увеличением молекулярной массы аминов увеличивается их плотность, повышается температура кипения и уменьшается растворимость в воде. Высшие амины в воде нерастворимы. Низшие амины имеют неприятный запах, несколько напоминающий запах испорченной рыбы. Высшие амины или не имеют запаха, или обладают очень слабым запахом. Ароматические амины представляют собой бесцветные жидкости или твердые вещества, обладающие неприятным запахом и ядовиты.
Химические свойства аминов
Химическое поведение аминов определяется наличием в молекуле аминогруппы. На внешней электронной оболочке атома азота имеется 5 электронов. В молекуле амина также, как и в молекуле аммиака, атом азота затрачивает на образование трех ковалентных связей три электрона, а два остаются свободными.
Наличие свободной электронной пары у атома азота дает ему возможность присоединять протон, поэтому амины подобны аммиаку, проявляют основные свойства, образуют гидроксиды, соли.
Солеобразование. Амины с кислотами дают соли, которые под действием сильного основания вновь дают свободные амины:
Амины дают соли даже со слабой угольной кислотой:
Как и аммиак, амины обладают основными свойствами что объясняется связыванием протонов в слабо диссоциирующий катион замещенного аммония:
| |
При растворении амина в воде часть протонов воды расходуется на образование катиона; таким образом, в растворе появляется избыток гидроксид-ионов, и он имеет щелочные свойства, достаточные для окрашивания растворов лакмуса в синий цвет и фенолфталеина в малиновый. Основность аминов предельного ряда колеблется в очень небольших пределах и близка к основности аммиака.
Эффект метильных групп несколько повышает основность метил- и диметиламина. В случае триметиламина метильные группы уже затрудняют сольватацию образующегося катиона и уменьшают его стабилизацию, а следовательно, и основность.
Соли аминов следует рассматривать как комплексные соединения. Центральным атомом в них является атом азота, координационное число которого равно четырем. Атомы водорода или алкилы связаны с атомом азота и расположены во внутренней сфере; кислотный остаток расположен во внешней сфере.
Ацилирование аминов. При действии на первичные и вторичные амины некоторых производных органических кислот (галогенангидридов, ангидридов и др.) образуются амиды:
Вторичные амины с азотистой кислотой дают нитрозоамины - желтоватые жидкости, мало растворимые в воде:
Третичные амины устойчивы к действию разбавленной азотистой кислоты на холоду (образуют соли азотистой кислоты), в более жестких условиях один из радикалов отщепляется и образуется нитрозоамин.
Диамины
Диамины играют важную роль в биологических процессах. Как правило, они легко растворимы в воде, обладают характерным запахом, имеют сильно щелочную реакцию, взаимодействуют с С0 2 воздуха. Диамины образуют устойчивые соли с двумя эквивалентами кислоты.
Этилендиамин (1,2-этандиамин) H 2 NCH 2 СН 2 NН 2 . Он является простейшим диамином; может быть получен действием аммиака на этиленбромид:
Тетраметилендиамин (1,4-бутандиамин), или путресцин, NН 2 СН 2 СН 2 СН 2 СН 2 NH 2 и пентаметилендиамин (1,5-пентандиамин) NН 2 СН 2 СН 2 СН 2 СН 2 СН 2 NН 2 , или кадаверин. Они были открыты в продуктах разложения белковых веществ; образуются при декарбоксилировании диаминокислот и названы птомаинами (от греч.- труп), их считали ранее «трупными ядами». В настоящее время выяснено, что ядовитость гниющих белков вызвана не птомаинами, а присутствием других веществ.
Путресцин и кадаверин образуются в результате жизнедеятельности многих микроорганизмов (например, возбудителей столбняка и холеры) и грибков; они встречаются в сыре, спорынье, мухоморе, пивных дрожжах.
Некоторые диамины применяются в качестве сырья для получения полиамидных волокон и пластмасс. Так, из гекса-метилендиамина NН 2 СН 2 СН 2 СН 2 СН 2 СН 2 СН 2 NН 2 получено весьма ценное синтетическое волокно - найлон (США) или анид (Россия).
Аминоспирты
Аминоспирты - соединения со смешанными функциями, в молекуле которых содержатся амино- и оксигруппы.
Аминоэтанол (этаноламин) НО-СН 2 СН 2 -NH 2 , или коламин.
Этаноламин - густая маслянистая жидкость, смешивается с водой во всех отношениях, обладает сильными щелочными свойствами. Hаряду с моноэтаноламином получаются также диэтаноламин и триэтаноламин:
Холин входит в состав лецитинов - жироподобных веществ, весьма распространенных в животных и растительных организмах, и может быть выделен из них. Холин представляет собой кристаллическую, весьма гигроскопичную, легко расплывающуюся на воздухе массу. Он обладает сильными щелочными свойствами и с кислотами легко образует соли.
При ацилировании холина уксусным ангидридом образуется холинацетат, называемый также ацетилхолином:
 |
Ацетилхолин играет крайне важную биохимическую роль, так как является медиатором (посредником), передающим возбуждение от нервных рецепторов к мышцам.
Классификация аминов разнообразна и определяется тем, какой признак строения взят за основу.
В зависимости от числа органических групп, связанных с атомом азота, различают:
первичные амины одна органическая группа у азота RNH 2
вторичные амины две органических группы у азота R 2 NH, органические группы могут быть различными R"R"NH
третичные амины три органических группы у азота R 3 N или R"R"R""N
По типу органической группы, связанной с азотом, различают алифатические СH 3 N6H 5 N
По числу аминогрупп в молекуле амины делят на моноамины СH 3 NН 2 , диамины H 2 N(СH 2) 2 NН 2 , триамины и т.д.
Номенклатура аминов.
к названию органических групп, связанных с азотом, добавляют слово «амин», при этом группы упоминают в алфавитном порядке, например, СН 3 NHС 3 Н 7 метилпропиламин, СН 3 N(С 6 Н 5) 2 метилдифениламин. Правила допускают также составлять название, взяв за основу углеводород, в котором аминогруппу рассматривают как заместитель. В таком случае ее положение указывают с помощью числового индекса: С 5 Н 3 С 4 Н 2 С 3 Н(NН 2)С 2 Н 2 С 1 Н 3 3-аминопентан (верхние числовые индексы синего цвета указывают порядок нумерации атомов С). Для некоторых аминов сохранились тривиальные (упрощенные) названия: С 6 Н 5 NH 2 анилин (название по правилам номенклатуры фениламин).
В некоторых случаях применяют устоявшиеся названия, которые представляют собой искаженные правильные названия: Н 2 NСН 2 СН 2 ОН моноэтаноламин (правильно 2-аминоэтанол); (ОНСН 2 СН 2) 2 NH диэтаноламин, правильное название бис(2-гидроксиэтил)амин. Тривиальные, искаженные и систематические (составленные по правилам номенклатуры) названия довольно часто сосуществуют в химии.
Физические свойства аминов.
Первые представители ряда аминов метиламин CH 3 NH 2 , диметиламин (CH 3) 2 NH, триметиламин (CH 3) 3 N и этиламин C 2 H 5 NH 2 при комнатной температуре газообразные, далее при увеличении числа атомов в R амины становятся жидкостями, а при увеличении длины цепи R до 10 атомов С кристаллическими веществами. Растворимость аминов в воде убывает по мере увеличения длины цепи R и при возрастании числа органических групп, связанных с азотом (переход к вторичным и третичным аминам). Запах аминов напоминает запах аммиака, высшие (с большими R) амины практически лишены запаха.
Химические свойства аминов.
Отличительная способность аминов присоединять нейтральные молекулы (например, галогеноводороды HHal, с образованием органоаммониевых солей, подобных аммонийным солям в неорганической химии. Для образования новой связи азот предоставляет неподеленную электронную пару, исполняя роль донора. Участвующий в образовании связи протон Н + (от галогеноводорода) играет роль акцептора (приемника), такую связь называют донорно-акцепторной (рис. 1). Возникшая ковалентная связь NH полностью эквивалентна имеющимся в амине связям NH.
Третичные амины также присоединяют HCl, но при нагревании полученной соли в растворе кислоты она распадается, при этом R отщепляется от атома N:
(C 2 H 5) 3 N + HCl ® [(C 2 H 5) 3 N H]Сl
[(C 2 H 5) 3 N H]Сl ® (C 2 H 5) 2 N H + C 2 H 5 Сl
При сравнении этих двух реакций видно, что C 2 H 5 -группа и Н, как бы меняются местами, в итоге из третичного амина образуется вторичный.
Растворяясь в воде, амины по такой же схеме захватывают протон, в результате в растворе появляются ионы ОН , что соответствует образованию щелочной среды, ее можно обнаружить с помощью обычных индикаторов.
C 2 H 5 N H 2 + H 2 O ® + + OH
С образованием донорно-акцепторной связи амины могут присоединять не только HCl, но и галогеналкилы RCl, при этом образуется новая связь NR, которая также эквивалентна уже имеющимся. Если в качестве исходного взять третичный амин, то получается соль тетраалкиламмония (четыре группы R у одного атома N):
(C 2 H 5) 3 N + C 2 H 5 I ® [(C 2 H 5) 4 N ]I
Эти соли, растворяясь в воде и некоторых органических растворителях, диссоциируют (распадаются), образуя ионы:
[(C 2 H 5) 4 N ]I ® [(C 2 H 5) 4 N ] + + I
Такие растворы, как и все растворы, содержащие ионы, проводят электрический ток. В тетраалкиламмониевых солях можно заменить галоген НО-группой:
[(CH 3) 4 N ]Cl + AgOH ® [(CH 3) 4 N ]OH + AgCl
Получающийся гидроксид тетраметиламмония представляет собой сильное основание, по свойствам близкое к щелочам.
Первичные и вторичные амины взаимодействуют с азотистой кислотой HON=O, однако реагируют они различным образом. Из первичных аминов образуются первичные спирты:
C 2 H 5 N H 2 + HN O 2 ® C 2 H 5 OH + N 2 +H 2 O
В отличие от первичных, вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины соединения, содержащие фрагмент >NN = O:
(C 2 H 5) 2 N H + HN O 2 ® (C 2 H 5) 2 N N =O + H 2 O
Третичные амины при обычной температуре с азотистой кислотой не реагируют, таким образом, азотистая кислота является реагентом, позволяющим различить первичные, вторичные и третичные амины.
При конденсации аминов с карбоновыми кислотами образуются амиды кислот соединения с фрагментом С(О)N
Конденсация аминов с альдегидами и кетонами приводит к образованию так называемых оснований Шиффа соединений, содержащих фрагмент N=C2.
При взаимодействии первичных аминов с фосгеном Cl 2 С=O образуются соединения с группировкой N=C=O, называемые изоцианатами (рис. 2Г, получение соединения с двумя изоцианатными группами).
Среди ароматических аминов наиболее известен анилин (фениламин) С 6 Н 5 NH 2 . По свойствам он близок к алифатическим аминам, но его основность выражена слабее в водных растворах он не образует щелочную среду. Как и алифатические амины, с сильными минеральными кислотами он может образовывать аммониевые соли [С 6 Н 5 NH 3 ] + Сl . При взаимодействии анилина с азотистой кислотой (в присутствии HCl) образуется диазосоединение, содержащее фрагмент RN=N, оно получается в виде ионной соли, называемой солью диазония (рис. 3А). Таким образом, взаимодействие с азотистой кислотой идет не так, как в случае алифатических аминов. Бензольное ядро в анилине обладает реакционной способностью, характерной для ароматических соединений (см . АРОМАТИЧНОСТЬ), при галогенировании атомы водорода в орто - и пара -положениях к аминогруппе замещаются, получаются хлоранилины с различной степенью замещения (рис. 3Б). Действие серной кислоты приводит к сульфированию в пара -положение к аминогруппе, образуется так называемая сульфаниловая кислота (рис. 3В).
Получение аминов.
При взаимодействии аммиака с галогеналкилами, например RCl, образуется смесь первичных, вторичных и третичных аминов. Образующийся побочный продукт HCl присоединяется к аминам, образуя аммониевую соль, но при избытке аммиака соль разлагается, что позволяет проводить процесс вплоть до образования четвертичных аммониевых солей (рис. 4А). В отличие от алифатических галогеналкилов, арилгалогениды, например, С 6 Н 5 Cl, реагируют с аммиаком с большим трудом, синтез возможен только при катализаторах, содержащих медь. В промышленности алифатические амины получают каталитическим взаимодействием спиртов с NH 3 при 300500° С и давлении 120 МПа, в результате получают смесь первичных, вторичных и третичных аминов(рис. 4Б).
При взаимодействии альдегидов и кетонов с аммонийной солью муравьиной кислоты HCOONH 4 образуются первичные амины (рис. 4В), а реакция альдегидов и кетонов с первичными аминами (в присутствии муравьиной кислоты НСООН) приводит к вторичным аминам (рис. 4Г).
Нитросоединения (содержащие группу NO 2) при восстановлении образуют первичные амины. Этот метод, предложенный Н.Н.Зининым, мало применяется для алифатических соединений, но важен для получения ароматических аминов и лег в основу промышленного производства анилина (рис. 4Д).
Как отдельные соединения амины применяются мало, например, в быту используется полиэтиленполиамин [-C 2 H 4 NH-] n (торговое название ПЭПА) как отвердитель эпоксидных смол. Основное применение аминов как промежуточные продукты при получении различных органических веществ. Ведущая роль принадлежит анилину, на основе которого производится широкий спектр анилиновых красителей, причем цветовая «специализация» закладывается уже на стадии получения самого анилина. Сверхчистый анилин без примеси гомологов называют в промышленности «анилин для синего» (имеется в виду цвет будущего красителя). «Анилин для красного» должен содержать, помимо анилина, смесь орто - и пара -толуидина (СН 3 С 6 Н 4 NH 2).
Алифатические диамины исходные соединения для получения полиамидов, например, найлона (рис. 2), широко применяемого для изготовления волокон, полимерных пленок, а также узлов и деталей в машиностроении (полиамидные зубчатые передачи).
Из алифатических диизоцианатов (рис. 2) получают полиуретаны, которые обладают комплексом технически важных свойств: высокой прочностью в сочетании с эластичностью и очень высоким сопротивлением истиранию (полиуретановые обувные подошвы), а также хорошей адгезией к широкому кругу материалов (полиуретановые клеи). Широко их применяют и во вспененной форме (пенополиуретаны).
На основе сульфаниловой кислоты (рис. 3) синтезируют противовоспалительные лекарственные препараты сульфаниламиды.
Соли диазония (рис. 2) применяют в фоточувствительных материалах для светокопирования, которое позволяет получать изображение, минуя обычную галоидосеребряную фотографию (см . СВЕТОКОПИРОВАНИЕ).
Михаил Левицкий