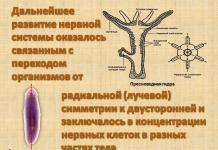
ОПРЕДЕЛЕНИЕ
Хлорид аммония представляет собой малоустойчивый мелкокристаллический порошок белого цвета. Летуч. Он хорошо растворяется в воде (гидролизуется). Кристаллогидратов не образует.
Рис. 1. Хлорид аммония. Внешний вид.
Основные характеристики хлорида аммония приведены в таблице ниже:
Получение хлорида аммония
Получение хлорида аммония в промышленных масштабах заключается в упаривании маточного раствора, остающегося после отделения гидрокарбоната натрия, образующегося по следующей реакции:
NaCl + H 2 O + CO 2 + NH 3 = NaHCO 3 ↓ + NH 4 Cl.
В лабораторных условиях эту соль получают, используя такие реакции, как
8NH 3 + 3Cl 2 = 6NH 4 Cl + N 2 ;
NH 3 + HCl = NH 4 Cl.
Химические свойства хлорида аммония
Хлорид аммония - это средняя соль, образованная слабым основанием - гидроксидом аммония (NH 4 OH) и сильной кислотой - соляной (хлороводородной) (HCl). В водном растворе гидролизуется. Гидролиз протекает по катиону. Наличие катионов Н + свидетельствует о кислом характере среды.
NH 4 Cl ↔NH 4 + + Cl — ;
NH 4 + + HOH ↔ NH 4 OH + H + ;
NH 4 + + Cl — + HOH ↔ NH 4 OH + Cl — + H + ;
NH 4 Cl + H 2 O ↔ NH 4 OH +HCl.
При нагревании хлорид аммония как бы возгоняется - разлагается на аммиак и хлороводород, которые на холодных частях сосуда вновь соединяются в хлорид аммония:
NH 4 Cl↔ NH 3 + HCl.
Хлорид аммония разлагается концентрированной серной кислотой и щелочами:
2NH 4 Cl + H 2 SO 4 (conc) = (NH 4) 2 SO 4 + 2HCl;
NH 4 Cl + NaOH = NaCl + NH 3 + H 2 O;
2NH 4 Cl + Ca(OH) 2 = 2NH 3 + CaCl 2 + 2H 2 O (t = 200 o C).
Он реагирует с хлором (1), типичными металлами (2), оксидами (3) и нитритами металлов (4):
NH 4 Cl + 3Cl 2 = Cl 3 N + 4HCl (t = 60 - 70 o C) (1);
2NH 4 Cl + Mg = MgCl 2 + H 2 + 2NH 3 (2);
2NH 4 Cl + 4CuO = N 2 + 4H 2 O + CuCl 2 + 3Cu (t = 300 o C) (3);
NH 4 Cl + KNO 2 = N 2 + KCl + 2H 2 O (4).
Применение хлорида аммония
Хлорид аммония, или нашатырь, применяется в красильном деле, в ситцепечатании, при паянии и лужении, а также в гальванических элементах. Применение хлорида аммония при паянии основано на том, что он способствует удалению с поверхности металла оксидных пленок, благодаря чему припой хорошо пристает к металлу. При соприкосновении сильно нагретого металла с хлоридом аммония оксиды, находящиеся на поверхности металла, либо восстанавливаются, либо переходят в хлориды. Последние, будучи более летучи, чем оксиды, удаляются с поверхности металла. Для случая меди и железа основные происходящие при этом процессы можно выразить такими уравнениями:
4CuO + NH 4 Cl = 3Cu + CuCl 2 + N 2 + 4H 2 O;
Fe 3 O 4 + 8NH 4 Cl = FeCl 2 + 2FeCl 3 + 8NH 3 + 4H 2 O.
Примеры решения задач
ПРИМЕР 1
| Задание | Какую массу хлорида аммония можно получить при взаимодействии 17,7 г хлороводорода и 12 л аммиака (н.у.)? Какой объем 0,06М раствора можно приготовить из этой массы соли? |
| Решение | Запишем уравнение реакции:
NH 3 + HCl = NH 4 Cl. Найдем количество моль хлороводорода (молярная масса - 36,5 г/моль) и аммиака, вступивших в реакцию используя данные указанные в условии задачи: n(HCl) = m (HCl) / M (HCl); n (HCl) = 17,7 / 36,5 = 0,5моль. n(NH 3) = V (NH 3) / V m ; n (NH 3) = 12 / 22,4 = 0,54 моль. Согласно уравнению задачи n (HCl):n (NH 3) = 1:1. Это означает, что аммиак находится в избытке и все дальнейшие расчеты следует вести по хлороводороду. Найдем количество вещества и массу образовавшегося хлорида аммония (молярная масса 53,5 г/моль): n (HCl): n (NH 4 Cl) = 1:1; n (NH 4 Cl) = n (HCl) = 0,5моль. m (NH 4 Cl)= n (NH 4 Cl)×M (NH 4 Cl); m (NH 4 Cl)=0,5×53,5 = 26,75 г. Рассчитаем объем 0,06М раствора, который можно получить из 26,75 г хлорида аммония: V(NH 4 Cl) = n (NH 4 Cl)/ c (NH 4 Cl); V (NH 4 Cl)=0,5/ 0,06= 8,33 л. |
| Ответ | Масса хлорида аммония равна 26,75 г, объем 0,06М раствора - 8,33 л (833 мл). |
170133 0
Каждый атом обладает некоторым числом электронов.
Вступая в химические реакции, атомы отдают, приобретают, либо обобществляют электроны, достигая наиболее устойчивой электронной конфигурации. Наиболее устойчивой оказывается конфигурация с наиболее низкой энергией (как в атомах благородных газов). Эта закономерность называется "правилом октета" (рис. 1).
Рис. 1.
Это правило применимо ко всем типам связей . Электронные связи между атомами позволяют им формировать устойчивые структуры, от простейших кристаллов до сложных биомолекул, образующих, в конечном счете, живые системы. Они отличаются от кристаллов непрерывным обменом веществ. При этом многие химические реакции протекают по механизмам электронного переноса , которые играют важнейшую роль в энергетических процессах в организме.
Химическая связь - это сила, удерживающая вместе два или несколько атомов, ионов, молекул или любую их комбинацию .
Природа химической связи универсальна: это электростатическая сила притяжения между отрицательно заряженными электронами и положительно заряженными ядрами, определяемая конфигурацией электронов внешней оболочки атомов. Способность атома образовывать химические связи называется валентностью , или степенью окисления . С валентностью связано понятие о валентных электронах - электронах, образующих химические связи, то есть находящихся на наиболее высокоэнергетических орбиталях. Соответственно, внешнюю оболочку атома, содержащую эти орбитали, называют валентной оболочкой . В настоящее время недостаточно указать наличие химической связи, а необходимо уточнить ее тип: ионная, ковалентная, диполь-дипольная, металлическая.
Первый тип связи - ионная связь
В соответствии с электронной теорией валентности Льюиса и Косселя, атомы могут достичь устойчивой электронной конфигурации двумя способами: во-первых, теряя электроны, превращаясь в катионы , во-вторых, приобретая их, превращаясь в анионы . В результате электронного переноса благодаря электростатической силе притяжения между ионами с зарядами противоположного знака образуется химическая связь, названная Косселем «электровалентной » (теперь ее называют ионной ).
В этом случае анионы и катионы образуют устойчивую электронную конфигурацию с заполненной внешней электронной оболочкой. Типичные ионные связи образуются из катионов Т и II групп периодической системы и анионов неметаллических элементов VI и VII групп (16 и 17 подгрупп - соответственно, халькогенов и галогенов ). Связи у ионных соединений ненасыщенные и ненаправленные, поэтому возможность электростатического взаимодействия с другими ионами у них сохраняется. На рис. 2 и 3 показаны примеры ионных связей, соответствующих модели электронного переноса Косселя.
Рис. 2.
Рис. 3. Ионная связь в молекуле поваренной соли (NaCl)
Здесь уместно напомнить о некоторых свойствах, объясняющих поведение веществ в природе, в частности, рассмотреть представление о кислотах и основаниях .
Водные растворы всех этих веществ являются электролитами. Они по-разному изменяют окраску индикаторов . Механизм действия индикаторов был открыт Ф.В. Оствальдом. Он показал, что индикаторы представляют собой слабые кислоты или основания, окраска которых в недиссоциированном и диссоциированном состояниях различается.
Основания способны нейтрализовать кислоты. Не все основания растворимы в воде (например, нерастворимы некоторые органические соединения, не содержащие ‑ ОН-групп, в частности, триэтиламин N(С 2 Н 5) 3) ; растворимые основания называют щелочами .
Водные растворы кислот вступают в характерные реакции:
а) с оксидами металлов - с образованием соли и воды;
б) с металлами - с образованием соли и водорода;
в) с карбонатами - с образованием соли, СO 2 и Н 2 O .
Свойства кислот и оснований описывают несколько теорий. В соответствие с теорией С.А. Аррениуса, кислота представляет собой вещество, диссоциирующее с образованием ионов Н + , тогда как основание образует ионы ОН ‑ . Эта теория не учитывает существования органических оснований, не имеющих гидроксильных групп.
В соответствие с протонной теорией Бренстеда и Лоури, кислота представляет собой вещество, содержащее молекулы или ионы, отдающие протоны (доноры протонов), а основание - вещество, состоящее из молекул или ионов, принимающие протоны (акцепторы протонов). Отметим, что в водных растворах ионы водорода существуют в гидратированной форме, то есть в виде ионов гидроксония H 3 O + . Эта теория описывает реакции не только с водой и гидроксидными ионами, но и осуществляющиеся в отсутствие растворителя или с неводным растворителем.
Например, в реакции между аммиаком NH 3 (слабым основанием) и хлороводородом в газовой фазе образуется твердый хлорид аммония, причем в равновесной смеси двух веществ всегда присутствуют 4 частицы, две из которых - кислоты, а две другие - основания:
Эта равновесная смесь состоит из двух сопряженных пар кислот и оснований:
1) NH 4 + и NH 3
2) HCl и Сl ‑
Здесь в каждой сопряженной паре кислота и основание различаются на один протон. Каждая кислота имеет сопряженное с ней основание. Сильной кислоте соответствует слабое сопряженное основание, а слабой кислоте - сильное сопряженное основание.
Теория Бренстеда-Лоури позволяет объяснить уникальность роли воды для жизнедеятельности биосферы. Вода, в зависимости от взаимодействующего с ней вещества, может проявлять свойства или кислоты, или основания. Например, в реакциях с водными растворами уксусной кислоты вода является основанием, а с водными растворами аммиака - кислотой.
1) СН 3 СООН + Н 2 O ↔ Н 3 O + + СН 3 СОО ‑ . Здесь молекула уксусной кислоты донирует протон молекуле воды;
2) NH 3 + Н 2 O ↔ NH 4 + + ОН ‑ . Здесь молекула аммиака акцептирует протон от молекулы воды.
Таким образом, вода может образовывать две сопряженные пары:
1) Н 2 O (кислота) и ОН ‑ (сопряженное основание)
2) Н 3 О + (кислота) и Н 2 O (сопряженное основание).
В первом случае вода донирует протон, а во втором - акцептирует его.
Такое свойство называется амфипротонностью . Вещества, способные вступать в реакции в качестве и кислот, и оснований, называются амфотерными . В живой природе такие вещества встречаются часто. Например, аминокислоты способны образовывать соли и с кислотами, и с основаниями. Поэтому пептиды легко образуют координационные соединения с присутствующими ионами металлов.
Таким образом, характерное свойство ионной связи - полное перемещение нары связывающих электронов к одному из ядер. Это означает, что между ионами существует область, где электронная плотность почти нулевая.
Второй тип связи - ковалентная связь
Атомы могут образовывать устойчивые электронные конфигурации путем обобществления электронов.
Такая связь образуется, когда пара электронов обобществляется по одному от каждого атома. В таком случае обобществленные электроны связи распределены между атомами поровну. Примерами ковалентной связи можно назвать гомоядерные двухатомные молекулы Н 2 , N 2 , F 2 . Этот же тип связи имеется у аллотропов O 2 и озона O 3 и у многоатомной молекулы S 8 , а также у гетероядерных молекул хлороводорода НСl , углекислого газа СO 2 , метана СH 4 , этанола С 2 Н 5 ОН , гексафторида серы SF 6 , ацетилена С 2 Н 2 . У всех этих молекул электроны одинаково общие, а их связи насыщенные и направлены одинаково (рис. 4).
Для биологов важно, что у двойной и тройной связей ковалентные радиусы атомов по сравнению с одинарной связью уменьшены.
Рис. 4. Ковалентная связь в молекуле Сl 2 .
Ионный и ковалентный типы связей - это два предельных случая множества существующих типов химических связей, причем на практике большинство связей промежуточные.
Соединения двух элементов, расположенных в противоположных концах одного или разных периодов системы Менделеева, преимущественно образуют ионные связи. По мере сближения элементов в пределах периода ионный характер их соединений уменьшается, а ковалентный - увеличивается. Например, галогениды и оксиды элементов левой части периодической таблицы образуют преимущественно ионные связи (NaCl, AgBr, BaSO 4 , CaCO 3 , KNO 3 , CaO, NaOH ), а такие же соединения элементов правой части таблицы - ковалентные (Н 2 O, СO 2 , NH 3 , NO 2 , СН 4 , фенол C 6 H 5 OH , глюкоза С 6 H 12 О 6 , этанол С 2 Н 5 ОН ).
Ковалентная связь, в свою очередь, имеет еще одну модификацию.
У многоатомных ионов и в сложных биологических молекулах оба электрона могут происходить только из одного атома. Он называется донором электронной пары. Атом, обобществляющий с донором эту пару электронов, называется акцептором электронной пары. Такая разновидность ковалентной связи названа координационной (донорно-акцепторной , или дативной ) связью (рис. 5). Этот тип связи наиболее важен для биологии и медицины, поскольку химия наиболее важных для метаболизма d-элементов в значительной степени описывается координационными связями.
Pиc. 5.
Как правило, в комплексном соединении атом металла выступает акцептором электронной пары; наоборот, при ионных и ковалентных связях атом металла является донором электрона.
Суть ковалентной связи и ее разновидности - координационной связи - можно прояснить с помощью еще одной теории кислот и оснований, предложенной ГН. Льюисом. Он несколько расширил смысловое понятие терминов «кислота» и «основание» по теории Бренстеда-Лоури. Теория Льюиса объясняет природу образования комплексных ионов и участие веществ в реакциях нуклеофильного замещения, то есть в образовании КС.
Согласно Льюису, кислота - это вещество, способное образовывать ковалентную связь путем акцептирования электронной пары от основания. Льюисовым основанием названо вещество, обладающее неподеленной электронной парой, которое, донируя электроны, образует ковалентную связь с Льюисовой кислотой.
То есть теория Льюиса расширяет круг кислотно-основных реакций также на реакции, в которых протоны не участвуют вовсе. Причем сам протон, по этой теории, также является кислотой, поскольку способен акцептировать электронную пару.
Следовательно, согласно этой теории, катионы являются Льюисовыми кислотами, а анионы - Льюисовыми основаниями. Примером могут служить следующие реакции:
Выше отмечено, что подразделение веществ на ионные и ковалентные относительное, поскольку полного перехода электрона от атомов металла к акцепторным атомам в ковалентных молекулах не происходит. В соединениях с ионной связью каждый ион находится в электрическом поле ионов противоположного знака, поэтому они взаимно поляризуются, а их оболочки деформируются.
Поляризуемость определяется электронной структурой, зарядом и размерами иона; у анионов она выше, чем у катионов. Наибольшая поляризуемость среди катионов - у катионов большего заряда и меньшего размера, например, у Hg 2+ , Cd 2+ , Pb 2+ , Аl 3+ , Тl 3+ . Сильным поляризующим действием обладает Н + . Поскольку влияние поляризации ионов двустороннее, она значительно изменяет свойства образуемых ими соединений.
Третий тип связи - диполь-дипольная связь
Кроме перечисленных типов связи, различают еще диполь-дипольные межмолекулярные взаимодействия, называемые также вандерваалъсовыми .
Сила этих взаимодействий зависит от природы молекул.
Выделяют взаимодействия трех типов: постоянный диполь - постоянный диполь (диполь-дипольное притяжение); постоянный диполь - индуцированный диполь (индукционное притяжение); мгновенный диполь - индуцированный диполь (дисперсионное притяжение, или лондоновские силы; рис. 6).
Рис. 6.
Диполь-дипольным моментом обладают только молекулы с полярными ковалентными связями (HCl, NH 3 , SO 2 , Н 2 O, C 6 H 5 Cl ), причем сила связи составляет 1-2 дебая (1Д = 3,338 × 10 ‑30 кулон-метра - Кл × м).
В биохимии выделяют еще один тип связи - водородную связь, являющуюся предельным случаем диполь-дипольного притяжения. Эта связь образована притяжением между атомом водорода и электроотрицательным атомом небольшого размера, чаще всего - кислородом, фтором и азотом. С крупными атомами, обладающими аналогичной электроотрицательностью (например, с хлором и серой), водородная связь оказывается значительно более слабой. Атом водорода отличается одной существенной особенностью: при оттягивании связывающих электронов его ядро - протон - оголяется и перестает экранироваться электронами.
Поэтому атом превращается в крупный диполь.
Водородная связь, в отличие от вандерваальсовой, образуется не только при межмолекулярных взаимодействиях, но и внутри одной молекулы - внутримолекулярная водородная связь. Водородные связи играют в биохимии важную роль, например, для стабилизации структуры белков в виде а-спирали, или для образования двойной спирали ДНК (рис. 7).
Рис.7.
Водородная и вандерваальсовая связи значительно слабее, чем ионная, ковалентная и координационная. Энергия межмолекулярных связей указана в табл. 1.
Таблица 1. Энергия межмолекулярных сил
Примечание : Степень межмолекулярных взаимодействий отражают показатели энтальпии плавления и испарения (кипения). Ионным соединениям требуется для разделения ионов значительно больше энергии, чем для разделения молекул. Энтальпии плавления ионных соединений значительно выше, чем молекулярных соединений.
Четвертый тип связи - металлическая связь
Наконец, имеется еще один тип межмолекулярных связей - металлический : связь положительных ионов решетки металлов со свободными электронами. В биологических объектах этот тип связи не встречается.
Из краткого обзора типов связей выясняется одна деталь: важным параметром атома или иона металла - донора электронов, а также атома - акцептоpa электронов является его размер .
Не вдаваясь в детали, отметим, что ковалентные радиусы атомов, ионные радиусы металлов и вандерваальсовы радиусы взаимодействующих молекул увеличиваются по мере возрастания их порядкового номера в группах периодической системы. При этом значения радиусов ионов - наименьшие, а вандерваальсовых радиусов - наибольшие. Как правило, при движении вниз по группе радиусы всех элементов увеличиваются, причем как ковалентные, так и вандерваальсовы.
Наибольшее значение для биологов и медиков имеют координационные
(донорно-акцепторные
) связи, рассматриваемые координационной химией.
Медицинская бионеорганика. Г.К. Барашков
Задание №1.
Электронную конфигурацию 1s 2 2s 2 2p 6 имеют частицы:
Объяснение: дана конфигурация частицы, второй энерегтический уровень которой заполнен (как у неона). Если атом натрия отдаст 1 электрон, то примет конфигурацию неона, а если фтор примет один электрон, то тоже станет неоном. Правильный ответ - 34.
Задание №2.
Расположите в порядке увеличения атомного радиуса химические элементы
Объяснение: атомный радиус увеличивается в группе сверху вних и в периоде справа налево, поэтому радиус натрия будет больше, чем радиус магния, а радиус калия - больше, чем натрия. Правильный ответ - 213.
Задание №3.
Степен окисления +2 могут проявлять оба элемента
Объяснение: степень окисления +2 проявляют, обычно, металлы (щелочно-земельные или переходные), так как металлы - хорошие восстановители (то есть отдают электроны), поэтому выберем магний и хром (MgO, CrSO4). А еще такую степень окисления могут проявлять неметаллы, имеющие много степеней окисления, например, углерод и азот (CO, NO). Правильный ответ - 13.
Задание №4.
В хлориде аммония присутствуют химические связи
2. Ковалентные полярные
3. Ковалентные неполярные
4. Водородные
5. Металлические
Объяснение: хлорид аммония - NH4Cl. Водород и азот соединяеются при помощи ковалентной полярной связи, а ион аммония с ионом хлора - при помощи ионной связи (ионная связь соединяет ионы металла и неметалла, но здесь ион аммония ведет себя как металл). Правильный ответ - 12.
Задание №5.
Установите соответствие между формулой вещества и классом, к которому это вещество принадлежит.
Формула вещества
1. Соль средняя
2. Оксид кислотный
3. Оксид несолеобразующий
4. Соль кислая
Объяснение: NH4HSO4 - гидросульфат аммония, кислая соль
KClO4 - перхлорат калия - средняя соль
N2O - несолеобразующий оксид (так как не имеет соответствующей кислоты)
Правильный ответ - 413.
Задание №6.
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует медь
1. Хлорид цинка (р-р)
2. Сульфат натрия (р-р)
3. Разбавленная азотная кислота
4. Концентрированная серная кислота
5. Оксид алюминия
Объяснение: медь стоит в ряду напряжений металлов после водорода, поэтому не может вытеснить цинк и натрий из их солей и алюминий из оксида. Но зато медь реагирует с кислотами:
1. С разбавленной азотной кислотой
3Сu+8HNO3 → 3Cu(NO3)2 + 4H2O + 2NO
2. С концентрированной серной кислотой
Cu + 2H2SO4 (конц) → CuSO4 + SO2 + 2H2O
Правильный ответ - 34.
Задание №7.
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует углекислый газ
1. Оксид железа (III)
2. Оксид кальция
3. Концентрированная азотная кислота
4. Гидроксид хрома (III)
5. Гидроксид калия
Объяснение: СО2 - солеобразующий оксид, значит он реагирует с оксидами щелочно-земельный металлов с образованием солей:
CaO + CO2 → CaCO3
и с гидроксидами щелочных металлов с образованием соли и воды:
CO2 + 2KOH → K2CO3 + H2O
Правильный ответ - 25.
Задание №8.
Гидроксид алюминия реагирует с
Объяснение: Al(OH)3 - нерастворимое основание, имеет амфотерные свойства, значит реагирует как с кислотами:
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
так и с основаниями:
2Al(OH)3 + Sr(OH)2(тв) → Sr(AlO2)2 + 4H2O
Правильный ответ - 14.
Задание №9.
В заданной схеме превращений
N2 → Ca3N2 → NH3
Объяснение: чтобы из молекулярного азота получить нитрид кальция, проведем реакцию с кальцием
3Ca + N2 → Ca3N2
а теперь, чтобы получить аммиак добавим воду
Ca3N2 + 6H2O → 3Ca(OH)2 + 2NH3
Правильный ответ - 13.
Задание №10.
Установите соответствие между формулой вещества и степенью окисления азота в ней
Формула вещества
Степень окисления азота
Объяснение: в ионе аммония, как и в аммиаке, азот имеет степень окисления -3, в NO2F - +5, в NOCl - +3, BaN2O2 - +2. Правильный ответ - 1654.
Задание №11.
Установите соответствие между простыми веществами и формулами реагентов, с которыми они могут взаимодействовать
Формулы реагентов
1. H2SO4(разб), Al
6. H2SO4(разб), S
Объяснение: Br2 - неметалл и из представленного перечня реагирует с гидроксидом калия:
6KOH+3Br2 → 5KBr+KBrO3+3H2O
и вытесняет йод из его соли:
Br2 + 2KI → 2KBr + I2
Водород реагирует с этиленом:
С2Н4 + Н2 → С2Н6
и с кислородом (со взрывом):
2Н2 + О2 → 2Н2О
Сера реагирует с кислородом:
и с алюминием:
3S + 2Al → Al2S3
Натрий реагирует с разбавленной серной кислотой:
Na + H2SO4(разб) → Na2SO4 + H2
и с серой:
2Na + S → Na2S
Правильный ответ - 2356.
Задание №12.
Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит.
Название соединения
А. Изобутан
Б. Бутен-2
В. Пентин-1
Г. Транс-пентен-2
Общая формула
Объяснение: изобутан (как и сам бутан) относится к алканам, они имеют общую формулу CnH2n+2.
Бутен-2 - алкен, общая формула CnH2n.
Пентин-1 - алкин, общая формула CnH2n-2.
Транс-пентен-2 - (изомер пентена-2) относится к алкенам, они имеют общую формулу - CnH2n.
Правильный ответ - 1232.
Задание №13.
Изомерами пентена-2 являются
1. Пентен-1
2. Циклопентан
3. Пентин-2
4. 2-метилпентен-2
5. Метилциклопентан
Объяснение: пентен-2 - алкен, СН3-СН=СН-СН2-СН3.
Это задание можем решать двумя способами:
1. Напишем структурные формулы всех вариантов ответа и роанализируем их
2. Запишем брутто-формулы всех вариантов ответа, ведь изомеры имеют одну и ту же формулу, но разное строение.
Правильный ответ - 12.
Задание №14.
Циклопропан, в отличие отпропана, реагирует с
1. Водородом
2. Кислородом
5. Бромоводородом
Объяснение: циклоалканы, в отличие от алканов, вступают в реакции присоединения, например, с водородом или бромоводородом. Алканам же свойственны реакции замещения. Правильный ответ - 15.
Задание №15.
Из предложенного перечня веществ выберите два вещества, с которыми реагирует пропанол-1.
1. Гидроксид натрия (р-р)
2. 2-метилбутан
4. Оксид углерода (IV)
5. Бромоводородная кислота
Объяснение: пропанол-1 - спирт. Спирты реагируют с металлами:
2СН3-СН2-СН2-ОН + 2К → 2СН3-СН2-СН2-ОК + Н2
И с галогенводородами:
С3Н7OH + HBr → C3H7Br + H2O
Правильный ответ - 35.
Задание №16.
Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
2. Водород
3. Кислород
4. Бромоводород
5. Алюминий
Объяснение: метиламин относится к аминам. Амины окисляются кислородом (как и все органические вещества):
2CH3NH2 + 9/2O2 → N2 + 2CO2 + 5H2O
Аминогруппа обладает основными свойствами и может присоединять галогенводороды:
CH3NH2 + HBr → CH3NH3 + Br -
Правильный ответ - 34.
Задание №17.
В заданной схеме превращений
НСООН → СН3ОН → СН3ОСН3
веществами Х и У соответственно являются:
Объяснение: в первой реакции из ацетальдегида образуется метиловый спирт, то есть происходит восстановление альдегида до соответствующего спирта. Это может произойти при взаимодействии с водородом:
CHOH + H2 → CH3OH
Во второй реакции из метилового спирта образуется диметиловый эфир - это реакция дегидратации (отсоединения воды) происходит в присутствии сильного водоотнимающего агента: 2CH3OH (H2SO4) → CH3OCH3 + H2O.
Правильный ответ - 15.
Задание №18.
Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ.
Реагирующие вещества
А. Метан (изб.) и хлор
Б. Ацетилен и водород
В. Пропан и бром
Г. Циклопропан и водород
Продукт взаимодействия
1. Тетрахлорметан
2. Хлорметан
4. 1-бромпропан
5. 2-бромпропан
Объяснение:
А - метан реагирует с хлором на свету, при этом получается хлорметан:
CH4 + Cl2 (hν) → CH3Cl + HCl
Б - ацетилен присоединяет водород до получения этана
CHΞCH + H2 → CH3-CH3
В - пропан вступает в реакцию галогенирования с бромом, при этом бром присоединяется ко второму атому углерода (по правилу Марковникова)
СН3-СН2-СН3 + Br2 (hν)→ CH3-CH(Br)-CH3 + HBr
Г - циклопропан реагирует с водородом, при этом цикл разрывается и образуется пропан
С3Н6 + Н2 → С3Н8
Правильный ответ - 2356.
Задание №19.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
Реагирующие вещества
А. Этанол и натрий
Б. Этанол и бромоводород
В. Этан и бром
Г. Этанол и метанол
Продукт взаимодействия
1. Этилнатрий
2. Этилат натрия
3. Бромэтан
4. Бромэтен
5. Метилэтанол
6. Метилэтиловый эфир
Объяснение: в реакции этанола с натрием получается этилат натрия:
2C2H5OH + 2Na → 2C2H5ONa + H2
При взаимодействии этанола с бромоводородом аолучается бромэтан и вода
C2H5OH + HBr → C2H5Br + H2O
При взаимодействии этана с бромом на свету получается бромэтан и бромоводород
C2H6 + Br2 (hν)→ C2H5Br + HBr
При взаимодействии спиртов между собой в присутствии сильного водоотнимающего агента - серной кислоты - получаются простые эфиры (в данном случае - метилэтиловый эфир)
C2H5OH + CH3OH (H2SO4)→ C2H5OCH3 + H2O
Правильный ответ - 2336.
Задание №20.
Взаимодействие натрия с водой относится к рекциям
1. Каталитическим
2. Гомогенным
3. Практически необратимым
4. Окислительно-восстановительным
Объяснение: запишем уравнение взаимодействия натрия с водой:
2Na + 2H2O → 2NaOH + H2
В данной реакции водород выделяется из реакционной смеси (и улетает навсегда), то есть в обратном направлении реакция пойти не можнт, то есть она - практически необратима. Натрий меняет степень окисления с 0 на +1, а водород, наоборот забирает элетроны (+1 → 0), значит это окислительно-восстановительная реакция.
Правильный ответ - 34.
Задание №21.
Скорость реакции 2NO + O2 = 2NO2 + Q
уменьшится при
1. Внесении катализатора
2. Уменьшении концентрации NO2
3. Увеличении концентрации NO2
4. Уменьшении давления в системе
5. Уменьшении концентрации кислорода
Объяснение: при уменьшении давления в системе частицы сталкиваются реже между собой, что уменьшает скорость реакции. При уменьшении концентрации кислорода не все молекулы оксида азота (II) могут прореагировать с молекулами кислорода (потому что их стало меньше), это тоже способствует уменьшению скорости реакции. Правильный ответ - 45.
Задание №22.
Установите соответствие между формулой соли и продуктом, выделяющимся на аноде при электролизе водного расвтора этого вещества.
Формула соли
Анодный продукт
1. Кислород
2. Галоген
3. Водород
Объяснение: перед решение данного задания рекомендуем повторить тему "Электролиз" . На аноде оседают анионы. При электролизе водных растворов фосфатов на аноде получается кислород, как при электролизе водных растворов фторидов. А при электролизе водных растворов галогенидов (кроме фтора) выпадает сам галоген. Правильный ответ - 1212.
Задание №23.
Установите соответствие между названием соли и средой ее водного раствора.
Название соли
А. Гидросульфид калия
Б. Гидросульфит натрия
В. Ортофосфат калия
Г. Хлорид хрома (III)
Среда раствора
1. Нейтральная
3. Щелочная
Объяснение: гидросульфид калия образован щелочью - гидроксидом калия и слабой сероводородной кислотой и хоть это и кислая соль, но из-за силы гидроксида ее водный раствор имеет щелочную среду. То же самое можно сказать про ортофосфат калия. В водном растворе гидросульфита натрия константа диссоциации больше константы гидролиза, это означает, что раствор гидросульфита натрия имеет кислую среду, как и раствор хлорида хрома (из-за сильной соляной кислоты и слабого нерастовримого основания). Правильный ответ - 3232.
Задание №24.
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при увеличении давления в системе:
Уравнение реакции
А. N2(г) + 3H2(г) ↔ 2NH3(г)
Б. 2H2(г) + O2(г) ↔ 2H2O(г)
В. H2(г) + Cl2(г) ↔ 2HCl(г)
Г. SO2(г) + Cl2(г) ↔ SO2Cl2(г)
Направление смещенияхимического равновесия
1. В сторону продуктов реакции
2. В сторону исходных веществ
3. Практически не смещается
Объяснение: при увеличении давления равновесие смещается в сторону уменьшения количества газообразных веществ, то есть в сторону понижения давления; при уменьшении давления равновесие смещается в сторону возрастания количеств газообразных веществ, то есть в сторону увеличения давления. Если реакция протекает без изменения числа молекул газообразных веществ, то давление не влияет на положение равновесия в этой системе.
Значит, в первой реакции равновесие сдвинется в сторону продуктов реакции, как и во второй. В третьей реакции количество молекул справа и слева одинаково, поэтому равновесие практически не смещается, и в последней реакции равновесие смещается вправо.
Правильный ответ - 1131.
Задание №25.
Установите соответствие между веществами и реагентом, с помощью которого их можно отличить друг от друга.
Вещества
А. Ацетилен и этилен
Б. Этилен и этан
В. Этандиол-1,2 и этанол
Г. Фенол и этанол
4. H2SO4 (р-р)
Объяснение: аммиачный раствор оксида серебра реагирует с алкинами (ацетиленом), но не с алкенами (этиленом). Для алкенов характерны реакции присоединения (так как они имеют непредельные связи), в отличие от алканов. Отличим этилен и этан при помощи бромной воды. Многоатомные спирты вступают в реакцию с гидроксидом меди, в отличие от одноатомных спиртов (такая реакция является качественной на многоатомные спирты). Фенол и этанол отличим при помощи бромной воды, с которой реагирует фенол. Правильный ответ - 2151.
Задание №26.
Наиболее токсичны для живого организма ионы:
Объяснение:
Ртуть токсична в любой своей форме. Ртуть в природных условиях довольно быстро превращается в летучее токсическое соединение — хлорид метилртути. В организме ионы метилртути быстро попадают в эритроциты, печень и почки, оседают в мозге, вызывая серьезные необратимые кумулятивные нарушения ЦНС. Это приводит, к конце концов, к общему и церебральному параличу, деформации конечностей, особенно пальцев, затрудненному глотанию, конвульсиям и смерти. Ртуть блокирует активность ряда важнейших ферментов, в частности карбоангидразы, карбоксипептидазы, щелочной фосфатазы. Легко замещает кобальт в корриноидах, извращая метаболические реакции, связанные с витамином В12. Повреждение механизма биосинтеза ДНК из-за недостаточности витамина В12 является причиной мегалобластических анемий и наиболее распространенной формы - пернициозной анемии, что приводит к дегенеративным изменениям нервной системы. (Источник - http://www.forens-med.ru/book.php?id=1839)
Медь является необходимым кофактором для нескольких важнейших ферментов, катализирующих разнообразные окислительно-восстановительные реакции, без которых нормальная жизнедеятельность невозможна. Медь входит в качестве необходимого элемента в состав цитохромоксидазы, тироназы и других белков. Их биологическая роль связана с процессами гидроксилирования, переноса кислорода, электронов и окислительного катализа. В тканях здорового организма концентрация меди в течение всей жизн и поддерживается строго постоянной. В норме существует система, препятствующая непрерывному накоплению мед и в тканях путем ограничения ее абсорбции ил и стимуляции ее выведения. Хронический избыток меди в тканях При соответствующих заболеваниях вызывают токсикоз: ведет к остановке роста, гемолизу, снижению содержания гемоглобина, к деградации тканей печени, почек, мозга. Около 95 % меди в организме присутствует в составе гликопротеина крови церулоплазмина. Известен факт недостатка этого белка При болезни Вильсона-Коновалова - врожденном дефиците метаболизма (гепатолентикулярная дегенерация). Из-за генетического дефекта в синтезе церулоплазмина его содержание в крови резко снижено. В результате медь не связывается в комплекс с нормальной для организма константой устойчивости. Это приводит к недостатк у мед и в цеп и реакций метаболизма, приводящей к естественному для здорового организма синтез у соединительной ткани. Для осуществления нормального процесса сшивки мономеров эластина и коллагена не хватает активной Си-лизолоксидазы. С другой стороны «освободившиеся» ионы меди, лишившись по сути единственного нормального потребителя, откладываются в специфических тканях (печень, ядра мозга, почки, эндокринные железы, радужная оболочка глаз), где оказывают прямой токсический эффект. Создается парадоксальная ситуация избытка меди в специфических тканях при ее недостатке в нормальной цепи метаболизма. (Источник - http://www.forens-med.ru/book.php?id=1839).
Правильный ответ - 13.
Задание №27.
К 200 г 5%-ного раствора хлорида аммония добавили 15 г этой же соли и столько же граммов воды. Чему равна массовая доля хлорида аммония в получившемся растворе?
Объяснение: найдем массу чистого хлорида аммония
m(чистого вва) = 200 x 0,05 = 10 г
Найдем массовую долю хлорида аммония в получившемся растворе:
ω(NH4Cl) = 25/230 х 100% = 11%
Ответ: 11%.
Задание №28.
Какой объем азота (н.у.) образуется при полном сгорании 20 л аммиака в избытке кислорода?
Объяснение: запишем уравнение реакции
4NH3 + 3O2 →2N2 + 6H2O
Найдем количество вещества аммиака:
n(NH3) = 20/22,4 = 0,9 моль
Количество вещества азота в два раза меньше, чем количество вещества аммиака (смотрим по коэффициентам: 4 и 2)
Теперь найдем объем получившегося азота:
V(N2) = 0,45 x 22,4 = 10 л
Ответ: 10 л.
Задание №29.
Рассчитайте массу хлорида алюминия, образующегося при действии избытка хлора на 2,7 г алюминия.
Объяснение: запишем уравнение реакции:
2Al + 3Cl2 → 2AlCl3
Найдем количество вещества алюминия, вступившего в реакцию:
n(Al) = 2,7/27 = 0,1 моль
Количество вещества хлорида алюминия равно количеству вещества алюминия так как коэффициенты одинаковы.
n(AlCl3) = n(Al) = 0,1 моль
Теперь найдем массу образовавшегося хлорида алюминия:
m(AlCl3) = 0,1 х (27 + 106,5) = 13,35 г
Ответ: 13,35 г.
Задание №30.
Используя метод электронного баланса, составьте уравнение реакции
K2S + ... + KBrO4 → S + KBr + ...
Определите окислитель и восстановитель.
Объяснение:
Среда в данном растворе щелочная (из-за калия), но гидроскид калия в реакции получается, тогда водород слева будет в виде воды.
K2S + Н2О + KBrO4 → S + KBr + КОН
Бром и сера меняют степени окисления. Запишем баланс.
S -2 -2e → S 0 | 4
Br +7 +8e → Br -1 | 1
Расставим коэффициенты.
4K2S + 4Н2О + KBrO4 → 4S + KBr + 8КОН
Задание №31.
Оксид алюминия сплавили с гидроксидом натрия. Продукт реакции внесли в раствор хлорида аммония. Выделившийся газ с резким запахом поглощен серной кислотой. Образовавшуюся при этом среднюю соль прокалили.
Запишите уравнения описанных реакций.
Объяснение: оксид алюминия реагирует с гидроксидом натрия
Al2O3 + 2NaOH (t) → 2NaAlO2 + H2O
Алюминат натрия реагирует с хлоридом аммония в растворе (добавляем дополнительно воду)
NaAlO2 + NH4Cl +H2O → NaCl + Al(OH)3↓ + NH3
Выделившийся газ - аммиак, реагирует с серной кислотой с образованием сульфата аммония
NH3 + H2SO4 → (NH4)2SO4
Теперь получившийся сульфат аммония подвергаем термическому разложению
(NH4)2SO4 (t) → NH3 + NH4HSO4
Задание №32.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения?
Метан → Х1 → Х2 → этен → этаналь → этанол
При написании уравнений реакций используйте структурные формулы органических соединений.
Объяснение: метан взаимодействует с бромом на свету по реакции радикального замещения
CH4 + Br2 (hν) → CH3Br + HBr
Затем записываем реакцию Вюрца (удвоение алканов) - получаем этан
CH3-CH (Ni, t) → CH2=CH2 + H2
Окисляем кислородом этен в присутствии катализатора
2СH2=CH2 + O2 (kat) → 2CH3CHO
Гидрируем этаналь и получаем этанол
CH3CH=O + H2 → CH3-CH2-OH
Задание 33.
Рассчитайте массовую долю серной кислоты в растворе, полученном смешением 200 мл 15%-ного раствора серной кислоты плотностью 1,2 г/мл и 150 мл 10%-ного раствора нитрата бария плотностью 1,04 г/мл.
Задача 2.
Какие типы связи осуществляются в молекуле NН 4 Сl? Ответ мотивировать.
Решение:
В молекуле NН 4 Сl имеется два вида связи.
а) Донорно-акцепторная связь
. Существование ионов аммония NН 4 + объясняется образованием химической связи по донорно-акцепторному механизму Возникает вопрос: как в нейтральной молекуле NH 3 , где все электронные орбитали заполнены, возникает связь с протоном и образуется ион NН 4 + с четырьмя химическими связями? В молекуле аммиака четыре валентные орбитали атома азота (одна 2s и три 2p) находятся в состоянии sp3-гибридизации. Три из них вовлечены в связи с атомами водорода по ковалентному способу. Одна оставшаяся орбиталь заполнена парой собственных электронов атома азота. Именно эта орбиталь с парой электронов и взаимодействует с протоном, ядром атома водорода, не имеющим своих электронов.
Таким образом, атом азота в молекуле аммиака играет роль донора электронной пары, а протон – роль акцептора:
В ионе NН 4 + все связи, несмотря на различное их происхождение, энергетически равноценны и все углы между связями равны 109°28"
б) Ионная связь
. Связь NН 4 – Сl – ионная. Ионной связью называется химическая связь, осуществляемая за счет электростатического притяжения между ионами,. Соединения, образованные путем притяжения ионов называются ионными. Ионные соединения состоят из отдельных молекул только в парообразном состоянии. В твердом (кристаллическом) состоянии ионные соединения состоят из закономерно расположенных положительных и отрицательных ионов. Молекулы в этом случае отсутствуют.
Определение типа химической связи в химических соединениях, пользуясь шкалой электроотрицательности
Задача 3.
Пользуясь шкалой электроотрицательностей определить тип химической связи в следующих соединенийх: СаСl 2 , Аl 2 О 3 , ТiО 2 , РН 3 . К атому какого элемента смещено электронное облако связи?
Решение:
Электроотрицательность
(ЭО) представляет собой обобщенную характеристику элемента, связанную не с электронами на отдельных орбиталях, а с внешними электронами вообще, определяемую как сумма энергии ионизации и сродства к электрону. Под электроотрицательностью понимают относительную характеристику способности атома, притягивать электронную пару. Если электроотрицательность атомов, образующих молекулу, одинакова или очень близка, то общая электронная пара располагается симметрично по отношению к обоим ядрам.
Если электроотрицательность атомов различная, то электронная пара смещается в сторону более электроотрицательного атома. В этом случае центры (+)
и (-)
зарядов не совпадают, и возникает система (электрический диполь) из двух равных по величине, но противоположных по знаку зарядов (d+ и d-)
, расстояние между которыми (l) называют длиной диполя.
Подобные ковалентные связи называют полярными. Степень полярности такой связи оценивается значением электрического момента диполя - m
, равного произведению эффективного заряда на длину диполя: (m = q · l)
.
Наконец, если разница электроотрицательностей (Dc)
превышает 1,9, то образуется ионная связь – предельный случай ковалентной полярной связи. Её можно рассматривать как электростатическое притяжение, возникающее между разноименно заряженными ионами.
Ионная связь
, в отличие от ковалентной, является ненаправленной, ненасыщенной, а координационные числа в ионных соединениях определяются соотношением радиусов взаимодействующих ионов.
Разница электроотрицательностей элементов
(Dc)СаСl 2 = 3,16 - 1,0 = 2,16 - связь ионная, электронное облако связи смещено в сторону хлора;
(Dc)Аl 2 О 3 = 3,44 - 1,16 = 2,28 - связь ионная, электронное облако связи смещено в сторону кислорода;
(Dc)ТiО 2 = 3,44 - 1,54 = 1,9 полярная ковалентная связь электронное облако связи смещено в сторону кислорода;
(Dc)РН 3 = 2,2 - 2,19 = 0,01 - связь ковалентная неполярная.
Хлористый аммоний (хлорид аммония, нашатырь) - неорганическое соединение, широко использующееся в самых разных областях. С химической точки зрения - соль аммония; формула NH 4 Cl.
Хлорид аммония был известен уже в Древней Греции и Древнем Египте. Одно из его названий, «нашатырь» происходит от египетского «нушадир» - вещества, которое жрецы собирали на стенках пещер, чтобы вдыхать его пары перед церемонией и настраиваться на общение с божественными силами. «Аммоний» ведет историю названия от имени египетского бога Солнца Амона. В Древней Греции вещество добывали из сажи, которая образовывалась на стенках дымоходов в результате горения верблюжьего навоза, служившего грекам топливом (хлористый аммоний получается при разложении выделений животных и человека).
Хлорид аммония встречается в природе в вулканических пещерах и около трещин в земной коре, в виде налета или корочек.
Свойства
NH 4 Cl - белый кристаллический порошок (реактив технической чистоты может быть желтоватым или розовым), слегка гигроскопичный, без запаха, солоноватый на вкус. Хорошо растворяется в воде и жидком аммиаке, с ростом температуры водорастворимость увеличивается. Вступает в реакцию со щелочами с образованием соли, воды и аммиака. В гораздо меньшей степени реактив растворяется в этиловом и метиловом спиртах. Горит с выделением густого белого дыма. Полностью разлагается при температуре свыше 338 °С, а также под действием электрического тока. Горящий хлорид аммония выделяет аммиак, который раздражает органы дыхания.
Водный раствор реактива - это нашатырный спирт, жидкость с резким запахом, который возбуждающе действует на нервную систему. Реактив используется как лекарство, но лечение нашатырным спиртом должно проводиться строго по рекомендации врача, так как передозировка может привести к остановке дыхания и коме (в качестве антидота вводят щелочные растворы, например, натрия гидрокарбонат). К тому же это лекарство имеет противопоказания.
 В промышленности хлористый аммоний получают как побочный продукт при производстве соды. В лаборатории соединение можно синтезировать из хлора и аммиака, или пропусканием аммиака с хлорводородом через раствор поваренной соли.
В промышленности хлористый аммоний получают как побочный продукт при производстве соды. В лаборатории соединение можно синтезировать из хлора и аммиака, или пропусканием аммиака с хлорводородом через раствор поваренной соли.
Хлористый аммоний относится к веществам умеренно опасным (класс 3), работать с ним следует в средствах защиты : резиновых перчатках, защитных очках и респираторе, в помещении с приточно-вытяжной вентиляцией. Нужно следить, чтобы реактив не попал на кожу и слизистые оболочки. Хранить хим. реактив нужно в герметично закрытых многослойных мешках, в крытых помещениях без доступа влаги. Соединение опасно для окружающей среды.
Применение
В цветной металлургии для травления металлов.
- Как составная часть электролитов в гальванике.
- Для удаления оксидной пленки при пайке и лужении стали, для производства сухих батарей в электротехнике.
- В текстильной индустрии - для отверждения клеев и лаков.
- Для получения нашатырного спирта, которым приводят в чувство при потере сознания. Также хлорид аммония является компонентом сердечных противоотечных средств, средств против кашля. Его используют для усиления некоторых мочегонных лекарств.
- В пищепроме это пищевая добавка E510, разрешенная в России и европейских странах. Его применяют для улучшения свойств муки, как загуститель и эмульгатор, для изготовления плодовых и ягодных вин, лакричных конфет, как приправу к рыбе. В последнее время добавка Е 510 применяется все реже из-за подозрений в ее вреде.
- При изготовлении сигнальных дымовых шашек, как дымообразователь.
- В сельском хозяйстве, при выращивании некоторых культур в качестве азотного удобрения на нейтральных и щелочных почвах.
- В аналитической химии и биологии в качестве фиксанала.
- Как составная часть быстрого фиксажа при проявке фотографий.
- При изготовлении фитилей для свечей.
- В быту в разведенном виде - для очистки различных поверхностей и украшений, при стирке.
В магазине «ПраймКемикалсГрупп» вы можете купить