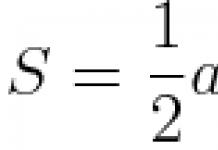Соли азотистой и азотной кислот
Азотные удобрения
9 класс
Тип урока – изучение нового материала.
Вид урока – беседа.
Цели и задачи урока.
Обучающие . Познакомить учащихся со способами получения, свойствами и областями применения нитратов и нитритов. Рассмотреть проблему повышенного содержания нитратов в сельскохозяйственной продукции. Дать представление об азотных удобрениях, их классификации и представителях.
Развивающие . Продолжить развитие умений: выделять главное, устанавливать причинно-следственные связи, вести конспект, проводить эксперимент, применять знания на практике.
Воспитательные. Продолжить формирование научного мировоззрения, воспитание положительного отношения к знаниям.
Методы и методические приемы. Самостоятельная работа учащихся с научно-популярной литературой, подготовка сообщений, выполнение лабораторных опытов и демонстрационного эксперимента, диалогический метод изложения знаний с элементами исследования, текущий контроль знаний с помощью теста.
Структура урока.
Объявление темы, целей.
Сообщение домашнего задания и комментарий к нему.
Изложение нового материала (эвристическаябеседа с опорой на эксперимент).
Текущий контроль знаний с помощью теста.
Подведение итогов урока.
Оборудование и реактивы. Плакат по технике безопасности; таблицы «Разложение нитратов при нагревании», «Классификация азотных удобрений», «Вытеснительный ряд кислот»; тест «Азот и его соединения» (два варианта); карточки с условиями задач.
Для демонстрационного эксперимента
:
демонстрационный штатив для пробирок, спиртовка,
спички, держатель для пробирок, тигельные щипцы,
железная ложечка для сжигания веществ, лучина,
железный лист для сжигания черного пороха,
большие пробирки, вата, пропитанная
концентрированным раствором щелочи, чашка с
песком, три лабораторных штатива;
концентрированные растворы гидроксида натрия и
серной кислоты, кристаллические соли – нитрат
калия, нитрат меди(II), нитрат серебра; древесный
уголек, медная пластина, сера, раствор
дифениламина в концентрированной серной кислоте
(темная склянка, 0,1 г дифениламина на
10 мл H 2 SO 4 (конц.); растворы йодида калия,
разбавленной серной кислоты, нитрита калия; в
демонстрационных пробирках – растительные соки
капусты, кабачка, тыквы; йодкрахмальная бумажка.
Для лабораторных опытов: пробирка с двумя гранулами цинка, три пустые пробирки, стеклянные палочки, две пробирки с кристаллическими нитратами (объемом с горошину) – нитрата бария и нитрата алюминия, лакмус, растворы нитрата меди(II), нитрата серебра, соляной кислоты, хлорида бария, дистиллированная вода.
Эпиграф. «Ни одна наука не нуждается в эксперименте в такой степени как химия» (Майкл Фарадей).
ХОД УРОКА
Сведения по технике безопасности
Все нитраты относятся к огневзрывчатым веществам. Хранить нитраты необходимо отдельно от органических и неорганических веществ. Все опыты с образованием оксида азота(IV) необходимо проводить в больших пробирках, закрытых ватными тампонами, смоченными концентрированным раствором щелочи. Азотную кислоту следует хранить в темных склянках, беречь от огня. Особенно токсичны нитриты.
Домашнее задание
Учебник О.С.Габриеляна «Химия-9», § 26, упр. 7. Сильные ученики получают индивидуальные задания.
Индивидуальные задания
1. Переведите с алхимического языка такую запись: «“Крепкая водка” пожирает “луну”, выпуская “лисий хвост”. Сгущение полученной жидкости порождает “адский камень”, который чернит ткань, бумагу и руки. Чтобы “луна” опять взошла, прокаливай “адский камень” в печи».
Ответ .
«Адский камень» – нитрат серебра – при нагревании разлагается с образованием серебра – «луна взошла»:
2АgNO 3 (кр.) 2Аg + 2NO 2 + O 2 .
 2.
В одном старинном научном трактате описан опыт
получения «красного преципитата»*: «Ртуть
растворяют в азотной кислоте, раствор выпаривают
и остаток нагревают, пока он не сделается
“красным”». Что представляет собой «красный
преципитат»? Напишите уравнения реакций, ведущих
к его образованию, учитывая, что ртуть в
образующихся соединениях имеет степень
окисления +2 и что при действии азотной кислоты на
ртуть выделяется газ, буреющий на воздухе.
2.
В одном старинном научном трактате описан опыт
получения «красного преципитата»*: «Ртуть
растворяют в азотной кислоте, раствор выпаривают
и остаток нагревают, пока он не сделается
“красным”». Что представляет собой «красный
преципитат»? Напишите уравнения реакций, ведущих
к его образованию, учитывая, что ртуть в
образующихся соединениях имеет степень
окисления +2 и что при действии азотной кислоты на
ртуть выделяется газ, буреющий на воздухе.
Ответ . Уравнения реакций :

Оксид ртути(II) HgO в зависимости от способа получения бывает красного или желтого цвета (Hg 2 O – черного цвета). На воздухе ртуть при комнатной температуре не окисляется. При продолжительном нагревании ртуть соединяется с кислородом воздуха, образуя красный оксид ртути(II) – НgО, который при более сильном нагревании снова разлагается на ртуть и кислород:
2НgО = 2Нg + O 2 .
Изучение нового материала
Состав и номенклатура солей азотной кислоты
Учитель. Что означают латинское название «нитрогениум» и греческое «нитрат»?
Ученик. «Нитрогениум» означает «рождающий селитру», а «нитрат» означает «селитра».
Учитель. Нитраты калия, натрия, кальция и аммония называют селитрами . Например, селитры: KNO 3 – нитрат калия (индийская селитра) , NаNО 3 – нитрат натрия (чилийская селитра) , Са(NО 3) 2 – нитрат кальция (норвежская селитра) , NH 4 NO 3 – нитрат аммония (аммиачная или аммонийная селитра, ее месторождений в природе нет). Германская промышленность считается первой в мире, получившей соль NH 4 NO 3 из азота N 2 воздуха и водорода воды, пригодную для питания растений .
Физические свойства нитратов
Учитель. О том, какая взаимосвязь существует между строением вещества и его свойствами, мы узнаем из лабораторного опыта .
Физические свойства нитратов
Задание. В двух пробирках содержатся кристаллические нитраты: Ва(NO 3) 2 и Al(NO 3) 3 . В каждую пробирку прилить по 2 мл дистиллированной воды, перемешать стеклянной палочкой. Наблюдать процесс растворения солей. Растворы хранить до исследования характера среды.
Учитель. Что называют солями?
Ученик . Соли – это сложные вещества, состоящие из ионов металлов и ионов кислотных остатков .
Учитель. Нужно построить логическую цепочку: вид химической связи – тип кристаллической решетки – силы взаимодействия между частицами в узлах решетки – физические свойства веществ .
Ученик. Нитраты относятся к классу солей, поэтому для них характерны ионная связь и ионная кристаллическая решетка, в которой ионы удерживаются электростатическими силами. Нитраты – твердые кристаллические вещества, тугоплавки, растворимы в воде, сильные электролиты .
Получение нитратов и нитритов
Учитель. Назовите десять способов получения солей, основанных на химических свойствах важнейших классов неорганических соединений .
Ученик.
1) Металл + неметалл = соль;
2) металл + кислота = соль + водород;
3) оксид металла + кислота = соль + вода;
4) гидроксид металла + кислота = соль + вода;
5) гидроксид металла + кислотный оксид = соль + вода;
6) оксид металла + оксид неметалла = соль;
7) соль 1 + гидроксид металла (щелочь) = соль 2 + гидроксид металла (нерастворимое основание);
8) соль 1 + кислота (сильная) = соль 2 + кислота (слабая);
10) соль 1 + металл (активный) = соль 2 + металл (менее активный).
Специфические способы получения солей:
12) соль 1 + неметалл (активный) = соль 2 + неметалл (менее активный);
13) амфотерный металл + щелочь = соль + водород;
14) неметалл + щелочь = соль + водород.
Специфический способ получения нитратов и нитритов:
оксид азота(IV) + щелочь = соль1 + соль2 + вода, например (пишет на доске):

Это – окислительно-восстановительная реакция, ее тип – дисмутация, или диспропорционирование.
В присутствии кислорода из NO 2 и NaOH получается не две соли, а одна:

 Тип
окислительно-восстановительной реакции –
межмолекулярный.
Тип
окислительно-восстановительной реакции –
межмолекулярный.
Учитель. Почему опыты с образованием оксида азота(IV) следует проводить в больших пробирках, закрытых ватными тампонами, смоченными водной щелочью?
Ученик. Оксид азота(IV) – ядовитый газ, он взаимодействует со щелочью и обезвреживается.
Химические свойства нитратов
Учащиеся выполняют лабораторные опыты по напечатанной методике.
Свойства нитратов, общие с другими солями
Взаимодействие нитратов с металлами,
кислотами, щелочами, солями
Задание. Отметить признаки каждой реакции, записать молекулярные и ионные уравнения, соответствующие схемам:
Cu(NO 3) 2 + Zn … ,
AgNO 3 + HCl … ,
Cu(NO 3) 2 + NaOH … ,
AgNO 3 + BaCl 2 … .
Гидролиз нитратов
Задание. Определить реакцию среды предложенных растворов солей: Ва(NO 3) 2 и Al(NO 3) 3 . Записать молекулярное и ионные уравнения возможных реакций с указанием среды раствора.
Специфические свойства нитратов и нитритов
Учитель. Все нитраты термически неустойчивы. При нагревании они разлагаются с образованием кислорода. Характер других продуктов реакции зависит от положения металла, образующего нитрат, в электрохимическом ряду напряжений:

Особое положение занимает нитрат аммония, разлагающийся без твердого остатка:
NH 4 NO 3 (кр.) N 2 O + 2H 2 O.
Учитель проделывает демонстрационные опыты.
Опыт 1. Разложение нитрата калия. В большую пробирку поместить 2–3 г кристаллического нитрата калия, нагреть до расплавления соли. В расплав бросить предварительно нагретый в железной ложечке древесный уголек. Учащиеся наблюдают яркую вспышку и горение угля. Под пробирку необходимо подставить чашку с песком.
![]()

Учитель. Почему уголек, опущенный в расплавленную калийную селитру, мгновенно сгорает?
Ученик. Селитра разлагается с образованием газа кислорода, поэтому предварительно нагретый уголек мгновенно сгорает в нем:
С + О 2 = СО 2 .
Опыт 2. Разложение нитрата меди(II). В большую пробирку поместить кристаллический нитрат меди(II) (объемом с горошину), пробирку закрыть ватным тампоном, смоченным концентрированным раствором щелочи. Закрепить пробирку в штативе горизонтально и нагреть.
Учитель. Обратите внимание на признаки реакции .
Учащиеся наблюдают образование бурого газа NО 2 и черного оксида меди(II) СuО.
Ученик у доски составляет уравнение реакции:

Тип окислительно-восстановительной реакции – внутримолекулярный.
Опыт 3. Разложение нитрата серебра. Накалить в пробирке, закрытой ватным тампоном, смоченным концентрированным раствором щелочи, несколько кристалликов нитрата серебра.
Учитель. Какие выделяются газы? Что осталось в пробирке?
Ученик у доски отвечает на вопросы, составляет уравнение реакции:

Тип окислительно-восстановительной реакции – внутримолекулярный. В пробирке остался твердый остаток – серебро.
Учитель. Качественная реакция на нитрат-ион NO 3 – – взаимодействие нитратов c металлической медью при нагревании в присутствии концентрированной серной кислоты или с раствором дифениламина в Н 2 SO 4 (конц.).
Опыт 4. Качественная реакция на ион NO 3 – . В большую сухую пробирку поместить зачищенную медную пластинку, несколько кристалликов нитрата калия, прилить несколько капель концентрированной серной кислоты. Пробирку закрыть ватным тампоном, смоченным концентрированным раствором щелочи и нагреть.
Учитель. Назовите признаки реакции.
Ученик. В пробирке появляются бурые пары оксида азота(IV), что лучше наблюдать на белом экране, а на границе медь – реакционная смесь появляются зеленоватые кристаллы нитрата меди(II) .
Учитель (демонстрирует схему уменьшения относительной силы кислот). В cоответствии с рядом кислот каждая предыдущая кислота может вытеснить из соли последующую .

Ученик у доски составляет уравнения реакций:
КNO 3 (кр.) + Н 2 SO 4 (конц.) = КНSО 4 + НNО 3 ,

Тип окислительно-восстановительной реакции – межмолекулярный.
Учитель. Вторую качественную реакцию на нитрат-ион NO 3 – проведем чуть позже, при исследовании содержания нитратов в продуктах питания .
Качественная реакция на нитрит-ион NO 2 – – взаимодействие нитритов с раствором йодида калия КI, подкисленным разбавленной серной кислотой.
Опыт 5. Качественная реакция на ион NO 2 – . Взять 2–3 капли раствора йодида калия, подкисленного разбавленной серной кислотой, и прилить несколько капель раствора нитрита калия. Нитриты в кислой среде способны окислять йодид-ион I – до свободного I 2 , который обнаруживается йодкрахмальной бумажкой, смоченной в дистиллированной воде.
Учитель. Как должна изменить окраску йодкрахмальная бумажка под действием свободного I 2 ?
Ученик. Простое вещество I 2 обнаруживается по посинению крахмала .
Учитель составляет уравнение реакции:

Учитель. В этой реакции NO 2 – является окислителем. Однако существуют и другие качественные реакции на ион NO 2 – , в которых он является восстановителем. Отсюда можно сделать вывод, что ион NO 3 – проявляет только окислительные свойства, а ион NO 2 – – как окислительные, так и восстановительные свойства .
Применение нитратов и нитритов
Учитель (задает проблемный вопрос). Почему азота в природе много (он входит в состав атмосферы), а растения часто дают плохой урожай из-за азотного голодания?
Ученик. Растения не могут усваивать молекулярный азот N 2 из воздуха. Это проблема «связанного азота». При недостатке азота задерживается образование хлорофилла, поэтому растения имеют бледно-зеленую окраску, как следствие, задерживается рост и развитие растения. Азот – жизненно важный элемент. Без белка нет жизни, а без азота нет белка .
Учитель. Назовите способы усвоения атмосферного азота .
Ученик. Часть связанного азота поступает в почву во время гроз. Химия процесса такова:

Учитель. Какие растения способны повышать плодородие почвы и в чем их особенность?
Ученик. Эти растения (люпин, люцерна, клевер, горох, вика) относятся к семейству бобовых (мотыльковые), на корнях которых развиваются клубеньковые бактерии, способные связывать атмосферный азот, переводя его в соединения, доступные для растений .
Учитель. Снимая урожаи, человек ежегодно уносит вместе с ними огромные количества связанного азота. Эту убыль он покрывает внесением не только органических, но и минеральных удобрений (нитратных, аммиачных, аммонийных). Азотные удобрения вносят под все культуры. Азот усваивается растениями в виде катиона аммония и нитрат-аниона NO 3 – .
Учитель демонcтрирует схему «Классификация азотных удобрений».
Схема

Учитель. Одной из важных характеристик является содержание питательного элемента в удобрении. Расчет питательного элемента для азотных удобрений ведут по содержанию азота .
 |
Растения, связывающие атмосферный азот |
Задача . Какова массовая доля азота в жидком аммиаке и аммиачной селитре?
Формула аммиака – NH 3 .
Массовая доля азота в аммиаке:
(N) = A r (N)/M r (NH 3) 100%,
(N) = 14/17 100% = 82%.
Формула аммиачной селитры – NH 4 NO 3 .
Массовая доля азота в аммиачной селитре:
(N) = 2A r (N)/M r (NH 4 NO 3) 100%,
Влияние нитратов на окружающую среду и организм человека
1-й ученик. Азот как основной питательный элемент влияет на рост вегетативных органов – зеленых стеблей и листьев. Азотные удобрения не рекомендуется вносить поздней осенью или ранней весной, т. к. талые воды смывают до половины удобрений. Важно соблюдать нормы и сроки внесения удобрений, вносить их не сразу, а в несколько приемов. Применять медленно действующие формы удобрений (гранулы, покрытые защитной пленкой), при посадке использовать сорта, склонные к низкому накоплению нитратов. Коэффициент использования азотных удобрений – 40–60%. Избыточное употребление азотных удобрений не только ведет к аккумуляции нитратов в растениях, но и приводит к загрязнению ими водоемов и грунтовых вод. Антропогенными источниками загрязнения водоемов нитратами являются также металлургия, химическая, в том числе целлюлозно-бумажная, и пищевая отрасли промышленности. Одним из признаков загрязнения водоемов является «цветение» воды, вызванное бурным размножением синезеленых водорослей. Особенно интенсивно оно происходит во время таяния снега, летних и осенних дождей. Предельно допустимая концентрация (ПДК) нитратов регламентируется ГОСТом. Для суммы нитрат-ионов в почве принято значение 130 мг/кг, в воде разных водоисточников – 45 мг/л. (Ученики записывают в тетради: ПДК (NO 3 – в почве) – 130 мг/кг, ПДК (NO 3 – в воде) – 45 мг/л.)
Для самих растений нитраты безвредны, а вот для человека и травоядных животных они опасны. Смертельная доза нитратов для человека – 8–15 г, допустимое суточное потребление – 5 мг/кг. Многие растения способны накапливать большие количества нитратов, например: капуста, кабачки, петрушка, укроп, свекла столовая, тыква и др.
Такие растения называют нитратонакопителями. В организм человека 70% нитратов поступает с овощами, 20% – с водой, 6% – с мясом и рыбой. Попадая в организм человека, часть нитратов всасывается в желудочно-кишечном тракте в неизмененном виде, другая часть, в зависимости от присутствия микроорганизмов, значения рН и других факторов, может превращаться в более ядовитые нитриты, аммиак, гидроксиламин NН 2 ОН; в кишечнике из нитратов могут образоваться вторичные нитрозамины R 2 N–N=О, обладающие высокой мутагенной и канцерогенной активностью. Признаки небольшого отравления – слабость, головокружение, тошнота, расстройство желудка и т. д. Снижается работоспособность, возможна потеря сознания.
В организме человека нитраты взаимодействуют с гемоглобином крови, превращая его в метгемоглобин, в котором железо окислено до Fe 3+ и не может служить переносчиком кислорода. Именно поэтому один из признаков острого отравления нитратами – синюшность кожных покровов. Выявлена прямая зависимость между случаями появления злокачественных опухолей и интенсивностью поступления в организм нитратов при избытке их в почве.
Опыт. Исследование содержания нитратов
в продуктах питания
(качественная реакция на нитрат-ион NO 3 –)
В три большие демонстрационные пробирки поместить по 10 мл растительного сока капусты, кабачка, тыквы (на белом фоне). В каждую пробирку прилить по нескольку капель раствора дифениламина в концентрированной серной кислоте.
Синяя окраска раствора будет указывать на присутствие нитрат-ионов:
NO 3 – + дифениламин вещество интенсивного синего цвета.
Синяя окраска присутствовала только в растительном соке кабачка, причем окраска была неинтенсивно-синяя. Следовательно, содержание нитратов в кабачке незначительное, а в капусте с тыквой – и того меньше.
Первая помощь при отравлении нитратами
2-й ученик. Первая помощь при отравлении нитратами – это обильное промывание желудка, прием активированного угля, солевых слабительных – глауберовой соли Na 2 SO 4 10H 2 O и английской соли (горькая соль) MgSO 4 7H 2 O, cвежий воздух .
Уменьшить вредное влияние нитратов на организм человека можно с помощью аскорбиновой кислоты (витамина С); если ее соотношение с нитратами составляет 2:1, то нитрозамины не образуются. Доказано, что прежде всего витамин С, а также витамины Е и А являются ингибиторами – веществами, предотвращающими и тормозящими процессы преобразования нитратов и нитритов в организме человека. Необходимо ввести в рацион питания побольше черной и красной смородины, других ягод и фруктов (кстати, в висячих плодах нитратов практически нет). И еще один естественный нейтрализатор нитратов в организме человека – это зеленый чай .
Причины накопления нитратов в
овощах
и способы выращивания экологически чистой
продукции растениеводства
3-й ученик. Наиболее интенсивно азот поглощается во время роста и развития стеблей и листьев. При созревании семян потребление азота из почвы практически прекращается. Плоды, достигшие полной зрелости, уже не содержат нитратов – происходит полное превращение соединений азота в белки. Но у многих овощей ценится именно незрелый плод (огурцы, кабачки). Удобрять такие культуры азотными удобрениями желательно не позднее чем за 2–3 недели до уборки урожая. Кроме того, полному превращению нитратов в белки препятствуют плохая освещенность, избыточная влажность и несбалансированность питательных элементов (недостаток фосфора и калия). Не следует увлекаться внесезонными тепличными овощами. Например, 2 кг тепличных огурцов, съеденных за один прием, могут вызвать опасное для жизни отравление нитратами. Надо также знать, преимущественно в каких частях растения накапливаются нитраты: у капусты – в кочерыжке, у моркови – в сердцевине, у кабачков, огурцов, арбузов, дыни, картофеле – в кожуре. У дыни и арбуза не следует есть незрелую мякоть, прилежащую к корке. Огурцы лучше почистить и срезать место прикрепления их к стеблю. У зеленных культур нитраты накапливаются в стеблях (петрушка, салат, укроп, сельдерей). Содержание нитратов в различных частях растений неравномерно: в черешках листьев, стебле, корне содержание их в 1,5–4,0 раза выше, чем в листьях. Всемирная организация здравоохранения считает допустимым содержание нитратов в диетических продуктах до 300 мг NO 3 – на 1 кг сырого вещества. (Ученики записывают в тетради: ПДК (NO 3 – в диетических продуктах) – 300 мг/кг.)
Если самое высокое содержание нитратов отмечается в свекле, капусте, салате, зеленом луке, то самое низкое содержание нитратов – в репчатом луке, томатах, чесноке, перце, фасоли.
Чтобы вырастить экологически чистую продукцию, прежде всего необходимо грамотно вносить азотные удобрения в почву: в строго рассчитанных дозах и в оптимальные сроки. Выращивать овощи, особенно зеленные культуры, надо при хорошей освещенности, оптимальных показателях влажности почвы и температуры. И все же для уменьшения содержания нитратов овощные культуры лучше подкармливать органическими удобрениями. Несвоевременное внесение удобрений, особенно в избыточных дозах, в том числе и органического удобрения – навоза, приводит к тому, что поступившие в растение минеральные соединения азота не успевают полностью превратиться в белковые.
4-й ученик. Весной на прилавках магазинов и рынков появляются зеленные культуры: салат, шпинат, зеленый лук, огурцы, выращенные в теплице, в закрытом грунте. Как уменьшить содержание нитратов в них? Перечислим некоторые из них.
1. Такие ранние культуры, как зелень петрушки, укропа, сельдерея, необходимо поставить как букет в воду на прямой солнечный свет. В таких условиях нитраты в листьях в течение 2–3 ч полностью перерабатываются и потом практически не обнаруживаются. После этого зелень можно без опасений употреблять в пишу.
2. Свеклу, кабачки, тыкву перед приготовлением необходимо порезать мелкими кубиками и 2–3 раза залить теплой водой, выдерживая по 5–10 минут. Нитраты хорошо растворимы в воде, особенно теплой, и вымываются водой (посмотрите таблицу растворимости кислот, оснований, солей). При мытье и чистке теряется 10–15% нитратов.
3. Варка овощей снижает содержание нитратов на 50–80%.
4. Уменьшает количество нитратов в овощах квашение, соление, маринование.
5. При долгом хранении содержание нитратов в овощах уменьшается.
А вот сушка, приготовление соков и пюре, наоборот, повышают количество нитратов.
1) варка овощей;
2) очистка от кожуры;
3) удаление участков наибольшего скопления нитратов;
4) вымачивание.
Для того чтобы оценить, насколько реальна опасность отравления нитратами, учащимся предлагается расчетная задача.
Задача . В столовой свекле содержится в среднем 1200 мг нитрат-ионов на 1 кг. При очистке свеклы теряется 10% нитратов, а при варке – еще 40%. Будет ли превышена суточная норма потребления нитратов (325 мг), если ежедневно съедать по 200 г вареной свеклы?
Дано:
m(свеклы) = 1 кг,
с (NO 3 –) = 1200 мг/кг,
m макс (NO 3 – в сутки) = 325 мг,
m (свеклы) = 200 г (0,2 кг),
(потерь при очистке) = 10%,
(потерь при варке) = 40%.
__________________________________
Найти: m (NO 3 – в 200 г вареной свеклы).
Решение
1 кг свеклы – 1200 мг NO 3 – ,
0,2 кг свеклы – х мг NO 3 – .
Отсюда х = 240 мг (NO 3 –).
Общая доля потерь нитрат-ионов:
(потерь NO 3 –) = 10% + 40% = 50%.
Следовательно, в организм попадает половина от 240 мг или 120 мг NO 3 – .
Ответ. После очистки и варки свеклы суточная норма по нитратам (325 мг), содержащимся в 200 г готового продукта (120 мг NO 3 –), не превышена, употреблять в пищу ее можно.
Нитраты в производстве взрывчатых веществ
Учитель. Многие взрывчатые смеси содержат в своем составе окислитель (нитраты металлов или аммония и др.) и горючее (дизельное топливо, алюминий, древесную муку). Поэтому соли – нитрат калия, нитрат бария, нитрат стронция и другие – применяются в пиротехнике .
Какое азотное удобрение вместе с алюминием и древесным углем входит в состав взрывчатой смеси – аммонала?
Ученик. Аммонал содержит также нитрат аммония. Основная реакция, которая протекает при взрыве:
3NН 4 NО 3 + 2Аl 3N 2 + 6Н 2 О + Аl 2 O 3 + Q .
Высокая теплота сгорания алюминия повышает энергию взрыва. Применение нитрата аммония в составе аммонала основано на его свойстве разлагаться при детонации с образованием газообразных веществ:
2NН 4 NО 3 (кр.) = 2N 2 + 4Н 2 О + O 2 .
В руках террористов взрывчатые вещества приносят мирным людям только страдания.
Шесть веков продолжалось господство черного пороха в военном деле. Теперь его применяют в качестве взрывчатого вещества в горном деле, в пиротехнике (ракеты, фейерверки), а также как охотничий порох. Черный или дымный порох – это смесь 75% нитрата калия, 15% древесного угля и 10% серы.
Опыт. Горение черного или дымного пороха
Готовят черный порох смешиванием 7,5 г нитрата калия, 1 г серы и 1,5 г древесного угля. Перед смешиванием каждое вещество измельчают в фарфоровой ступке. Во время демонстрации опыта смесь горочкой помещают на железный лист и поджигают горящей лучиной. Смесь сгорает, образуя облако дыма (тяга).
Учитель. Какую роль играет селитра?
Ученик. Селитра выступает в роли окислителя при нагревании :

Применение нитратов и нитритов в медицине
5-й ученик. Нитрат серебра AgNO 3 , который чернит ткань, бумагу, парты и руки (ляпис), применяют как противомикробное средство для лечения кожных язв, для прижигания бородавок (учитель демонстрирует технику прижигания бородавок на своей руке) и в качестве противовоспалительного средства при хроническом гастрите и язве желудка: пациентам назначают пить 0,05%-й раствор АgNO 3 . Порошкообразные металлы Zn, Мg, Al, cмешанные с нитратом серебра, используют в петардах .
Основный нитрат висмута Вi(ОН) 2 NО 3 назначают внутрь при язвенной болезни желудка и двенадцатиперстной кишки в качестве вяжущего и антисептического средства. Наружно – в мазях, присыпках при воспалительных заболеваниях кожи.
Соль нитрит натрия NaNО 2 применяют в медицине как спазмолитическое средство .
Применение нитритов в пищевой отрасли промышленности
6-й ученик. Нитриты применяют в колбасном производстве: 7 г на 100 кг фарша. Нитриты придают колбасе розовый цвет, без них она серая, как вареное мясо, и не имеет товарного вида. К тому же присутствие нитритов в колбасе необходимо еще и по другой причине: они предотвращают развитие микроорганизмов, выделяющих токсичные яды .
Контроль знаний с помощью теста «Азот и его соединения»
Вариант I
1. Наиболее прочная молекула:
а) Н 2 ; б) F 2 ; в) О 2 ; г) N 2 .
2. Окраска фенолфталеина в растворе аммиака:
а) малиновая; б) зеленая;
в) желтая; г) синяя.
3. Степень окисления +3 у атома азота в соединении:
а) NH 4 NO 3 ; б) NaNО 3 ; в) NО 2 ; г) КNO 2 .
4. При термическом разложении нитрата меди(II) образуются:
а) нитрит меди(II) и О 2 ;
б) оксид азота(IV) и О 2 ;
в) оксид меди(II), бурый газ NO 2 и О 2 ;
г) гидроксид меди(II), N 2 и О 2 .
5. Какой ион образован по донорно-акцепторному механизму?
а) ; б) NO 3 – ; в) Сl – ; г) SO 4 2– .
6. Укажите сильные электролиты:
а) азотная кислота;
б) азотистая кислота;
в) водный раствор аммиака;
г) нитрат аммония.
7. Водород выделяется при взаимодействии:
а) Zn + HNO 3 (разб.);
б) Cu + HCl (р-р);
в) Al + NaOH + H 2 O;
г) Zn + H 2 SO 4 (разб.);
д) Fe + HNO 3 (конц.).
8. Составьте уравнение реакции цинка с очень разбавленной азотной кислотой, если один из продуктов реакции – нитрат аммония. Укажите коэффициент, стоящий перед окислителем.
9.
Дайте названия веществам А, В, С.
Вариант II
1. Cпособом вытеснения воды нельзя собрать:
а) азот; б) водород;
в) кислород; г) аммиак.
2. Реактивом на ион аммония служит раствор:
а) сульфата калия; б) нитрата серебра;
в) гидроксида натрия; г) хлорида бария.
3. При взаимодействии НNО 3 (конц.) с медной стружкой образуется газ:
а) N 2 O; б) NН 3 ; в) NO 2 ; г) Н 2 .
4. При термическом разложении нитрата натрия образуется:
а) оксид натрия, бурый газ NO 2 , O 2 ;
б) нитрит натрия и О 2 ;
в) натрий, бурый газ NO 2 , O 2 ;
г) гидроксид натрия, N 2 , О 2 .
5. Cтепень окисления азота в сульфате аммония:
а) –3; б) –1; в) +1; г) +3.
6. С какими из указанных веществ реагирует концентрированная HNO 3 при обычных условиях?
а) NаОН; б) АgСl; в) Al; г) Fе; д) Сu.
7. Укажите число ионов в сокращенном ионном уравнении взаимодействия сульфата натрия и нитрата серебра:
а) 1; б) 2; в) 3; г) 4.
8. Составьте уравнение взаимодействия магния с разбавленной азотной кислотой, если один из продуктов реакции – простое вещество. Укажите коэффициент, стоящий в уравнении перед окислителем.
9. Напишите уравнения реакций для следующих превращений:
Дайте названия веществам А, В, С, D.
Ответы на вопросы тестов
Вариант I
1 – г; 2 – а; 3 – г; 4 – в; 5 – а; 6 – а, г; 7 – в, г; 8 – 10,

9. А – NH 3 , B – NH 4 NO 3 , C – NO,


Вариант II
1 – г; 2 – в; 3 – в; 4 – б; 5 – а; 6 – а, д; 7 – в,
2Ag + + SO 4 2– = Ag 2 SO 4 ;
8 – 12,

9. А – NO, B – NO 2 , C – HNO 3 , D – NH 4 NO 3 ,

В заключение урока учитель высказывает свое отношение к проделанной учащимися работе, оценивает их выступления и ответы.
ЛИТЕРАТУРА
Габриелян О.С
. Химия-9. М.: Дрофа, 2001; Габриелян
О.С, Остроумов И.Г
. Настольная книга учителя.
Химия. 9 класс. М.: Дрофа, 2002; Пичугина Г.В
.
Обобщение знаний о превращении соединений азота
в почве и в растениях. Химия в школе, 1997, № 7; Харьковская
Н.Л
.,
Ляшенко Л.Ф., Баранова Н.В
. Осторожно – нитраты!
Химия в школе, 1999, № 1; Железнякова Ю.В.,
Назаренко В.М
. Учебно-исследовательские
экологические проекты. Химия в школе, 2000, № 3.
*«Красный преципитат» – это одна из модификаций оксида ртути(II) HgO. (Прим. ред .)
Азотистая кислота
HNO 2 - слабая одноосновная кислота, существует только в разбавленных водных растворах.
Соли азотистой кислоты называются нитритами. Нитриты гораздо более устойчивы, чем HNO 2 , все они токсичны.
Получение:
1. N 2 O 3 + H 2 O = 2HNO 2
Как можно еще получить азотистую кислоту? ()
Какая степень окисления в азотистой кислоте?
Значит, кислота проявляет как окислительные, так и восстановительные свойства.
При действии более сильных окислителей окисляется в HNO 3:
5HNO 2 +2HMnO 4 → 2Mn(NO 3) 2 + HNO 3 + 3H 2 O;
HNO 2 + Cl 2 + H 2 O → HNO 3 + 2HCl.
2HNO 2 + 2HI → 2NO + I 2 ↓ + 2H 2 O – восстановительные свойства
Качественная реакция на нитрит-ион NO 2 – – взаимодействие нитритов с раствором йодида калия КI, подкисленным разбавленной серной кислотой.
Как должна изменить окраску йодкрахмальная бумажка под действием свободного I 2 ?

Получение солей (нитратов и нитритов)
Назовите способы получения солей, которые вам известны? Как можно получить нитраты и нитриты?
1) Металл + неметалл = соль;
2) металл + кислота = соль + водород;
3) оксид металла + кислота = соль + вода;
4) гидроксид металла + кислота = соль + вода;
5) гидроксид металла + кислотный оксид = соль + вода;
6) оксид металла + оксид неметалла = соль;
7) соль 1 + гидроксид металла (щелочь) = соль 2 + гидроксид металла (нерастворимое основание);
8) соль 1 + кислота (сильная) = соль 2 + кислота (слабая);
9) соль 1 + соль 2 = соль 3 + соль 4
10) соль 1 + металл (активный) = соль 2 + металл (менее активный).
Специфический способ получения нитратов и нитритов:

диспропорционирование.
В присутствии избытка кислорода

Соли азотной кислоты – нитраты
нитраты щелочных металлов, кальция, аммония – селитры
KNO 3 - калийная селитра,
NH 4 NO 3 - аммиачная селитра.
Физические свойства:
Все нитраты твёрдые кристаллические вещества, белого цвета, хорошо растворимые в воде. Ядовиты!
Химические свойства нитратов
Взаимодействие нитратов с металлами, кислотами, щелочами, солями
Задание . Отметить признаки каждой реакции, записать молекулярные и ионные уравнения, соответствующие схемам:
Cu(NO 3) 2 + Zn… ,
AgNO 3 + HCl… ,
Cu(NO 3) 2 + NaOH… ,
AgNO 3 + BaCl 2 … .
Разложение нитратов
При нагревании твердых нитратов все они разлагаются с выделением кислорода (исключением является нитрат аммония), при этом их можно разделить на три группы.
Первую группу составляют нитраты щелочных металлов
2КNО 3 = 2КNО 2 + О 2 .
Вторую группу от щелочноземельных металлов до меди включительно
2Сu(NО 3) 2 = 2СuО + 4NО 2 + O 2 ,
Третью группу Ме после Сu
Hg(NО 3) 2 = Нg + 2NО 2 + О 2 ,
Почему азота в природе много (он входит в состав атмосферы), а растения часто дают плохой урожай из-за азотного голодания? (Растения не могут усваивать молекулярный азот из воздуха. При недостатке азота задерживается образование хлорофилла, задерживается рост и развитие растения.)
Назовите способы усвоения атмосферного азота.
(Часть связанного азота поступает в почву во время гроз. Бобовые, на корнях которых развиваются клубеньковые бактерии, способные связывать атмосферный азот, переводя его в соединения, доступные для растений.)
Снимая урожаи, человек ежегодно уносит вместе с ними огромные количества связанного азота. Эту убыль он покрывает внесением не только органических, но и минеральных удобрений (нитратных, аммиачных, аммонийных). Азотные удобрения вносят под все культуры. Азот усваивается растениями в виде катиона аммония и нитрат-аниона NO 3 – .
Доклады учеников
Влияние нитратов на окружающую среду и организм человека
Первая помощь при отравлении нитратами
Причины накопления нитратов в овощах и способы выращивания экологически чистой продукции растениеводства
Три из пяти оксидов азота реагируют с водой, образуя азотистую Н1М0 2 и азотную HN0 3 кислоты.
Азотистая кислота слабая и неустойчивая. Она может присутствовать лишь в небольшой концентрации в охлажденном водном растворе. Практически ее получают действием серной кислоты на раствор соли (чаще всего NaN0 2) при охлаждении почти до 0°С. При попытке повышения концентрации азотистой кислоты из раствора на дно сосуда выделяется синяя жидкость - оксид азота(Ш). При повышении температуры азотистая кислота разлагается но реакции
Оксид азота(1У) реагирует с водой, давая две кислоты (см. выше). Но с учетом разложения азотистой кислоты суммарная реакция N 2 0 4 с водой при нагревании записывается так:
Соли азотистой кислоты (нитриты) достаточно устойчивы. Нитриты калия или натрия можно получить растворением оксида азота(1У) в щелочи:
Образование смеси солей вполне понятно, так как, реагируя с водой, N 2 0 4 образует две кислоты. Нейтрализация щелочью предотвращает разложение неустойчивой азотистой кислоты и приводит к смещению равновесия реакции N 2 0 4 с водой полностью вправо.
Нитриты щелочных металлов получаются также при термическом разложении их нитратов:

Соли азотистой кислоты хорошо растворимы в воде. Растворимость некоторых нитритов исключительно высока. Например, при 25°С коэффициент растворимости нитрита калия равен 314, т.е. в 100 г воды растворяется 314 г соли. Нитриты щелочных металлов термически устойчивы и плавятся без разложения.
В кислой среде нитриты действуют как довольно сильные окислители. Фактически окислительные свойства проявляет образующаяся слабая азотистая кислота. Из растворов иодидов выделяется иод:
Иод обнаруживается по окраске, а оксид азота - по характерному запаху. Азот переходит из СО +3 в СО +2.
Окислители более сильные, чем азотистая кислота, окисляют нитриты до нитратов. В кислой среде раствор перманганата калия обесцвечивается при добавлении нитрита натрия:
Азот переходит из СО +3 в СО +5. Таким образом, азотистая кислота и нитриты проявляют окислительно-восстановительную двойственность.
Нитриты ядовиты, так как они окисляют в гемоглобине железо(П) до железа(Н1) и гемоглобин теряет способность присоединять и переносить кислород в крови. Применение большого количества азотных удобрений значительно ускоряет рост растений, но при этом они содержат в повышенной концентрации нитраты и нитриты. Употребление выращенных таким образом овощей и ягод (арбузы, дыни) приводит к отравлениям.
Огромное практическое значение имеет азотная кислота. В ее свойствах сочетаются сила кислоты (практически полная ионизация в водном растворе), сильные окислительные свойства и способность передавать нитро- группу N0 2 + другим молекулам. Азотную кислоту применяют в больших количествах для производства удобрений. В этом случае она служит источником необходимого для растений азота. Ее применяют для растворения металлов и получения хорошо растворимых солей - нитратов.
Чрезвычайно важным направлением использования азотной кислоты является нитрование органических веществ для получения разнообразных органических продуктов, содержащих нитрогруппы. Среди органических нитросоединений есть лекарственные вещества, красители, растворители, взрывчатые вещества. Ежегодно мировое производство азотной кислоты превышает 30 млн т.
В период до промышленного освоения синтеза аммиака и его окисления азотную кислоту получали из нитратов, например из чилийской селитры NaN0 3 . Селитру нагревали с концентрированной серной кислотой:
Выделяющиеся пары азотной кислоты в охлаждаемом приемнике конденсируются в жидкость с высоким содержанием HN0 3 .
В настоящее время азотную кислоту получают по различным вариантам метода, в котором исходным веществом является оксид азота(П). Как следует из рассмотрения свойств азота, его оксид NO можно получить из азота и кислорода при температуре более 2000°С. Поддержание такой высокой температуры требует большой затраты энергии. Метод был технически осуществлен в 1905 г. в Норвегии. Нагретый воздух проходил через зону горения вольтовой дуги при температуре 3000-3500°С. Выходящие из устройства газы содержали всего 2-3% оксида азота(Н). К 1925 г. мировое производство азотных удобрений по этому способу достигло 42 000 т. По современным масштабам производства удобрений - это очень мало. В дальнейшем расширение производства азотной кислоты пошло по пути окисления аммиака до оксида азота(И).
При обычном горении аммиака образуются азот и вода. Но при проведении реакции при более низкой температуре с применением катализатора окисление аммиака заканчивается образованием NO. Появление NO при пропускании смеси аммиака и кислорода через платиновую сетку было известно уже давно, но этот катализатор не дает достаточно высокого выхода оксида. Использовать этот процесс для заводского производства удалось только в XX в., когда был найден более эффективный катализатор - сплав платины и родия. Металл родий, оказавшийся чрезвычайно необходимым в производстве азотной кислоты, приблизительно в 10 раз более редок, чем платина. С катализатором Pt/Rh в смеси аммиака и кислорода определенного состава при 750°С реакция
дает выход NO до 98%. Этот процесс термодинамически менее выгоден, чем сгорание аммиака до азота и воды (см. выше), но катализатор обеспечивает быстрое соединение атомов азота, остающихся после потери водорода молекулой аммиака, с кислородом, предотвращая образование молекул N 2 .
При охлаждении смеси, содержащей оксид азота(П) и кислород, образуется оксид азота(1У) N0 2 . Далее применяются разные варианты превращения N0 2 в азотную кислоту. Разбавленную азотную кислоту получают растворением NQ 2 в воде при повышенной температуре. Реакция приведена выше (с. 75). Азотную кислоту с массовой долей до 98% получают по реакции в смеси жидкого N 2 0 4 с водой в присутствии газообразного кислорода под большим давлением. В этих условиях образующийся одновременно с азотной кислотой оксид азота(П) успевает окисляться кислородом до N0 2 , который сразу же реагирует с водой. Получается следующая суммарная реакция:
Всю цепочку последовательных реакций превращения атмосферного азота в азотную кислоту можно представить так:

Реакции оксида азота(1У) с водой и кислородом идут довольно медленно, и практически не удается достигнуть полного его превращения в азотную кислоту. Поэтому на заводах, производящих азотную кислоту, всегда происходит выброс оксидов азота в атмосферу. Из заводской трубы выходит рыжеватый дым - «лисий хвост». Окраска дыма обусловлена присутствием N0 2 . На значительном пространстве вокруг большого завода от оксидов азота погибают леса. Особенно чувствительны к воздействию N0 2 хвойные породы деревьев.
Безводная азотная кислота - бесцветная жидкость с плотностью 1,5 г/см 3 , кипящая при 83°С и замерзающая при -41,б°С в прозрачное кристаллическое вещество. На воздухе азотная кислота подобно концентрированной соляной кислоте дымит, так как пары кислоты образуют с водяным паром воздуха капли тумана. Поэтому азотная кислота с малым содержанием воды называется дымящей. Она, как правило, имеет желтую окраску, так как под действием света разлагается с образованием N0 2 . Дымящая кислота применяется сравнительно редко.
Обычно азотная кислота выпускается промышленностью в виде водного раствора с массовой долей 65-68%. Такой раствор называют концентрированной азотной кислотой. Растворы с массовой долей HN0 3 менее 10% - разбавленная азотная кислота. Раствор с массовой долей 68,4% (плотность 1,41 г/см 3) представляет собой азеотропную смесь , кипящую при 122°С. Азеотропная смесь характеризуется одинаковым составом как жидкости, так и пара над ней. Поэтому перегонка азеотропной смеси не приводит к изменению ее состава. В концентрированной кислоте наряду с обычными молекулами HN0 3 присутствуют малодиссоциироваиные молекулы ортоазотной кислоты H 3 N0 4 .
Концентрированная азотная кислота пассивирует поверхность некоторых металлов, например железа, алюминия, хрома. При контакте этих металлов с концентрированной HN() 3 химическая реакция не идет. Это значит, что они перестают реагировать с кислотой. Азотную кислоту можно транспортировать в стальных цистернах.
Как дымящая, так и концентрированная азотная кислота является сильным окислителем. Тлеющий уголь вспыхивает при соприкосновении с азотной кислотой. Капли скипидара, попадая в азотную кислоту, воспламеняются, образуя большое пламя (рис. 20.3). Концентрированная кислота окисляет при нагревании серу и фосфор.

Рис. 20.3.
Азотная кислота в смеси с концентрированной серной кислотой проявляет основные свойства. От молекулы HN0 3 отщепляется гидроксид-ион, и образуется ион нитроил (нитроний) NOJ:
Равновесная концентрация нитрония небольшая, но такая смесь нитрует органические вещества при участии этого иона. Из данного примера следует, что в зависимости от характера растворителя поведение вещества может коренным образом измениться. В воде HN0 3 проявляет свойства сильной кислоты, а в серной кислоте оказывается основанием.
В разбавленных водных растворах азотная кислота практически полностью ионизирована.
В концентрированных растворах азотной кислоты в качестве окислителя действуют молекулы HN0 3 , а в разбавленных - ионы N0 3 при поддержке кислой среды. Поэтому азот в зависимости от концентрации кислоты и природы металла восстанавливается до разных продуктов. В нейтральной среде, т. е. в солях азотной кислоты, ион N0 3 становится слабым окислителем, но при добавлении сильной кислоты к нейтральным растворам нитратов последние действуют как азотная кислота. По силе окислительных свойств в кислой среде ион N0 3 сильнее, чем Н + . Отсюда вытекает следующее важное следствие.
При действии азотной кислоты на металлы вместо водорода выделяются различные оксиды азота, а в реакциях с активными металлами азот восстанавливается до иона NH*.
Рассмотрим важнейшие примеры реакций металлов с азотной кислотой. Медь в реакции с разбавленной кислотой восстанавливает азот до NO (см. выше), а в реакции с концентрированной кислотой - до N0 2:
Железо пассивируется концентрированной азотной кислотой, а кислотой средней концентрации окисляется до степени окисления +3:
Алюминий реагирует с сильно разбавленной азотной кислотой без выделения газа, так как азот восстанавливается до СО -3, образуя соль аммония:

Соли азотной кислоты, или нитраты, известны для всех металлов. Нередко применяется старое название некоторых нитратов - селитра (натриевая селитра, калийная селитра). Это единственное семейство солей, в котором все соли растворимы в воде. Ион N0 3 не окрашен. Поэтому нитраты или оказываются бесцветными солями, или имеют окраску входящего в их состав катиона. Большинство нитратов выделяются из водных растворов в виде кристаллогидратов. Безводными нитратами являются NH 4 N0 3и нитраты щелочных металлов, кроме LiN0 3 *3H 2 0.
Нитраты часто применяют для проведения обменных реакций в растворах. Нитраты щелочных металлов, кальция и аммония в больших количествах используются в качестве удобрений. На протяжении нескольких веков нитрат калия имел огромное значение в военном деле, так как был компонентом единственного взрывчатого состава - пороха. Его получали главным образом из мочи лошадей. Содержащийся в моче азот при участии бактерий в особых селитряных кучах переходил в нитраты. При выпаривании получавшейся жидкости в первую очередь кристаллизовался нитрат калия. Этот
пример показывает, насколько ограничены были источники получения соединений азота до освоения промышленностью синтеза аммиака.
Термическое разложение нитратов происходит при температурах ниже 500°С. При нагревании нитратов активных металлов они превращаются в нитриты с выделением кислорода (см. выше). Нитраты менее активных металлов при термическом разложении дают оксид металла, оксид азота(1У) и кислород:
Если нагревать калиевую или натриевую селитру, они теряют часть своего кислорода и переходят в соли азотистой кислоты HNO 2 . Разложение идет легче в присутствии свинца, связывающего выделяющийся :
KNO 3 + Pb = KNO 2 + PbO
Соли азотистой кислоты - нитриты - кристаллические , хорошо растворимые в воде (за исключением серебряной соли). NaNO 2 широко применяется при производстве различных красителей.
При действии на раствор какого-нибудь нитрита разбавленной серной кислотой получается свободная азотистая кислота:
2NaNO 2 + H 2 SO 4 = Na 2 SO 4 + 2HNO 2
Она принадлежит к числу слабых кислот (К = 5 10 -4) и известна только в сильно разбавленных водных растворах. При концентрировании раствора или при его нагревании азотистая кислота распадается с выделением окиси и двуокиси азота:
2HNO 2 = NO + NO 2 + H 2 O
Азотистая кислота - сильный , но в же время при действии других, более энергичных окислителей сама может окисляться в азотную кислоту.
Вы читаете, статья на тему Азотистая кислота HNO2
Азотистая кислота HN0 2 известна лишь в разбавленных растворах. Она неустойчива, поэтому в чистом виде не существует. Формула азотистой кислоты может быть представлена в виде двух таутомерных форм:
Нитрит-ион N0 2 имеет угловую форму:

При нагревании азотистая кислота расщепляется:
Азот в азотистой кислоте имеет степень окисления +3, что соответствует промежуточному состоянию между наивысшей (+5) и низшей (-3) степенями окисления. Поэтому азотистая кислота проявляет как окислительные, так и восстановительные свойства.
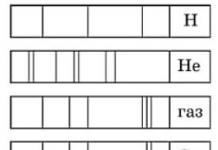
Окислитель:
Восстановитель:
![]()
Соли азотистой кислоты - нитриты - являются устойчивыми соединениями и за исключением AgN0 2 легко растворимы в воде. Как и сама азотистая кислота, нитриты обладают окислительно-восстановительными свойствами.
Окислитель:
Восстановитель:
Реакция с KI в кислой среде находит широкое применение в аналитической химии для обнаружения нитрит-иона N0 2 (выделяющийся свободный иод окрашивает раствор крахмала).
Большинство солей азотистой кислоты ядовиты. Наибольшее применение имеет нитрит натрия NaN0 2 , который широко используют в производстве органических красителей, лекарственных веществ, в аналитической химии. В медицинской практике применяется как сосудорасширяющее средство при стенокардии.
Азотную кислоту HN0 3 в лабораторных условиях можно получить действием концентрированной серной кислоты на NaN0 3:
Азотную кислоту в промышленных масштабах получают каталитическим окислением аммиака кислородом воздуха. Этот метод получения HN() 3 состоит из нескольких стадий. Вначале смесь аммиака с воздухом пропускают над платиновым катализатором при 800°С. Аммиак при этом окисляется до NO:
При охлаждении происходит дальнейшее окисление NO до N0 2:
![]()
Образующийся N0 2 растворяется в воде с образованием HN0 3:
Чистая азотная кислота - это бесцветная жидкость, которая при 42°С переходит в кристаллическое состояние. На воздухе она «дымит», так как пары ее с влагой воздуха образуют мелкие капельки тумана. С водой смешивается в любых соотношениях. HN0 3 имеет плоское строение:

Азот в HN0 3 является однозарядным и четырехковалентным. Нитрат- ион N0 3 имеет форму плоского треугольника, что объясняется ^-гибридизацией валентных орбиталей азота:

Азотная кислота относится к числу наиболее сильных кислот. В водных растворах она полностью диссоциирована на ионы Н + и N0 3 .
Для азотной кислоты характерны исключительно окислительные свойства. Азот в азотной кислоте находится в состоянии наивысшего окисления +5, поэтому он может только присоединять электроны. Уже под влиянием света азотная кислота разлагается с выделением N0 2 и 0 2:
В зависимости от концентрации азотной кислоты и природы восстановителя образуются различные продукты, где азот проявляет степень окисления от +4 до
Концентрированная азотная кислота окисляет большинство металлов (кроме золота и платины).
При взаимодействии концентрированной HN0 3 с малоактивными металлами, как правило, образуется N0 2:
Однако разбавленная азотная кислота в этом случае восстанавливается до NO:
Если в реакцию окисления с разбавленной азотной кислотой вступают более активные металлы, то выделяется N 3 0:
Очень разбавленная азотная кислота при взаимодействии с активными металлами восстанавливается до солей аммония:
Железо легко взаимодействует с разбавленной азотной кислотой и не реагирует на холоде с концентрированной. Аналогично ведут себя хром и алюминий. Объясняется это тем, что на поверхности этих металлов образуются оксидные пленки, которые и тормозят дальнейшее окисление металла (пассивация металла).
Таким образом, при взаимодействии азотной кислоты с металлами водород не выделяется.
Неметаллы при нагревании с HN0 3 окисляются до кислородных кислот. В зависимости от концентрации азотная кислота восстанавливается до N0 2 или NO:

Смесь, состоящая из одного объема азотной и трех объемов концентрированной соляной кислоты, называется царской водкой. Эта смесь - более сильный окислитель и растворяет такие благородные металлы, как золото и платину. Действие царской водки основано на том, что HN0 3 окисляет НС1 с выделением нитрозилхлорида, разлагающегося с образованием атомарного хлора и NO. Роль окислителя при взаимодействии с металлами выполняет хлор:

Взаимодействие с золотом протекает по реакции
Азотная кислота в зависимости от концентрации по-разному ведет себя по отношению к сульфидам, проявляющим восстановительные свойства. Так, разбавленная азотная кислота (до 20%) окисляет сульфид-ион S 2- до нейтральной серы, а сама восстанавливается до NO. Более концентрированная азотная кислота (30%-ный раствор) окисляет S 2 до SOf , восстанавливаясь при этом до NO:
В безводной азотной кислоте протекают следующие равновесные процессы:
Для распознавания нитрат-иона N0 3 и отличия его от нитрит-иона N0 2 пользуются несколькими реакциями:
а) нитраты в щелочной среде могут быть восстановлены до аммиака металлами - цинком или алюминием:
- (выделяющийся газообразный аммиак можно обнаружить по посинению влажной лакмусовой бумаги);
- б) сульфат железа(П) в кислой среде окисляется азотной кислотой до сульфата железа(Ш). Азотная кислота восстанавливается до NO, который с избытком FeSO^ образует комплексное соединение бурого цвета:
Соли азотной кислоты, называемые нитратами, - кристаллические вещества, хорошо растворимые в воде. При нагревании они разлагаются с выделением 0 9 . Нитраты, содержащие щелочные металлы и металлы, стоящие в ряду стандартных электродных потенциалов левее магния (включая магний), с отщеплением кислорода переходят в соответствующие нитриты:
Нитраты металлов, стоящих в ряду стандартных электродных потенциалов правее меди, расщепляются с образованием свободных металлов:
Нитраты остальных металлов разлагаются до оксидов:

Для качественного обнаружения применяется реакция
в результате которой выделяется бурый газ (N0 9).
Так как нитраты легко отщепляют кислород при высоких температурах и, следовательно, являются окислителями, то их применяют для изготовления легко воспламеняющихся и взрывчатых смесей. Например, порох представляет собой смесь состава 68% KN0 3 , 15% S и 17% С.
Наиболее важное значение имеют NaNO ;j (чилийская селитра), KN0 3 (калийная селитра), NH 4 N0 3 (аммонийная селитра) и Ca(NO:i) 2 (кальциевая селитра). Все эти соединения используются в сельском хозяйстве в качестве удобрений.
Биологическая роль азота. Азот - это макроэлемент, входит в состав аминокислот белков, РНК и ДНК, гормонов, ферментов, витаминов и многих других жизненно важных субстратов.